Clear Sky Science · pl
Mechanizm aktywacji Src pośredniczonej przez beta-arrestynę 1 poprzez domenę SH3 Src ujawniony za pomocą kriotransmisyjnej mikroskopii elektronowej
Jak komórki zamieniają sygnały w działanie
Nasze komórki nieustannie wyczuwają hormony i neurotransmitery za pośrednictwem receptorów na powierzchni i muszą zdecydować, kiedy reagować, kiedy przerwać odpowiedź i które wewnętrzne szlaki uruchomić. W tym badaniu skupiono się na dwóch kluczowych uczestnikach tego procesu decyzyjnego — beta-arrestynie 1 i enzymie Src — aby w szczegółach atomowych pokazać, jak jeden białkowy partner fizycznie przełącza „włącznik” drugiego. Zrozumienie tej choreografii pomaga wyjaśnić, jak działa codzienna sygnalizacja komórkowa, i może rzucić światło na zaburzenia występujące w chorobach takich jak rak, gdzie Src bywa często nadaktywny.
Regulator ruchu, który jest też wyłącznikiem
Receptory sprzężone z białkami G (GPCR) to ogromna rodzina czujników na powierzchni komórek, kontrolująca procesy od widzenia po pracę serca. Przez długi czas beta-arrestyny postrzegano głównie jako komórkowych regulatorów ruchu: przyczepiają się do aktywowanych GPCR, wyłączają dalszą sygnalizację i kierują receptory do wnętrza komórki. Jednak w ciągu ostatniej dekady okazało się, że beta-arrestyny same w sobie są przenośnikami sygnału, potrafią łączyć GPCR z wieloma enzymami efektorowymi. Jednym z najważniejszych partnerów jest Src, kinaza tyrozynowa, która może napędzać wzrost komórek, ich migrację i przeżycie. Dokładny sposób, w jaki beta-arrestyna 1 (β-arrestyna 1, lub βarr1) komunikuje się z Src — i faktycznie go aktywuje — pozostawał jednak tajemnicą, ponieważ interakcja ta jest efemeryczna i stosunkowo słaba.
Dwa uściski dłoni na jednym białku
Wykorzystując kriotransmisyjną mikroskopię elektronową, zdolną wizualizować zespoły białkowe z niemal atomową rozdzielczością, autorzy uchwycili βarr1 związane z domeną SH3 Src, małym modułem dokującym występującym w wielu białkach sygnałowych. Odkryli, że βarr1 nie polega na jednym punkcie kontaktowym. Zamiast tego oferuje dwa oddzielne „uściski dłoni” na różnych częściach swojej struktury. Jedno miejsce znajduje się w regionie N‑terminalnym βarr1 i zawiera krótki odcinek bogaty w proliny — aminokwasy często angażujące domeny SH3. Drugie miejsce, w obszarze zwanym centralnym grzebieniem, wykorzystuje inną kombinację aminokwasów, aby wesprzeć się na tej samej aromatycznej powierzchni domeny SH3. Pomiary biofizyczne i eksperymenty wymiany wodór–deuter potwierdzają, że oba obszary βarr1 stają się chronione w obecności SH3, nawet bez sztucznych skrzyżowań, co pokazuje, że te podwójne kontakty zachodzą w realistycznych warunkach.
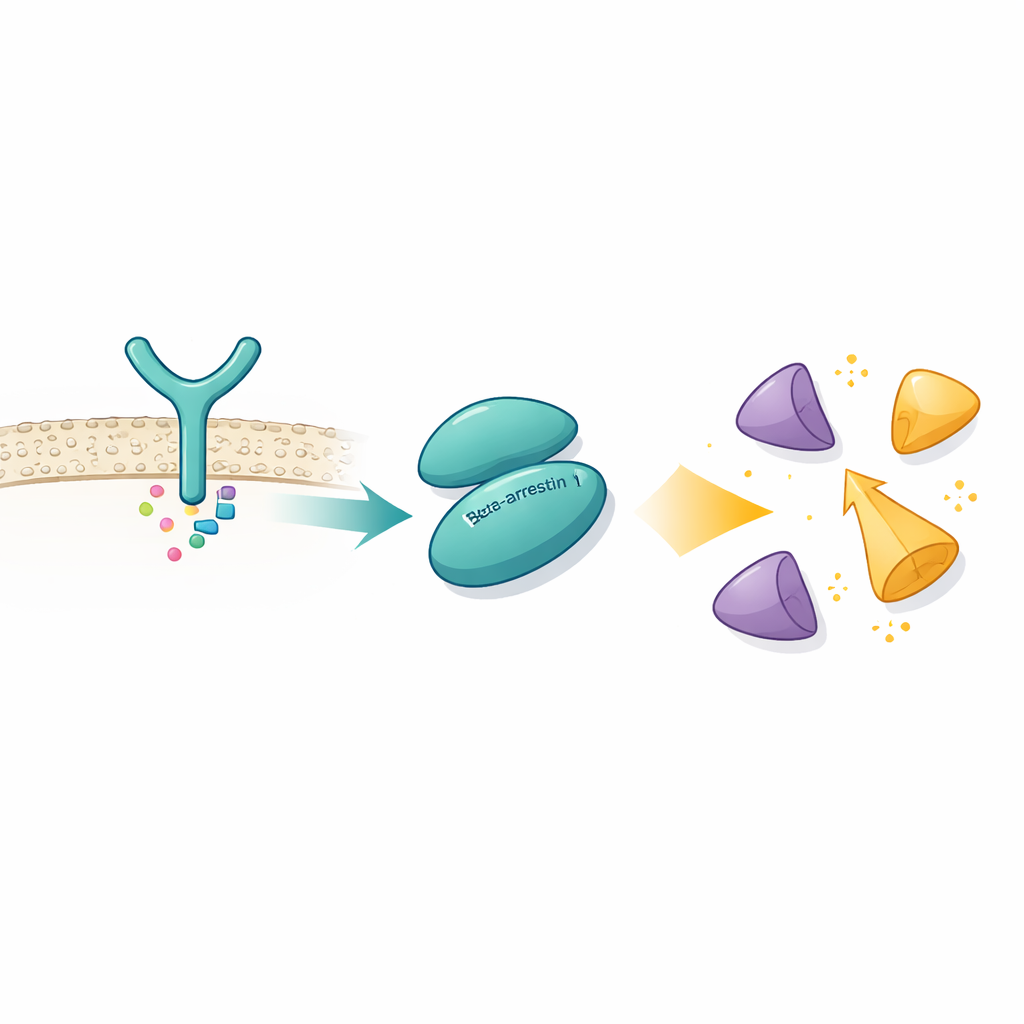
Odblokowanie autoinhibowanego enzymu
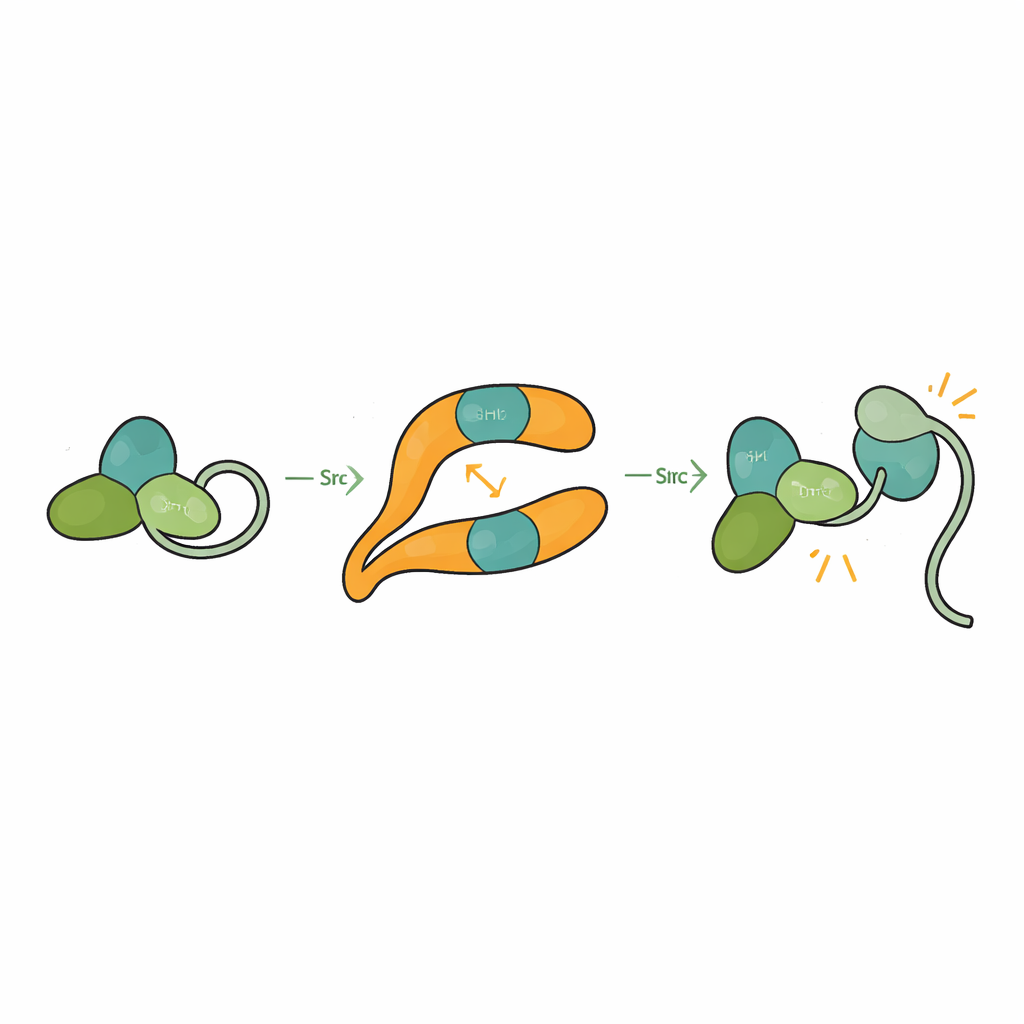
Src zwykle utrzymywany jest w samozaciskowej, czyli autoinhibowanej, konformacji, w której jego domeny SH3, SH2 i domena katalityczna przylegają do siebie, a segment ogonowy spinający strukturę zamyka ją. Zapobiega to przypadkowemu uruchomieniu, które mogłoby uszkodzić komórkę. Poprzez rozwiązanie struktury βarr1 związanej z trójdomenową formą Src badacze zaobserwowali, że gdy SH3 wiąże się z miejscem centralnego grzebienia na βarr1, nie może już zacisnąć wewnętrznego łącznika, który pomaga utrzymać Src w stanie zamkniętym. Domena katalityczna staje się bardziej ruchoma, a ogólny kształt ulega poluzowaniu, zgodnie ze stanem aktywnym. Testy biochemiczne pokazują, że βarr1 preferencyjnie wiąże Src, gdy jego ogon nie jest ufosforylowany — bardziej elastyczna forma, która chwilowo odsłania SH3. Gdy SH3 zaczepia o βarr1, zacisk utrzymujący Src w spoczynku zostaje podważony, co pozwala Src na autokinazę i pełną aktywację.
Elastyczne centrum przekierowujące sygnały
Badanie ujawnia także, że sama βarr1 nie jest sztywna. Gdy SH3 się wiąże, kluczowe łańcuchy i pętle wewnątrz βarr1 przesuwają się o kilka angstremów, szczególnie wokół centralnego grzebienia. Te subtelne ruchy mogą zmieniać, jak mocno βarr1 trzyma GPCR. Eksperymenty z fluorescencyjnie znakowaną βarr1 pokazują, że nadmiar SH3 może osłabić sposób, w jaki βarr1 wkłada część siebie do rdzenia receptora — konfiguracja uznawana za istotną do wyłączania sygnalizacji białek G. W komórkach żywych nadekspresja Src wydłuża wzrost drugiego przekaźnika o nazwie cAMP po aktywacji receptora beta-adrenergicznego, co wskazuje na opóźnioną desensytyzację. Razem te obserwacje sugerują, że wysokie lokalne poziomy Src mogą przechylić zespoły GPCR–βarr1 z trybu pełnego „wyłączenia” i pozwolić białkom G na dłuższe utrzymanie sygnalizacji.
Dlaczego to ma znaczenie dla zdrowia i terapii
Bezpośrednio wizualizując, jak βarr1 chwyta Src w dwóch miejscach i wyciąga go z autoinhibowanego ułożenia, ta praca ustanawia βarr1 jako aktywnego regulatora, a nie tylko bierną podstawę. Pokazuje, że pojedyncze białko adaptorowe może łączyć wiele stosunkowo słabych kontaktów w solidną i regulowaną kontrolę nad potężną kinazą. Ponieważ Src jest często nadmiernie eksprymowany lub nieprawidłowo regulowany w nowotworach, poznanie tej drogi aktywacji może zainspirować strategie selektywnego zakłócania komunikacji βarr1–Src bez wyłączania innych funkcji Src. Szerzej, odkryte tu rozpoznawanie z dwóch miejsc może być ogólnym wzorcem tego, jak beta-arrestyny angażują wielu swoich partnerów, oferując nowe podejścia do projektowania leków, które przesuwają sygnalizację GPCR w stronę korzystnych szlaków przy jednoczesnym unikaniu szkodliwych efektów.
Cytowanie: Pakharukova, N., Thomas, B.N., Bansia, H. et al. Mechanism of beta-arrestin 1 mediated Src activation via Src SH3 domain revealed by cryo-electron microscopy. Nat Commun 17, 2973 (2026). https://doi.org/10.1038/s41467-026-69884-1
Słowa kluczowe: beta-arrestyna, kinaza Src, sygnalizacja GPCR, kriotransmisyjna mikroskopia elektronowa, sygnalizacja komórkowa