Clear Sky Science · ja
クライオ電子顕微鏡で明らかになったSrc SH3ドメインを介するβ-アレスチン1によるSrc活性化の機構
細胞はどうやってシグナルを作用に変えるか
細胞は表面の受容体を通じてホルモンや神経伝達物質を常に感知し、いつ応答するか、いつ止めるか、どの内部経路をオンにするかを決定しなければなりません。本研究は、その決定過程で重要な二つの担い手――β-アレスチン1と酵素Src──に着目し、一つのタンパク質がどのようにして別のタンパク質の「オン」スイッチを物理的に入れるかを原子レベルで明らかにします。この振る舞いを理解することは日常的なシグナル伝達の仕組みを説明する助けとなり、Srcが過剰に活性化することの多い癌などの疾患で何が誤るかを照らす可能性があります。
交通整理役でありつつスイッチでもある分子
Gタンパク質共役受容体(GPCR)は視覚から心拍数までのプロセスを制御する巨大な細胞表面センサー群です。β-アレスチンは長く細胞内の交通整理役と考えられてきました:活性化されたGPCRに結合してさらなるシグナルを遮断し、受容体を細胞内へ誘導します。しかしここ10年ほどで、β-アレスチンはそれ自体が信号を運ぶ担い手として浮上し、GPCRを多くの下流酵素に結びつけることができると分かってきました。その重要なパートナーの一つがSrcであり、細胞増殖、運動、生存を促進し得るチロシンキナーゼです。それでもβ-アレスチン1(βarr1)がSrcとどのように会話し、実際に活性化するかは、相互作用が短時間で比較的弱いことから明確ではありませんでした。
一つのタンパク質に対する二つの握手
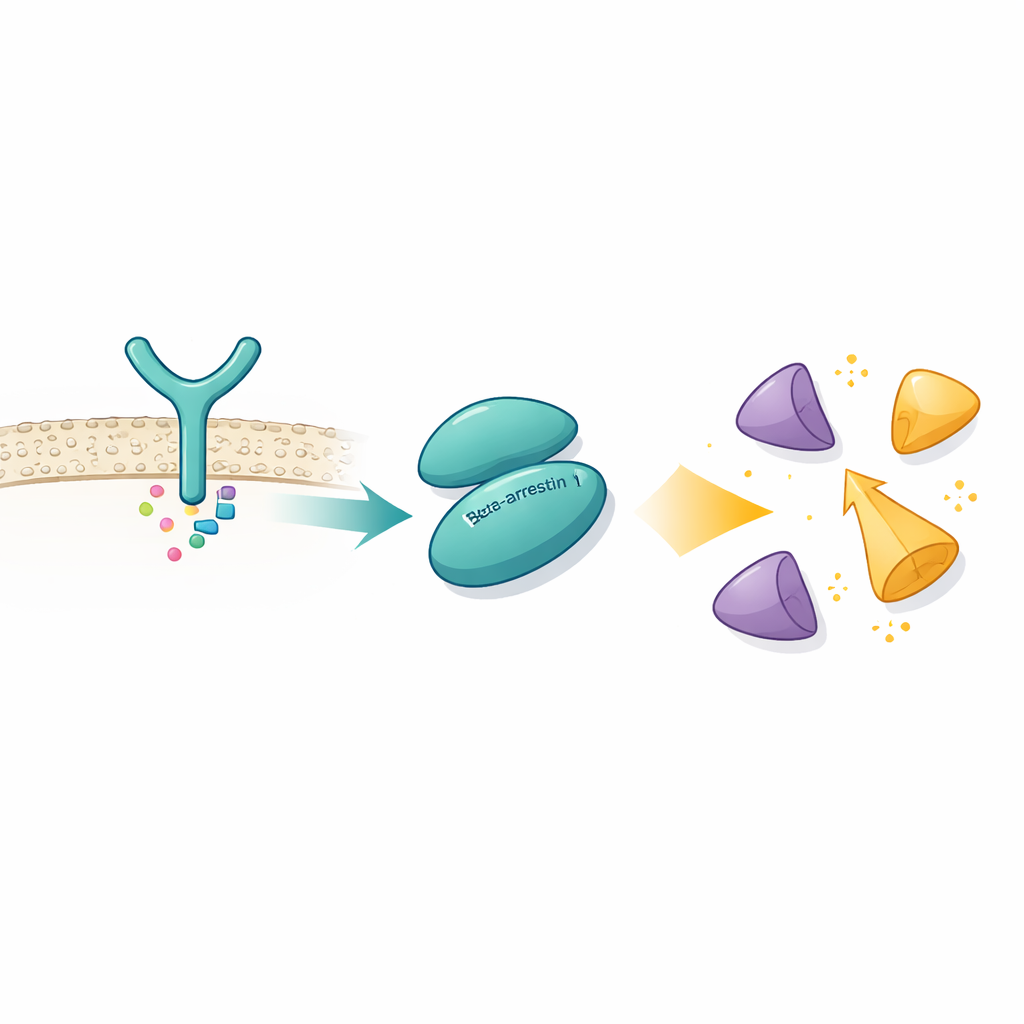
クライオ電子顕微鏡を用いて、近原子分解能でタンパク質複合体を可視化した著者らは、βarr1がSrcのSH3ドメインに結合した状態を捉えました。彼らはβarr1が単一の接触点に依存しないことを発見しました。代わりに、βarr1は構造の異なる二箇所でそれぞれ別の“握手”を差し出しています。一つの部位はβarr1のN末端領域にあり、プロリンに富む短い配列を含みます。プロリンはしばしばSH3ドメインと相互作用します。第二の部位は中央クレストと呼ばれる領域にあり、異なるアミノ酸の組み合わせを用いて同じSH3ドメインの芳香族表面に着地します。生物物理学的測定と水素-重水素交換実験は、エンジニアリングされた架橋がなくてもSH3が存在すると両領域が保護されることを示し、この二重接触が現実的な条件下で起こることを裏付けます。
オートインヒビテッド酵素の解除
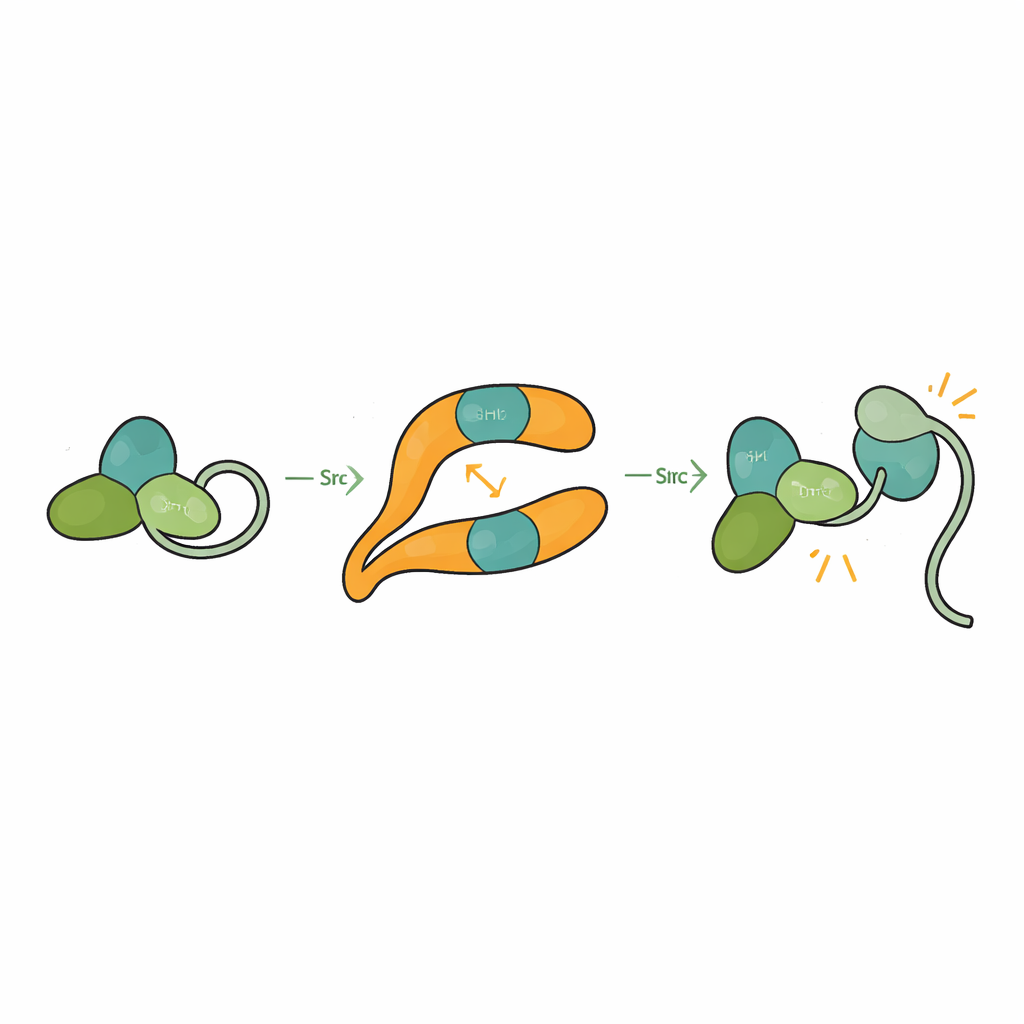
Srcは通常、SH3、SH2、触媒ドメインが互いに密着し、尾部配列が構造を閉じるように留める自己抑制(オートインヒビション)形状で保持されています。これは偶発的な活性化が細胞を損なうのを防ぎます。βarr1が三つのドメインを持つSrcの形に結合した構造を解いたところ、SH3がβarr1の中央クレスト部位に結合すると、Srcを閉じたままにするのに寄与する内部リンカーをSH3が掴めなくなることが観察されました。触媒ドメインはより可動になり全体の形状は緩み、活性型に一致する変化を示します。生化学的アッセイは、βarr1が尾部がリン酸化されていない、より柔軟で一時的にSH3が露出する状態のSrcを好んで結合することを示しています。一旦SH3がβarr1に噛み付くと、Srcを静めているクランプはこじ開けられ、Srcは自己リン酸化して完全に活性化されます。
シグナルの経路を振り分ける柔軟なハブ
本研究はまた、βarr1自身が剛直ではないことを明らかにします。SH3が結合すると、βarr1の重要なβストランドやループが特に中央クレスト周辺で数オングストロームずつ移動します。これらの微妙な動きは、βarr1がGPCRを掴む強さを変える可能性があります。蛍光標識したβarr1を用いた実験では、過剰なSH3がβarr1の一部が受容体コアに挿入される様式を弱め得ることが示され、この構成はGタンパク質シグナルを遮断する上で重要と考えられています。生細胞内では、Srcを過剰発現させるとβ-アドレナリン受容体を活性化した後にセカンドメッセンジャーであるcAMPの上昇が長引き、脱感作が遅れることが示されました。これらの知見は、高局所濃度のSrcがGPCR–βarr1複合体を完全な“オフ”モードから傾け、Gタンパク質がより長くシグナルを維持することを許すことを示唆しています。
健康と治療における意義
βarr1がSrcを二箇所で直接つかみ、自己抑制状態から引き出す様子を可視化することで、本研究はβarr1を単なる受動的な足場ではなく能動的な調節因子として位置づけます。一つのアダプタータンパク質が複数の比較的弱い接触を組み合わせて強固で調節可能な強力酵素に対する制御を実現できることを示しています。Srcは多くの癌で過剰発現または誤調節されるため、この活性化経路の理解はβarr1–Srcの通信を選択的に断つような戦略を生み出し、他のSrc機能を止めずに対処する手がかりを与える可能性があります。より広くは、ここで明らかになった二箇所認識はβ-アレスチンが多くのパートナーと関わる一般的な設計図であるかもしれず、GPCRシグナルを有益な経路へ偏らせ有害な経路を避ける薬剤設計に新たな視点を提供します。
引用: Pakharukova, N., Thomas, B.N., Bansia, H. et al. Mechanism of beta-arrestin 1 mediated Src activation via Src SH3 domain revealed by cryo-electron microscopy. Nat Commun 17, 2973 (2026). https://doi.org/10.1038/s41467-026-69884-1
キーワード: β-アレスチン, Srcキナーゼ, GPCRシグナル伝達, クライオ電子顕微鏡, 細胞シグナル伝達