Clear Sky Science · sv
Mechanism of beta-arrestin 1 mediated Src activation via Src SH3 domain revealed by cryo-electron microscopy
Hur celler omvandlar signaler till handling
Våra celler känner ständigt av hormoner och neurotransmittorer via receptorer på ytan och måste avgöra när de ska reagera, när de ska sluta och vilka interna vägar som ska aktiveras. Denna studie undersöker två nyckelspelare i den beslutsprocessen—beta-arrestin 1 och enzymet Src—för att på atomnivå visa hur ett protein fysiskt vrider på "på"-knappen för ett annat. Att förstå detta samspel hjälper oss att förklara hur vanlig signalering fungerar och kan ge ledtrådar till vad som går fel i sjukdomar som cancer, där Src ofta är överaktivt.
En trafikpolis som också är en strömbrytare
G-protein-kopplade receptorer (GPCR) är en stor familj av yt-sensorer som styr processer från syn till hjärtfrekvens. Beta-arrestiner sågs länge främst som cellulära trafikpoliser: de fäster vid aktiverade GPCR, stänger av fortsatt signalering och guidar receptorer in i cellen. Under det senaste decenniet har beta-arrestiner emellertid framträtt som signalbärare i egen rätt och kan koppla GPCR till många nedströms enzym. En av de viktigaste partnerna är Src, en tyrosinkinas som kan driva celltillväxt, rörelse och överlevnad. Men exakt hur beta-arrestin 1 (β-arrestin 1, eller βarr1) kommunicerar med Src—och faktiskt aktiverar det—har förblivit ett mysterium eftersom interaktionen är flyktig och relativt svag.
Två handslag på ett protein
Genom att använda kryoelektronmikroskopi, som kan visualisera proteinkomplex i nästan atomupplösning, fångade forskarna βarr1 bunden till SH3-domänen i Src, en liten dockningsmodul som finns i många signalproteiner. De upptäckte att βarr1 inte förlitar sig på en enda kontaktpunkt. Istället erbjuder det två separata handslag på olika delar av sin struktur. En sajt sitter i den N-terminala regionen av βarr1 och innehåller ett kort stycke rikt på prolin—aminosyror som ofta engagerar SH3-domäner. Den andra sajten, i ett område kallat central crest, använder en annan blandning av aminosyror för att landa på samma aromatiska yta av SH3-domänen. Biofysiska mätningar och väte–deuteriumbytesexperiment bekräftar att båda områdena i βarr1 blir skyddade när SH3 är närvarande, även utan konstruerade korslänkar, vilket visar att dessa dubbla kontakter uppstår under realistiska förhållanden.
Låsa upp ett autoinhiberat enzym
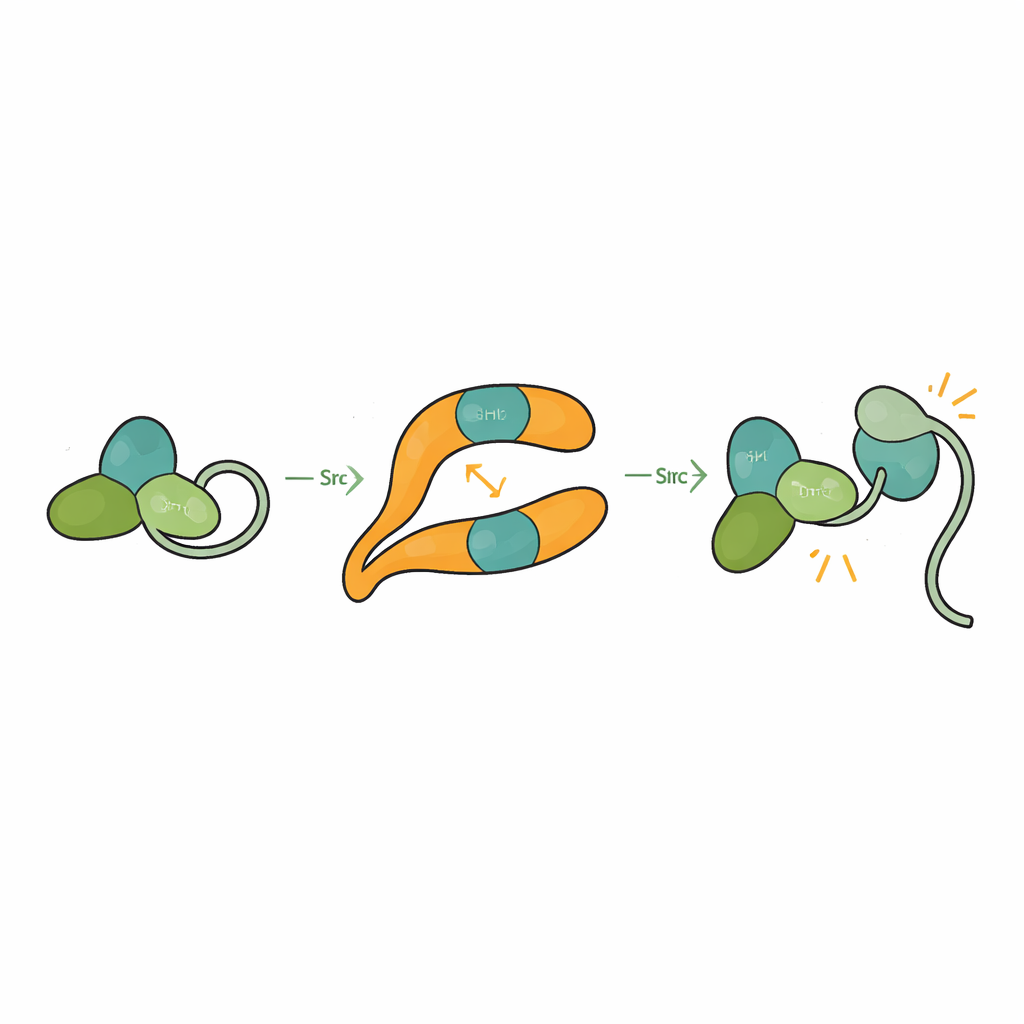
Src hålls normalt i en självklämd, eller autoinhiberad, konformation där dess SH3-, SH2- och katalytiska domäner packas mot varandra och en svanssekvens håller strukturen stängd. Detta förhindrar oavsiktlig aktivering som kan skada cellen. Genom att bestämma strukturen av βarr1 bunden till en tredomänform av Src såg forskarna att när SH3 engagerar central crest-sajten på βarr1 kan den inte längre hålla i den interna länken som hjälper till att hålla Src stängt. Den katalytiska domänen blir mer rörlig och den övergripande formen lossnar, vilket stämmer med ett aktivt tillstånd. Biokemiska analyser visar att βarr1 föredrar att binda Src när dess svans inte är fosforylerad, en mer flexibel form som tillfälligt exponerar SH3. När SH3 väl hakar i βarr1 pränger det upp det spärrande greppet som håller Src tyst, vilket tillåter Src att autofosforylera och fullt ut aktiveras.
En flexibel knutpunkt för signalrouting
Studien visar också att βarr1 själv inte är stel. När SH3 binder förskjuts viktiga strängar och slingor inom βarr1 med flera ångström, särskilt kring central crest. Dessa subtila rörelser kan förändra hur hårt βarr1 håller i GPCR. Experiment med fluorescensmärkt βarr1 visar att ett överskott av SH3 kan försvaga hur βarr1 skjuter in en del av sig själv i receptor-kärnan, en konfiguration man tror är viktig för att stänga av G-protein-signalering. I levande celler förlänger överuttryck av Src ökningen av en second messenger kallad cAMP efter aktivering av en beta-adrenerg receptor, vilket indikerar fördröjd desensitisering. Tillsammans tyder dessa fynd på att höga lokala nivåer av Src kan luta GPCR–βarr1-komplex bort från fullt "av"-läge och tillåta G-protein att fortsätta signalera längre.
Varför detta betyder något för hälsa och terapi
Genom att direkt visualisera hur βarr1 greppar Src på två platser och drar det ur dess självhiberade pose etablerar detta arbete βarr1 som en aktiv regulator, inte bara ett passivt stödelement. Det visar att ett enda adaptorprotein kan kombinera flera, relativt svaga kontakter till en robust och justerbar kontroll över ett kraftfullt enzym. Eftersom Src ofta är överuttryckt eller felreglerat i cancer kan förståelsen av denna aktiveringsväg inspirera strategier som selektivt stör βarr1–Src-kommunikation utan att stänga av andra Src-funktioner. Mer allmänt kan den dubbla sajtkännedomen som blottläggs här vara en generell mall för hur beta-arrestiner engagerar många av sina partner, vilket ger nya vinklar för att designa läkemedel som vinklar GPCR-signalering mot fördelaktiga vägar samtidigt som skadliga undviks.
Citering: Pakharukova, N., Thomas, B.N., Bansia, H. et al. Mechanism of beta-arrestin 1 mediated Src activation via Src SH3 domain revealed by cryo-electron microscopy. Nat Commun 17, 2973 (2026). https://doi.org/10.1038/s41467-026-69884-1
Nyckelord: beta-arrestin, Src kinase, GPCR signaling, cryo-electron microscopy, cell signaling