Clear Sky Science · nl
Mechanisme van beta-arrestine-1-gemedieerde Src-activatie via de Src SH3-domijn onthuld door cryo-elektronenmicroscopie
Hoe cellen signalen omzetten in actie
Onze cellen registreren voortdurend hormonen en neurotransmitters via receptoren op hun oppervlak en moeten beslissen wanneer ze reageren, wanneer ze moeten stoppen en welke interne routes ze inschakelen. Deze studie onderzoekt twee sleutelspelers in dat besluitvormingsproces — beta-arrestine 1 en het enzym Src — en onthult op atomaire schaal hoe het ene eiwit fysiek de "aan"-schakelaar van het andere omzet. Inzicht in deze choreografie helpt verklaren hoe alledaagse signalering werkt en kan licht werpen op wat er misgaat bij ziekten zoals kanker, waarbij Src vaak overactief is.
Een verkeersagent die ook een schakelaar is
G-eiwitgekoppelde receptoren (GPCR's) vormen een enorme familie van sensors op het celoppervlak die processen regelen van zicht tot hartslag. Beta-arrestines werden lange tijd vooral gezien als cellulair verkeeragenten: ze hechten zich aan geactiveerde GPCR's, schakelen verdere signalering uit en leiden receptoren de cel in. In het afgelopen decennium zijn beta-arrestines echter naar voren gekomen als signaaldraaiers op zich, in staat om GPCR's met vele downstream-enzymen te verbinden. Een van de belangrijkste partners is Src, een tyrosinekinase dat celgroei, beweging en overleving kan aandrijven. Toch bleef de precieze manier waarop beta-arrestine 1 (β-arrestine 1, of βarr1) met Src communiceert — en het daadwerkelijk activeert — een raadsel omdat de interactie vluchtig en relatief zwak is.
Twee handdrukken op één eiwit
Met cryo-elektronenmicroscopie, die eiwitassemblages op bijna atomair niveau kan visualiseren, vingen de auteurs βarr1 vastgebonden aan het SH3-domein van Src, een kleine dockingsmodule die in veel signaalproteïnen voorkomt. Ze ontdekten dat βarr1 niet op één contactpunt vertrouwt. In plaats daarvan biedt het twee afzonderlijke handdrukken op verschillende delen van zijn structuur. De ene site bevindt zich in het N-terminale gebied van βarr1 en bevat een korte reeks rijk aan proline — aminozuren die vaak SH3-domeinen binden. De tweede site, in een regio die de centrale kam wordt genoemd, gebruikt een andere mix van aminozuren om op hetzelfde aromatische oppervlak van het SH3-domein te landen. Biofysische metingen en waterstof-deuteriumuitwisselingsexperimenten bevestigen dat beide gebieden van βarr1 beschermd raken wanneer SH3 aanwezig is, zelfs zonder geconstrueerde cross-links, wat aantoont dat deze dubbele contacten onder realistische omstandigheden voorkomen.
Een autonoom geremde enzym ontgrendelen
Src wordt normaal gesproken in een zelfgeklampte, of autogeremde, vorm gehouden waarbij zijn SH3-, SH2- en katalytische domeinen tegen elkaar aanpakken en een staartsegment de structuur gesloten houdt. Dit voorkomt accidentele activatie die de cel kan schaden. Door de structuur van βarr1 gebonden aan een driedomeinvorm van Src op te lossen, zagen de onderzoekers dat wanneer SH3 het centrale-kamgebied van βarr1 aangrijpt, het niet langer het interne linkereiwit kan vastklampen dat helpt Src gesloten te houden. Het katalytische domein wordt mobieler en de algehele vorm versoepelt, in overeenstemming met een actieve toestand. Biochemische assays tonen aan dat βarr1 voorkeur toont voor binding aan Src wanneer de staart niet gefosforyleerd is, een meer flexibele vorm die momentaan SH3 blootstelt. Zodra SH3 zich aan βarr1 hecht, wordt de klem die Src stilhoudt opengerukt, waardoor Src kan autophosporyleren en volledig activeren.
Een flexibel knooppunt voor signaalrouting
De studie laat ook zien dat βarr1 zelf niet stijf is. Wanneer SH3 bindt, verschuiven sleutelstrengen en lussen binnen βarr1 enkele angstroms, vooral rond de centrale kam. Deze subtiele bewegingen kunnen veranderen hoe strak βarr1 GPCR's vasthoudt. Experimenten met fluoresceen-gelabelde βarr1 tonen dat een overschot aan SH3 de manier kan verzwakken waarop βarr1 een deel van zichzelf in de receptorcore schuift, een configuratie waarvan wordt gedacht dat die belangrijk is voor het uitschakelen van G-eiwitsignalering. In levende cellen verlengt overexpressie van Src de toename van de tweede boodschapper cAMP na activatie van een beta-adrenerge receptor, wat wijst op vertraagde desensitisatie. Gezamenlijk suggereren deze bevindingen dat hoge lokale Src-niveaus GPCR–βarr1-assemblages uit balans kunnen brengen richting minder volledige "uit"-modus en G-eiwitten langer laten signaleren.
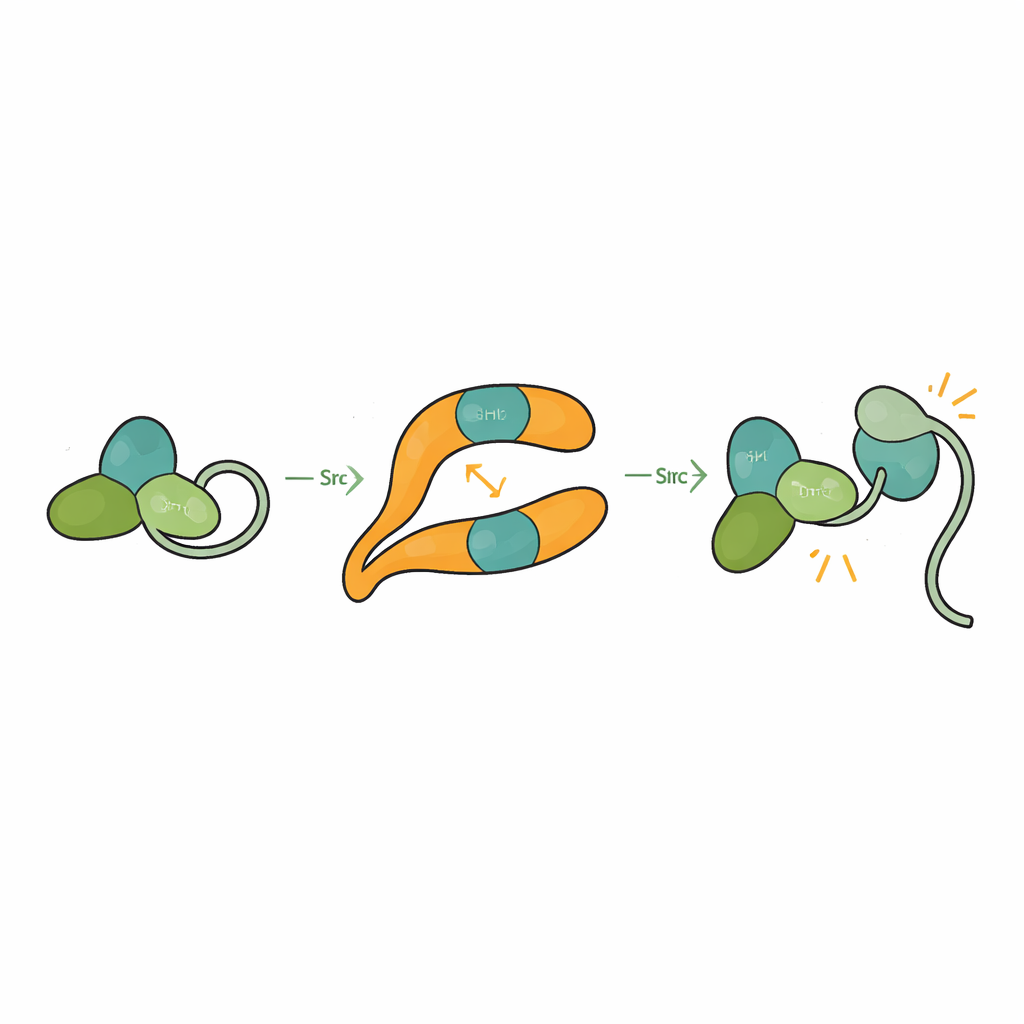
Waarom dit belangrijk is voor gezondheid en therapie
Door direct te visualiseren hoe βarr1 Src op twee plaatsen grijpt en uit zijn zelfgeremde houding trekt, stelt dit werk βarr1 neer als een actieve regulator, niet alleen een passief steiger. Het toont aan dat een enkele adaptor meerdere, relatief zwakke contacten kan combineren tot een robuuste en afstembare controle over een krachtig enzym. Omdat Src vaak overgeëxprimeerd of verkeerd gereguleerd is bij kanker, kan begrip van deze activatieroute strategieën inspireren die specifiek de βarr1–Src-communicatie verstoren zonder andere Src-functies uit te schakelen. Breder gezien kan de hier onthulde dubbele-siteherkenning een algemeen model zijn voor hoe beta-arrestines veel van hun partners binden, en nieuwe invalshoeken bieden voor het ontwerpen van geneesmiddelen die GPCR-signaalering naar gunstige paden sturen en schadelijke vermijden.
Bronvermelding: Pakharukova, N., Thomas, B.N., Bansia, H. et al. Mechanism of beta-arrestin 1 mediated Src activation via Src SH3 domain revealed by cryo-electron microscopy. Nat Commun 17, 2973 (2026). https://doi.org/10.1038/s41467-026-69884-1
Trefwoorden: beta-arrestine, Src-kinase, GPCR-signaaltransductie, cryo-elektronenmicroscopie, celsignalering