Clear Sky Science · tr
Mithramycin, EWS::FLI1 DNA bağlanmasını ve RNA polimeraz II processivity’sini değiştirerek yeni transkripsiyonu engelliyor
Kanser tedavisi için neden önemli
Ewing sarkomu, özellikle çocuklar ve genç erişkinleri etkileyen agresif bir kemik kanseridir. Hücrelerin DNA’yı okuma biçimini yeniden düzenleyen güçlü bir füzyon proteini, EWS::FLI1 tarafından sürülür. Bu çalışma, eski bir kemoterapi ilacı olan mithramycini yeniden ele alıyor ve—doğru şekilde verildiğinde—kanser sürücüsü programı seçici biçimde kapatırken hücrenin geri kalan makinarının çoğunu koruyabileceğini gösteriyor. Çalışma, yalnızca ilacın kendisinin değil, doz ve uygulama takviminin de geniş toksisite ile hassas hedefleme arasındaki farkı yaratabileceğini ortaya koyuyor.
Gizli bir yeteneğe sahip eski bir ilaç
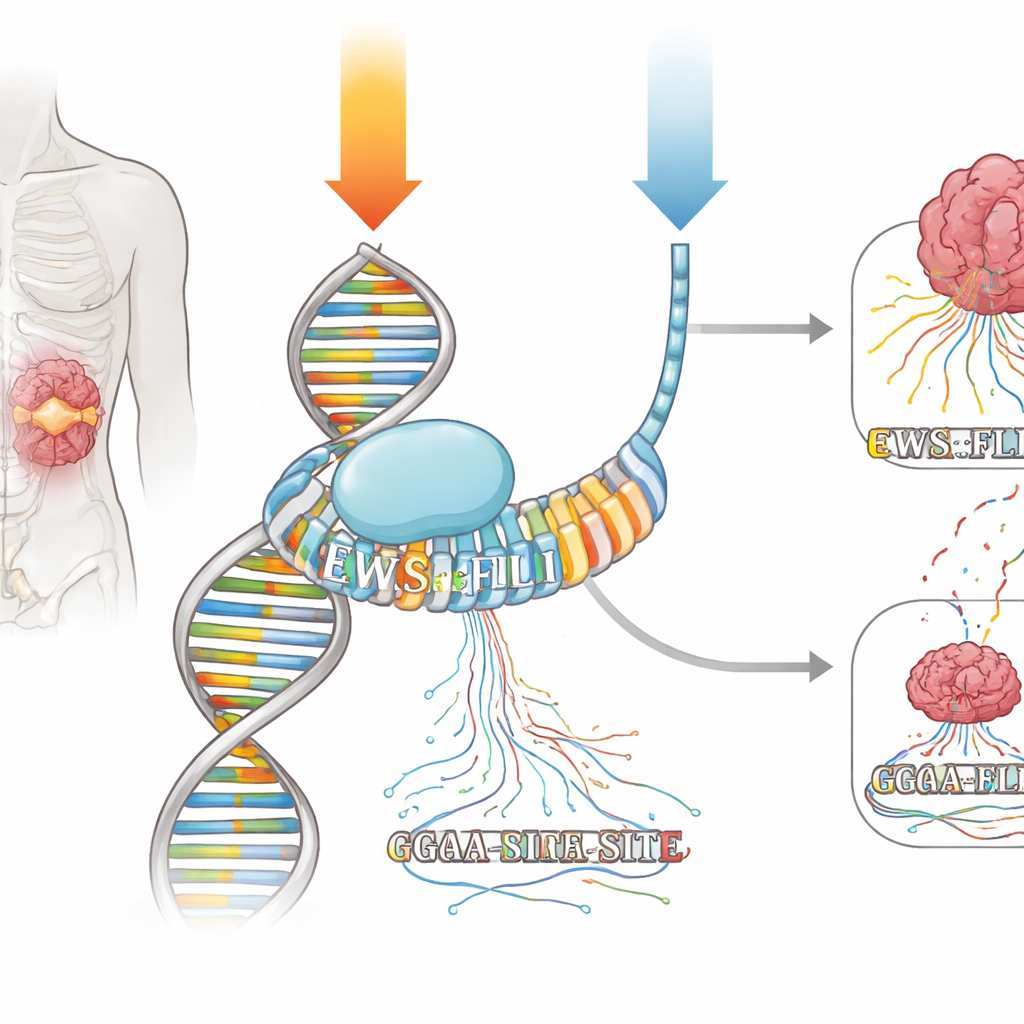
Mithramycin, özellikle G ve C açısından zengin kısa dizilere sahip DNA’nın minör oluğuna yerleşen doğal bir üründür. On yıllardır geniş spektrumlu bir “kemoterapi” aracı olarak kabul edilmiş, DNA’ya zarar verdiği ve transkripsiyonu genel olarak engellediği varsayılmıştır. Ancak 1960’larda doktorlar, mithramycin’in yedi günlük sürekli infüzyon olarak verildiği bir Ewing sarkomu hastasında tam yanıt bildirmişlerdir. Daha yakın zamanda aynı ilaç kısa günlük dozlar halinde test edildiğinde ise yalnızca sınırlı fayda görülmüştür. Yazarlar, modern genomik araçlarla mithramycin’in EWS::FLI1’e karşı bir hassas ilaç olarak hareket edip edemeyeceğini ve uygulama takviminin hasta yanıtlarındaki çarpıcı farkı açıklayıp açıklamadığını anlamak için yola çıktılar.
Füzyon sürücünün açılıp kapatılması nasıl gerçekleşiyor
EWS::FLI1, “GGAA” etrafında kurulu basit bir DNA kelimesine tutunan ETS ailesine ait bir transkripsiyon faktörüdür. Ewing sarkomunda EWS::FLI1, özellikle tekrar eden uzun GGAA dizilerine—mikrosatellitler denilen—güçlü biçimde bağlanarak gen ağlarını tümüyle açar veya kapatır. Ekip, ana EWS::FLI1 hedef genlerinin benzer baskılanmasını üreten iki mithramycin rejimine Ewing sarkomu hücrelerini maruz bıraktı: kısa süreli, yüksek doz bir atak ve çok daha uzun süre verilen daha düşük bir doz. EWS::FLI1’in DNA üzerindeki yerini ve yeni RNA moleküllerinin gerçek zamanda nerede üretildiğini eşzamanlı olarak haritalayan teknikleri kullanarak, her rejimin genom genelinde bağlanma ve transkripsiyonu nasıl değiştirdiğini izleyebildiler.
Transkripsiyon mekanizmasının ince ayarı
Eski in vitro çalışmalara ters düşerek, mithramycin klinik olarak ilgili düzeylerde basitçe evrensel bir transkripsiyon engelleyicisi olarak davranmadı. Özenle seçilmiş düşük konsantrasyonlarda, sürekli maruziyet öncelikle EWS::FLI1’in hedef bölgelerinde transkripsiyon başlatma biçimini değiştirdi. DNA’daki bazı EWS::FLI1 zirveleri zayıfladı, diğerleri güçlendi; her iki durumda da sonuç, programı “zehirlemek” oldu: füzyon tarafından normalde açılan genler aşağı indirildi, normalde baskılananlar serbest kaldı. Bununla birlikte daha yüksek konsantrasyonlarda mithramycin, DNA’yı RNA’ya çeviren enzim RNA polimeraz II’nin uzun genler boyunca ilerleme yeteneğini bozmayı başladı. Bu duraklama geniş, özgül olmayan etkilere yol açtı ve özellikle polimerazın genin başından sonuna kadar ilerlemesi gereken büyük genlerde EWS::FLI1 aktivitesinin istenen tersine çevrilmesini gölgeledi.
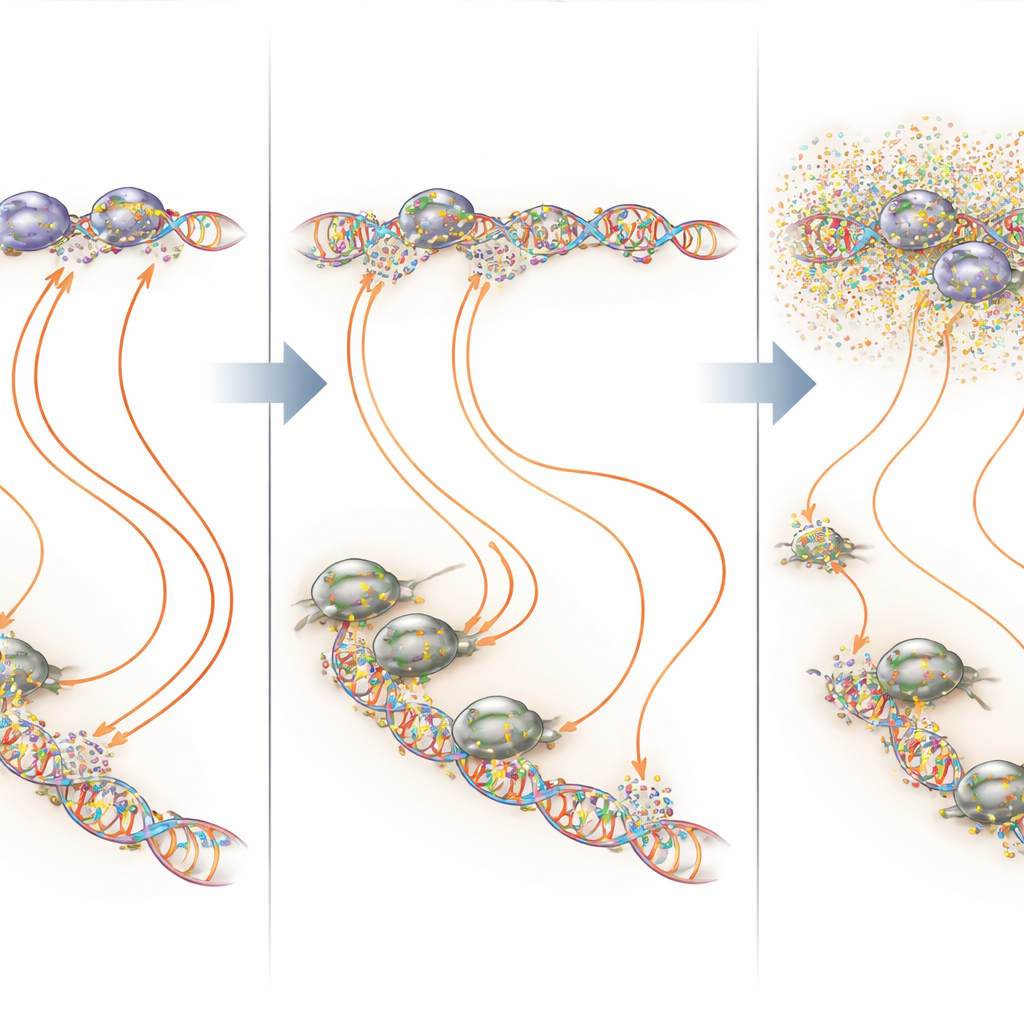
Tüm genom yerine DNA sıcak noktalarını hedeflemek
Bağlanma ve transkripsiyon haritalarını üst üste koyarak araştırmacılar, mithramycin’in en güçlü etkisini EWS::FLI1’in dayandığı GGAA zengini bölgelerde gösterdi. Bu mikrosatellitlerde ve izole GGAA bölgelerinde düşük doz sürekli mithramycin genellikle EWS::FLI1 tuttuğunu artırdı ancak yine de üretken transkripsiyonu kapattı—bir transkripsiyon faktörünün çok az veya çok fazla bağlanmasının işlevine zarar verebildiğini gösteren açık bir “Goldilocks” ilkesi örneği. EWS::FLI1’in AP-1, E2F veya RUNX2 gibi yardımcı faktörlerle ortak hareket ettiği diğer bölgelerde ise mithramycin genellikle kompleksleri istikrarsızlaştırdı ve bağlanmayı azalttı. Tüm bu senaryolarda net sonuç, kanser hücrelerinde gen etkinliğinin daha normal bir desenine dönüş olmasıydı; ilaç daha düşük, sabit bir seviyede tutulduğunda alakasız genlerde çok daha az bozulma görüldü.
Laboratuvar mekanizmasından daha iyi tedavi stratejisine
Ekip daha sonra bu mekanistik kavrayışın canlı hayvanlarda önemli olup olmadığını test etti. Ewing sarkomu tümörlü farelerde, aynı toplam mithramycin dozu yedi günlük sürekli infüzyon olarak verildiğinde dramatik tümör küçülmesi sağlarken, aynı miktarın günlük enjeksiyonlar halinde verilmesi çok daha az etkiliydi. Önemli olarak, bu güçlü etki tümörlerde ekstra DNA hasarı bulguları olmadan ortaya çıktı; bu da faydanın genomu yaralamaktan ziyade transkripsiyonun yeniden programlanmasından kaynaklandığını ileri sürüyor. Daha az toksik yeni bir mithramycin analoğu olan AIT-102, nispeten ılımlı dozlarda sürekli infüzyonla verildiğinde daha çarpıcı ve kalıcı tümör gerilemeleri üretti.
Gelecekteki kanser tedavileri için anlamı
Genel olarak çalışma, mithramycin’i kaba bir transkripsiyon zehirleyicisi yerine prototip bir “transkripsiyon faktörü modülatörü” olarak ortaya koyuyor. EWS::FLI1 ve ilişkili ETS faktörleri tarafından kullanılan DNA dizilerine seçici bağlanarak, aksi takdirde ilaçlanması zor olan bir füzyon kaynaklı gen ağını dağıtabiliyor. Kritik olarak bu özgüllük yalnızca dar bir doz ve uygulama penceresinde ortaya çıkıyor; sürekli düşük düzey maruziyet onkojenik programı engellerken hücrenin genel transkripsiyon makinasını geniş çapta durdurmuyor. Bu bulgular, transkripsiyon ve kromatin hedefleyen ilaçlar için ilacı verme biçimimizin molekülden en az onun kendisi kadar önemli olabileceğini savunuyor ve Ewing sarkomu ile ETS faktörlerine bağımlı diğer kanserler için mithramycin analoglarının klinik geliştirilmesinin yenilenmesini destekliyor.
Atıf: Kaufman, R., Flores, G., Boguslawski, E.A. et al. Mithramycin alters EWS::FLI1 DNA binding and RNA polymerase II processivity to inhibit nascent transcription. Nat Commun 17, 2844 (2026). https://doi.org/10.1038/s41467-026-69488-9
Anahtar kelimeler: Ewing sarkomu, mithramycin, EWS::FLI1, transkripsiyon faktörü hedefleme, ilaç dozlama programı