Clear Sky Science · sv
Mithramycin ändrar EWS::FLI1:s DNA‑bindning och RNA‑polymeras II‑processivitet för att hämma nybildad transkription
Varför detta spelar roll för cancerbehandling
Ewing‑sarkom är en aggressiv bentumör som främst drabbar barn och unga vuxna. Den drivs av ett potent fusionsprotein, EWS::FLI1, som omkonfigurerar hur celler läser sitt DNA. Denna studie tar ett nytt grepp på ett gammalt cytostatikum, mithramycin, och visar att—om det ges på rätt sätt—kan det selektivt stänga ner detta cancerdrivande program samtidigt som stora delar av cellens övriga maskineri lämnas i fred. Arbetet visar hur dos och administrationsschema, inte bara läkemedlets identitet, kan avgöra skillnaden mellan bred toxicitet och precis målning.
Ett gammalt läkemedel med en dold förmåga
Mithramycin är en naturprodukt som lägger sig i minor groove i DNA, särskilt vid korta sträckor rika på baserna G och C. I årtionden har det setts som ett kraftigt ”kemoterapeutikum”, antaget att det skadar DNA och blockerar transkription över hela linjen. Men redan på 1960‑talet rapporterade läkare en komplett remission hos en patient med Ewing‑sarkom när mithramycin gavs som en kontinuerlig sju dygn lång infusion. Mer nyligen, när samma läkemedel testades igen men administrerades som korta dagliga doser, sågs bara minimal nytta. Författarna ville med moderna genomiska verktyg förstå om mithramycin kan agera som ett precisionsläkemedel mot EWS::FLI1—och om administrationsschemat förklarar den markanta skillnaden i patientrespons.
Hur fusionsdrivaren slås på och av
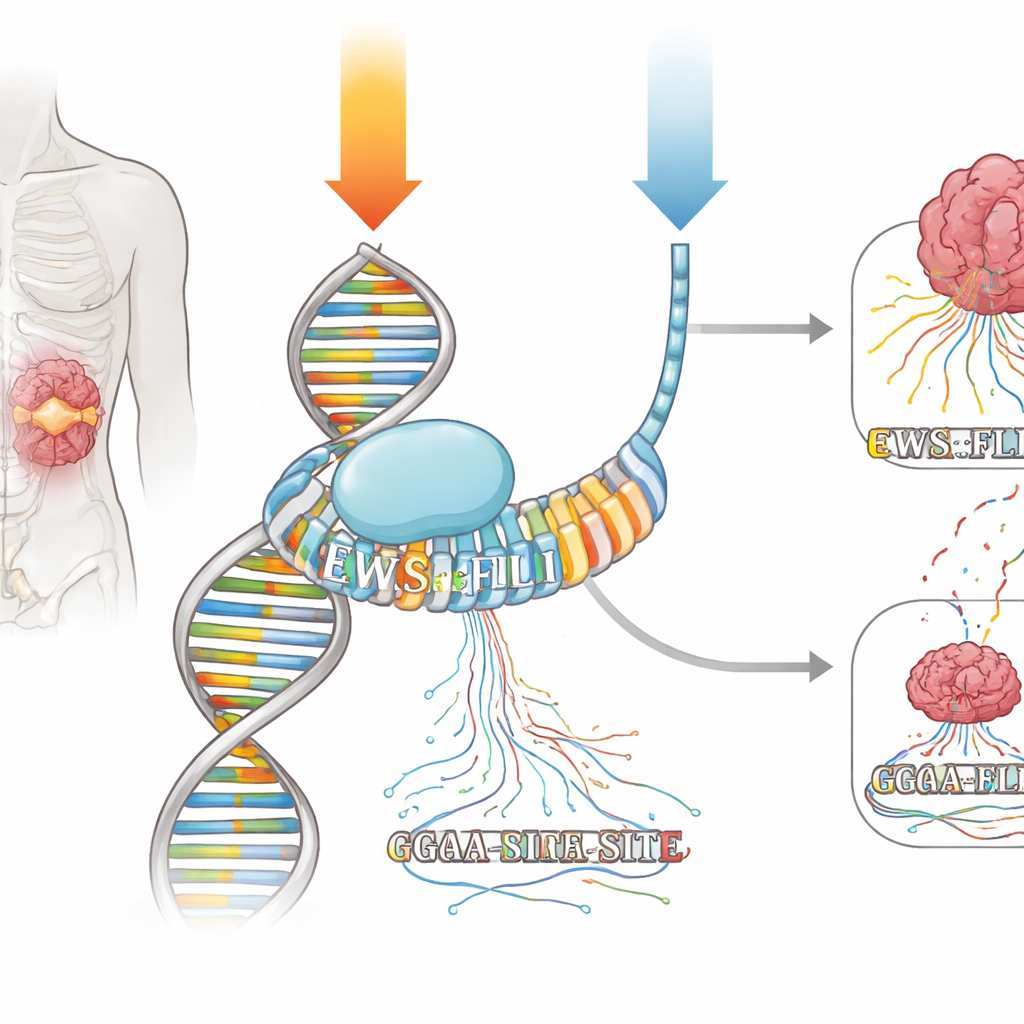
EWS::FLI1 tillhör ETS‑familjen av transkriptionsfaktorer, som fäster vid ett enkelt DNA‑ord byggt kring ”GGAA.” I Ewing‑sarkom binder EWS::FLI1 särskilt starkt till långa upprepade GGAA‑sekvenser, så kallade mikrosatelliter, för att slå upp eller ner hela gen‑nätverk. Teamet exponerade Ewing‑sarkomceller för två mithramycinregimer som gav likartad hämning av viktiga EWS::FLI1‑målgener: en kort, högdospulsering och en lägre dos given under en mycket längre tid. Med metoder som kartlägger både var EWS::FLI1 sitter på DNA och var nya RNA‑molekyler bildas i realtid kunde de följa hur varje regimen förändrade bindning och transkription över genomet.
Finjustering av transkriptionsmaskineriet
Tvärtemot äldre in vitro‑studier agerade mithramycin inte enbart som en universell transkriptionshämmare vid kliniskt relevanta nivåer. Vid noggrant valda låga koncentrationer förändrade kontinuerlig exponering främst hur EWS::FLI1 initierar transkription vid sina målställen. Vissa EWS::FLI1‑toppar på DNA blev svagare, andra starkare, men i båda fallen blev den efterföljande effekten att programmet blev ”förgiftat”: gener som normalt aktiveras av fusionen sänktes, och de som normalt undertrycks släpptes fria. Vid högre koncentrationer började dock mithramycin störa RNA‑polymeras II—enzymet som kopierar DNA till RNA—förmåga att förflytta sig längs långa gener. Denna blockering skapade breda, icke‑specifika effekter som dämpade vissa önskvärda reverseringar av EWS::FLI1:s aktivitet, särskilt för stora gener där polymeraset måste färdas långt från start till slut.
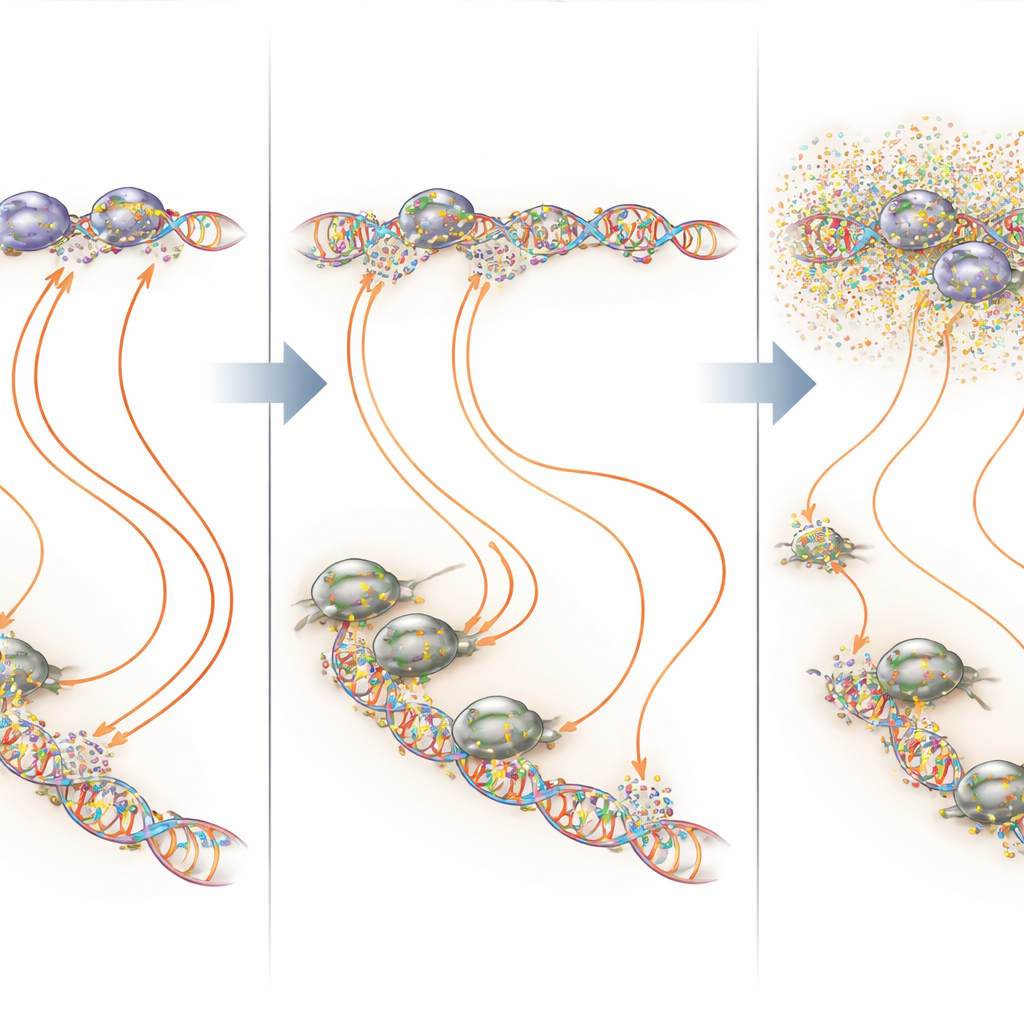
Målning av DNA‑hotspots i stället för hela genomet
Genom att överlagra bindnings‑ och transkriptionskartor visade forskarna att mithramycin verkar starkast vid de mycket GGAA‑rika regioner som EWS::FLI1 är beroende av. Vid dessa mikrosatelliter och vid isolerade GGAA‑ställen ökade lågdos kontinuerlig mithramycin ofta EWS::FLI1‑okupans men stängde ändå ner produktiv transkription—en tydlig illustration av en ”Guldlockens” princip, där både för lite och för mycket bindning av en transkriptionsfaktor kan skada dess funktion. Vid andra platser där EWS::FLI1 samarbetar med kofaktorer såsom AP‑1, E2F eller RUNX2 tenderade mithramycin att destabilisera komplexen och minska bindningen. I alla dessa scenarier var nettot en mer normal genaktivitetsprofil i cancercellerna, med avsevärt mindre störning av orelaterade gener när läkemedlet hölls på en lägre, jämn nivå.
Från laboratoriemekanism till bättre behandlingsstrategi
Teamet testade sedan om denna mekanistiska insikt spelade roll i levande djur. Hos möss med Ewing‑sarkomtumörer orsakade samma totala mängd mithramycin som gavs som en sju dygns kontinuerlig infusion dramatisk tumörkrympning, medan samma mängd levererad som dagliga injektioner var betydligt mindre effektiv. Viktigt är att denna kraftiga effekt uppträdde utan tecken på ökad DNA‑skada i tumörerna, vilket talar för att nyttan kommer från omprogrammering av transkription snarare än från att skada genomet. En nyare, mindre toxisk mithramycin‑analog, AIT‑102, gav ännu mer framträdande och bestående tumörregressioner när den administrerades som kontinuerlig infusion vid relativt måttliga doser.
Vad detta betyder för framtida cancerterapier
Sammantaget visar studien att mithramycin är en prototyp för en ”modulator av transkriptionsfaktorer” snarare än ett grovt transkriptionsgift. Genom att binda selektivt till DNA‑sekvenser som används av EWS::FLI1 och relaterade ETS‑faktorer kan det montera ner ett fusionsdrivet gen nätverk som annars är svårt att angripa med läkemedel. Avgörande är att denna specificitet endast framträder inom ett snävt fönster av dos och schema, där kontinuerlig låg nivå av exponering blockerar det onkogena programmet utan att brett stoppa cellens transkriptionsmaskineri. Dessa fynd talar för att, för läkemedel som riktar sig mot transkription och kromatin, kan hur vi ger läkemedlet vara lika viktigt som själva molekylen, och de stödjer förnyad klinisk utveckling av mithramycin‑analoger för Ewing‑sarkom och andra cancerformer som är beroende av ETS‑transkriptionsfaktorer.
Citering: Kaufman, R., Flores, G., Boguslawski, E.A. et al. Mithramycin alters EWS::FLI1 DNA binding and RNA polymerase II processivity to inhibit nascent transcription. Nat Commun 17, 2844 (2026). https://doi.org/10.1038/s41467-026-69488-9
Nyckelord: Ewing‑sarkom, mithramycin, EWS::FLI1, riktning av transkriptionsfaktorer, läkemedelsdosering schema