Clear Sky Science · it
Mithramycin altera il legame di EWS::FLI1 al DNA e la processività della RNA polimerasi II per inibire la trascrizione nascitante
Perché questo è importante per il trattamento del cancro
Il sarcoma di Ewing è un tumore osseo aggressivo che colpisce principalmente bambini e giovani adulti. È guidato da una potente proteina di fusione, EWS::FLI1, che riorganizza il modo in cui le cellule leggono il loro DNA. Questo studio riesamina un vecchio chemioterapico, la mithramicina, e mostra che—se somministrata nel modo corretto—può spegnere selettivamente questo programma oncogenico risparmiando gran parte degli altri meccanismi cellulari. Il lavoro rivela come dose e calendario, non solo il farmaco in sé, possano fare la differenza tra tossicità diffusa e targeting preciso.
Un vecchio farmaco con un talento nascosto
La mithramicina è un prodotto naturale che si inserisce nella solco minore del DNA, specialmente in brevi tratti ricchi delle lettere G e C. Per decenni è stata etichettata come un bruto strumento “chemioterapico”, ritenuta capace di danneggiare il DNA e bloccare la trascrizione in generale. Tuttavia, medici negli anni Sessanta riportarono una risposta completa in un paziente con sarcoma di Ewing quando la mithramicina fu somministrata come infusione continua di sette giorni. Più di recente, quando lo stesso farmaco è stato riesaminato ma somministrato come dosi giornaliere brevi, si osservò solo un beneficio minimo. Gli autori hanno voluto capire, con strumenti genomici moderni, se la mithramicina può agire come farmaco di precisione contro EWS::FLI1—e se il suo schema di somministrazione spiega la marcata differenza nelle risposte dei pazienti.
Come il driver di fusione viene acceso e spento
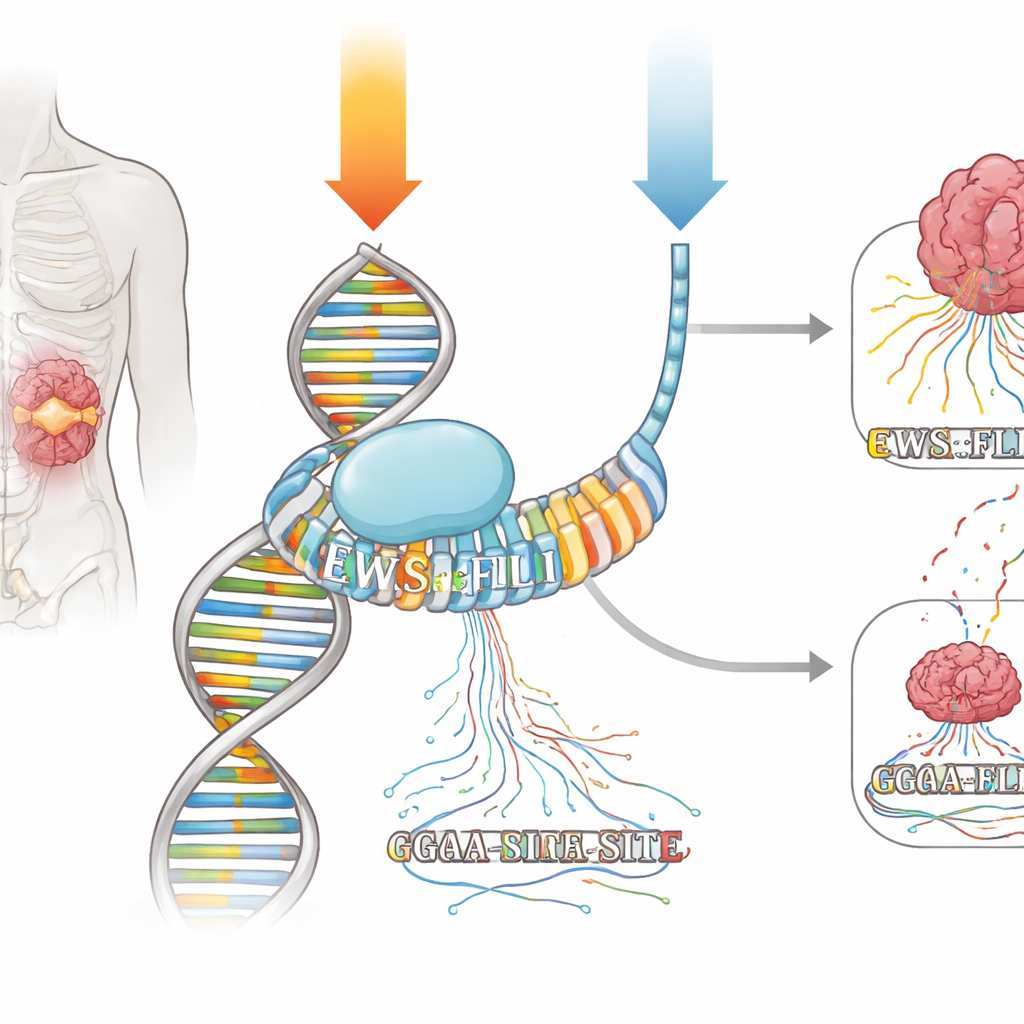
EWS::FLI1 appartiene alla famiglia ETS dei fattori di trascrizione, che si legano a una semplice parola del DNA costruita intorno a “GGAA.” Nel sarcoma di Ewing, EWS::FLI1 si lega particolarmente forte a lunghe sequenze ripetute di siti GGAA, chiamate microsatelliti, per attivare o reprimere intere reti geniche. Il team ha esposto cellule di sarcoma di Ewing a due regimi di mithramicina che produssero una soppressione simile dei principali geni bersaglio di EWS::FLI1: un impulso breve ad alta dose e una dose più bassa somministrata per un tempo molto più lungo. Usando tecniche che mappano sia dove EWS::FLI1 si trova sul DNA sia dove vengono prodotti nuovi RNA in tempo reale, hanno potuto osservare come ciascun regime modificasse il legame e la trascrizione nel genoma.
Affinare la macchina della trascrizione
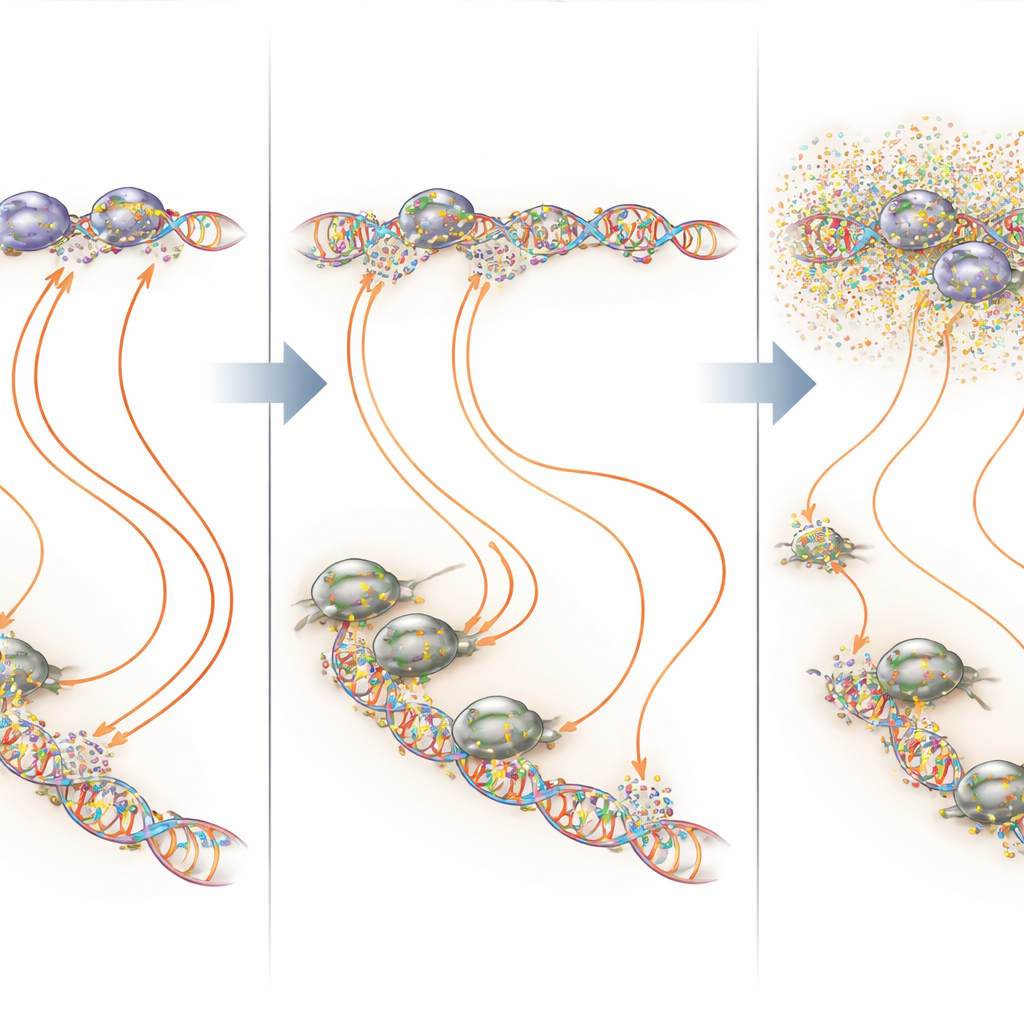
Contrariamente a studi in vitro più datati, la mithramicina non agì semplicemente come un blocco universale della trascrizione a livelli clinicamente rilevanti. A concentrazioni basse scelte con cura, l’esposizione continua alterò principalmente il modo in cui EWS::FLI1 avvia la trascrizione nei suoi siti bersaglio. Alcuni picchi di EWS::FLI1 sul DNA divennero più deboli, altri più forti, ma in entrambi i casi l’effetto a valle fu quello di «avvelenare» il programma: i geni normalmente attivati dalla fusione furono attenuati, e quelli normalmente soppressi furono rilasciati. A concentrazioni più elevate, però, la mithramicina iniziò a interferire con la capacità della RNA polimerasi II—l’enzima che copia il DNA in RNA—di procedere lungo geni lunghi. Quello stallo creò effetti ampi e non specifici, mascherando parte della desiderabile inversione dell’attività di EWS::FLI1, in particolare per i geni grandi che richiedevano che la polimerasi si muovesse a lunga distanza dall’inizio alla fine del gene.
Mirare punti caldi del DNA invece dell’intero genoma
Sovrapponendo mappe di legame e trascrizione, i ricercatori mostrarono che la mithramicina agisce più intensamente proprio sulle regioni ricche di GGAA da cui dipende EWS::FLI1. Su questi microsatelliti e su siti GGAA isolati, la mithramicina continua a basso dosaggio spesso aumentava l’occupazione di EWS::FLI1 ma comunque spegneva la trascrizione produttiva—una chiara illustrazione del principio della «via di mezzo», in cui sia troppo poco sia troppo molto legame di un fattore di trascrizione può danneggiarne la funzione. In altri siti dove EWS::FLI1 collabora con cofattori come AP-1, E2F o RUNX2, la mithramicina tendeva a destabilizzare i complessi e a ridurre il legame. In tutti questi scenari, il risultato netto fu uno schema di attività genica più normale nelle cellule tumorali, con molto meno disturbo di geni non correlati quando il farmaco veniva mantenuto a un livello basso e costante.
Dalla meccanica di laboratorio a una strategia di trattamento migliore
Il gruppo ha poi testato se questa intuizione meccanicistica avesse rilevanza negli animali viventi. Nei topi portatori di tumori di sarcoma di Ewing, la stessa dose totale di mithramicina somministrata come infusione continua di sette giorni causò un marcato restringimento del tumore, mentre la stessa quantità erogata come iniezioni giornaliere fu molto meno efficace. È importante sottolineare che questo effetto potente si verificò senza segni di ulteriore danno al DNA nei tumori, suggerendo che il beneficio deriva dalla riprogrammazione della trascrizione più che da lesioni al genoma. Un analogo più recente e meno tossico della mithramicina, AIT-102, produsse regressioni tumorali ancora più impressionanti e durature quando somministrato tramite infusione continua a dosi relativamente modeste.
Cosa significa per le future terapie oncologiche
Nel complesso, lo studio presenta la mithramicina come un prototipo di «modulatore del fattore di trascrizione» piuttosto che come un semplice veleno della trascrizione. Legandosi selettivamente a sequenze di DNA utilizzate da EWS::FLI1 e da fattori ETS correlati, può smantellare una rete genica guidata da una fusione che altrimenti è molto difficile da colpire farmacologicamente. Fondamentalmente, questa specificità emerge solo entro una finestra ristretta di dose e schema, dove un’esposizione continua a basso livello blocca il programma oncogenico senza arrestare in modo esteso la macchina di trascrizione cellulare. Questi risultati sostengono che, per i farmaci che mirano alla trascrizione e alla cromatina, il modo in cui si somministra il farmaco può essere importante quanto la molecola stessa, e supportano un rinnovato sviluppo clinico di analoghi della mithramicina per il sarcoma di Ewing e altri tumori che fanno affidamento sui fattori di trascrizione ETS.
Citazione: Kaufman, R., Flores, G., Boguslawski, E.A. et al. Mithramycin alters EWS::FLI1 DNA binding and RNA polymerase II processivity to inhibit nascent transcription. Nat Commun 17, 2844 (2026). https://doi.org/10.1038/s41467-026-69488-9
Parole chiave: Sarcoma di Ewing, mithramicina, EWS::FLI1, mirare i fattori di trascrizione, schema di dosaggio del farmaco