Clear Sky Science · pt
Mitramicina altera a ligação do EWS::FLI1 ao DNA e a produtividade da RNA polimerase II para inibir a transcrição nascente
Por que isso importa para o tratamento do câncer
O sarcoma de Ewing é um câncer ósseo agressivo que atinge principalmente crianças e jovens adultos. Ele é impulsionado por uma potente proteína de fusão, EWS::FLI1, que reprograma a leitura do DNA pelas células. Este estudo revisita um antigo quimioterápico, a mitramicina, e mostra que — se administrada da maneira correta — ela pode bloquear seletivamente esse programa oncogênico enquanto preserva grande parte das demais funções celulares. O trabalho revela como a dose e o esquema, e não apenas o fármaco em si, podem ser o fator determinante entre toxicidade ampla e direcionamento preciso.
Um fármaco antigo com um talento oculto
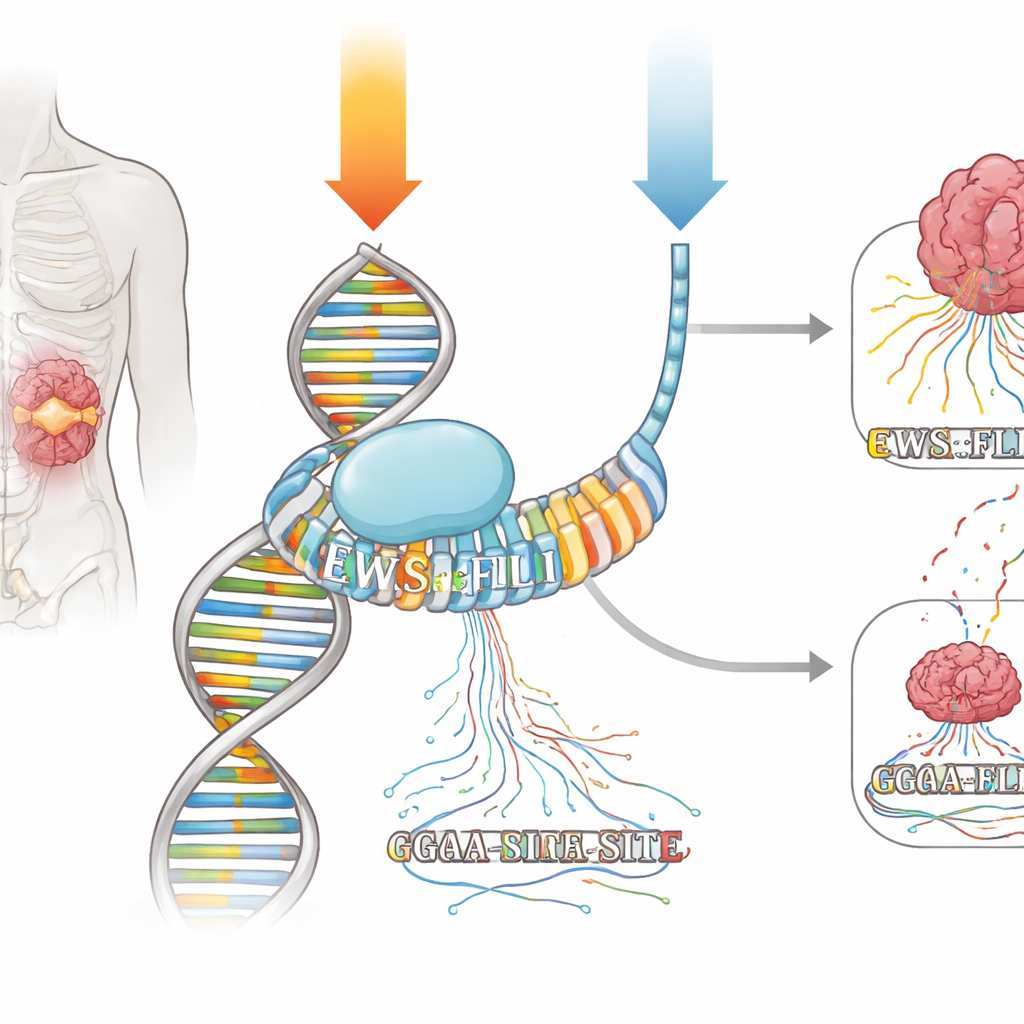
A mitramicina é um produto natural que se encaixa na pequena fenda do DNA, especialmente em trechos curtos ricos nas bases G e C. Durante décadas foi rotulada como uma ferramenta “quimioterápica” bruta, presumida como capaz de danificar o DNA e bloquear a transcrição de forma indiscriminada. Contudo, médicos na década de 1960 relataram uma resposta completa em um paciente com sarcoma de Ewing quando a mitramicina foi administrada como infusão contínua de sete dias. Mais recentemente, quando o mesmo fármaco foi testado novamente, mas dado em doses diárias curtas, observou-se apenas benefício mínimo. Os autores buscaram entender, com ferramentas genômicas modernas, se a mitramicina pode agir como um fármaco de precisão contra o EWS::FLI1 — e se o esquema de administração explica a diferença marcante nas respostas dos pacientes.
Como o motor de fusão é ligado e desligado
O EWS::FLI1 pertence à família ETS de fatores de transcrição, que se ligam a uma palavra simples do DNA centrada em “GGAA”. No sarcoma de Ewing, o EWS::FLI1 se liga com particular afinidade a longas repetições de sítios GGAA, chamadas de microssatélites, para ativar ou reprimir redes inteiras de genes. A equipe expôs células de sarcoma de Ewing a dois esquemas de mitramicina que produziram supressão parecida de genes-alvo chave do EWS::FLI1: um pulso breve de alta dose e uma dose menor administrada por muito mais tempo. Usando técnicas que mapeiam tanto onde o EWS::FLI1 se encontra no DNA quanto onde novas moléculas de RNA estão sendo produzidas em tempo real, eles puderam observar como cada esquema alterou a ligação e a transcrição ao longo do genoma.
Financiando o maquinário de transcrição
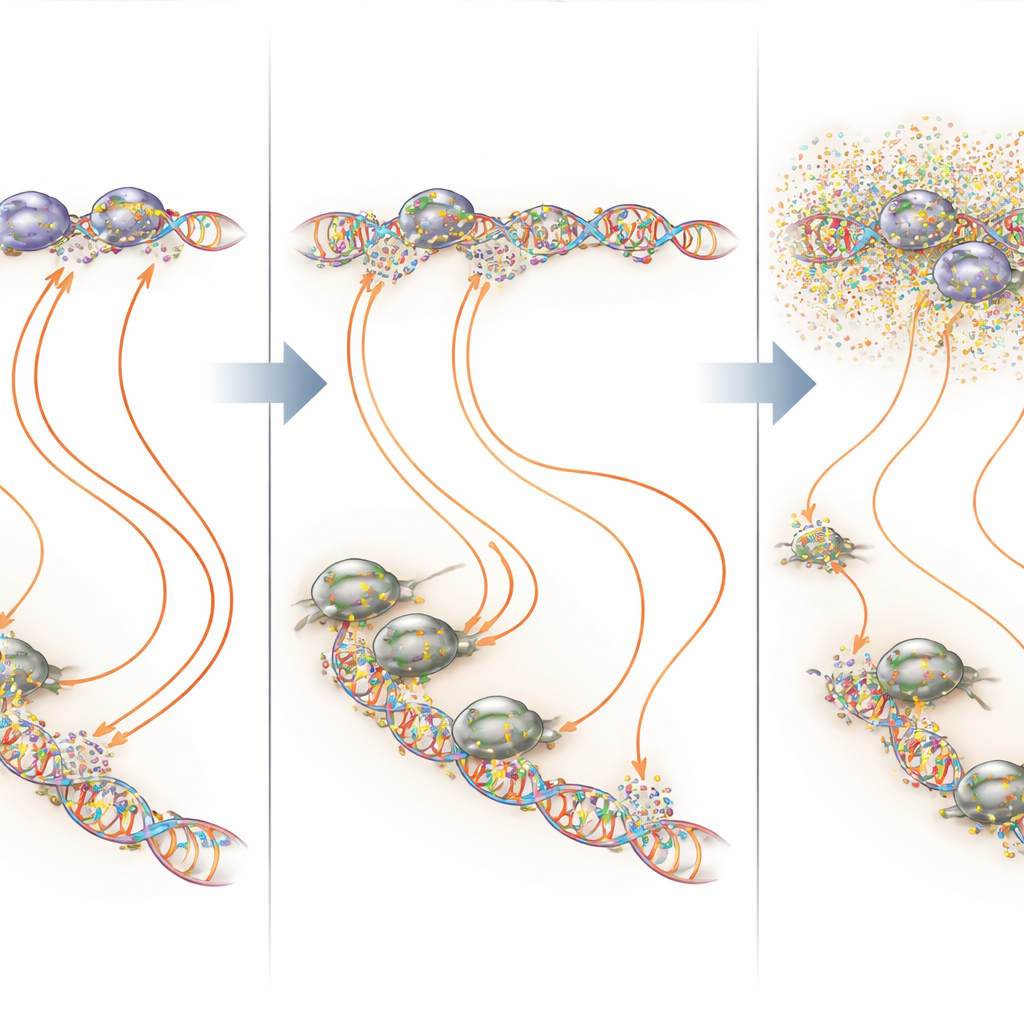
Ao contrário de estudos antigos in vitro, a mitramicina não atuou simplesmente como um bloqueador universal da transcrição em níveis clinicamente relevantes. Em concentrações baixas cuidadosamente escolhidas, a exposição contínua alterou principalmente como o EWS::FLI1 inicia a transcrição em seus sítios-alvo. Alguns picos de EWS::FLI1 no DNA ficaram mais fracos, outros mais fortes, mas em ambos os casos o efeito a montante foi “envenenar” o programa: genes normalmente ativados pela fusão foram reduzidos, e aqueles normalmente reprimidos foram liberados. Em concentrações mais altas, entretanto, a mitramicina começou a interferir na capacidade da RNA polimerase II — a enzima que copia DNA em RNA — de percorrer genes longos. Esse aprisionamento gerou efeitos amplos e não específicos, mascarando parte da reversão desejável da atividade do EWS::FLI1, particularmente em genes grandes que exigem que a polimerase se desloque muito desde o início até o fim do gene.
Alvejando pontos quentes do DNA em vez de todo o genoma
Ao sobrepor mapas de ligação e de transcrição, os pesquisadores mostraram que a mitramicina age com mais força nas regiões muito ricas em GGAA das quais o EWS::FLI1 depende. Nesses microssatélites e em sítios GGAA isolados, a mitramicina contínua em baixa dose frequentemente aumentou a ocupação de EWS::FLI1, mas ainda assim interrompeu a transcrição produtiva — uma ilustração clara do princípio “Cachinhos Dourados”, onde tanto pouca quanto muita ligação de um fator de transcrição pode ser prejudicial à sua função. Em outros sítios onde o EWS::FLI1 faz parceria com cofatores como AP-1, E2F ou RUNX2, a mitramicina tende a desestabilizar os complexos e reduzir a ligação. Em todos esses cenários, o resultado líquido foi um padrão de atividade gênica mais próximo do normal nas células tumorais, com bem menos perturbação de genes não relacionados quando o fármaco foi mantido em um nível mais baixo e constante.
Do mecanismo em laboratório a uma melhor estratégia terapêutica
A equipe então testou se esse insight mecanístico importava em animais vivos. Em camundongos portadores de tumores de sarcoma de Ewing, a mesma dose total de mitramicina administrada como infusão contínua de sete dias provocou um encolhimento tumoral dramático, enquanto a mesma quantidade entregue como injeções diárias foi muito menos eficaz. Importante, esse efeito potente ocorreu sem sinais de dano adicional ao DNA nos tumores, sugerindo que o benefício vem da reprogramação da transcrição em vez de lesar o genoma. Um análogo mais novo e menos tóxico da mitramicina, AIT-102, produziu regressões tumorais ainda mais impressionantes e duradouras quando administrado por infusão contínua em doses relativamente modestas.
O que isso significa para terapias futuras contra o câncer
No conjunto, o estudo revela a mitramicina como um protótipo de “modulador de fator de transcrição” em vez de um veneno bruto da transcrição. Ao se ligar seletivamente a sequências de DNA utilizadas pelo EWS::FLI1 e por fatores ETS relacionados, ela pode desmantelar uma rede gênica movida pela fusão que de outra forma é muito difícil de atingir com fármacos. Crucialmente, essa especificidade emerge apenas dentro de uma janela estreita de dose e esquema, onde a exposição contínua em baixo nível bloqueia o programa oncogênico sem aprisionar amplamente o maquinário de transcrição da célula. Essas descobertas sustentam a ideia de que, para fármacos que miram transcrição e cromatina, como damos o fármaco pode ser tão importante quanto a própria molécula, e apoiam o desenvolvimento clínico renovado de análogos da mitramicina para o sarcoma de Ewing e outros cânceres que dependem de fatores de transcrição ETS.
Citação: Kaufman, R., Flores, G., Boguslawski, E.A. et al. Mithramycin alters EWS::FLI1 DNA binding and RNA polymerase II processivity to inhibit nascent transcription. Nat Commun 17, 2844 (2026). https://doi.org/10.1038/s41467-026-69488-9
Palavras-chave: sarcoma de Ewing, mitramicina, EWS::FLI1, direcionamento de fator de transcrição, esquema de dosagem de fármaco