Clear Sky Science · de
Mithramycin verändert die DNA-Bindung von EWS::FLI1 und die Prozessivität der RNA-Polymerase II, um die neu entstehende Transkription zu hemmen
Warum das für die Krebsbehandlung wichtig ist
Das Ewing-Sarkom ist ein aggressiver Knochentumor, der vor allem Kinder und junge Erwachsene trifft. Angetrieben wird er von einem starken Fusionsprotein, EWS::FLI1, das die Art und Weise, wie Zellen ihre DNA lesen, neu verdrahtet. Diese Studie nimmt ein altes Chemotherapeutikum, Mithramycin, wieder in den Blick und zeigt, dass es—wenn es auf die richtige Weise verabreicht wird—dieses krebsfördernde Programm selektiv ausschalten kann, während große Teile der übrigen zellulären Maschinerie geschont bleiben. Die Arbeit zeigt, dass Dosis und Verabreichungsplan, nicht nur der Wirkstoff selbst, den Unterschied zwischen breiter Toxizität und präziser Zielsteuerung ausmachen können.
Ein altes Medikament mit verborgenem Talent
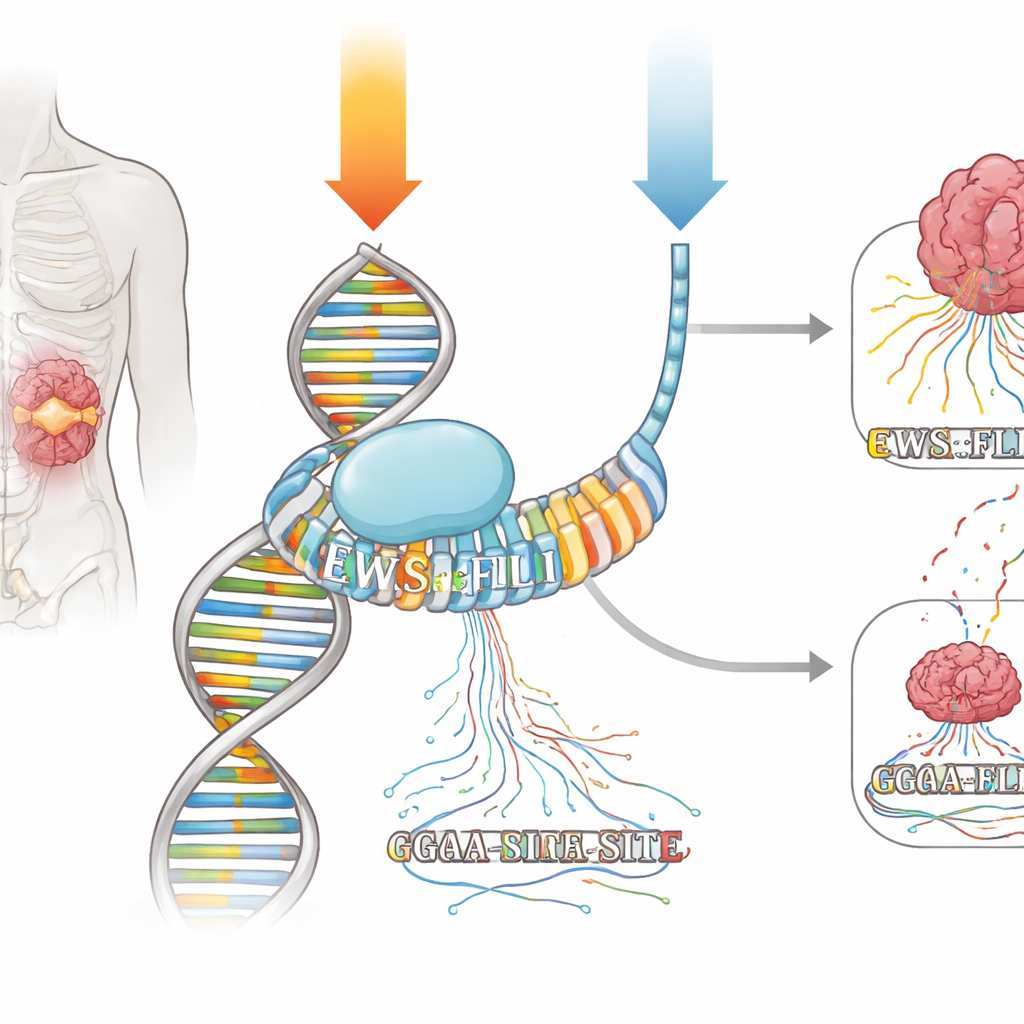
Mithramycin ist ein Naturstoff, der sich in die kleine Furche der DNA einlagert, insbesondere an kurze Abschnitte, die reich an G- und C-Basen sind. Jahrzehntelang galt es als grobes „Chemotherapie“-Werkzeug, dem man eine generelle DNA-Schädigung und eine breit angelegte Transkriptionsblockade zuschrieb. Ärzte in den 1960er-Jahren berichteten jedoch von einem kompletten Ansprechen bei einem Patienten mit Ewing-Sarkom, als Mithramycin als kontinuierliche Sieben-Tage-Infusion verabreicht wurde. Neuere Tests mit täglichen Kurzinfusionen brachten hingegen nur minimale Vorteile. Die Autoren wollten mit modernen genomischen Werkzeugen klären, ob Mithramycin als Präzisionswirkstoff gegen EWS::FLI1 wirken kann — und ob der Verabreichungsplan die auffälligen Unterschiede in den Patientenreaktionen erklärt.
Wie der Fusions-Treiber ein- und ausgeschaltet wird
EWS::FLI1 gehört zur ETS-Familie der Transkriptionsfaktoren, die an ein einfaches DNA-Motiv um „GGAA“ binden. Im Ewing-Sarkom heftet sich EWS::FLI1 besonders stark an lange Abfolgen wiederholter GGAA-Stellen, sogenannte Mikrosatelliten, und schaltet ganze Genetzwerke hoch oder runter. Das Team setzte Ewing-Sarkom-Zellen zwei Mithramycin-Regimen aus, die eine ähnliche Unterdrückung wichtiger EWS::FLI1-Zielgene erzeugten: ein kurzer Hochdosisimpuls und eine deutlich niedrigere Dosis über viel längere Zeit. Mit Techniken, die sowohl die Bindungsorte von EWS::FLI1 auf der DNA als auch die Stellen neu entstehender RNA in Echtzeit kartieren, konnten sie verfolgen, wie jedes Regime Bindung und Transkription im Genom veränderte.
Feinabstimmung der Transkriptionsmaschinerie
Entgegen älteren in vitro-Studien wirkte Mithramycin bei klinisch relevanten Konzentrationen nicht einfach als universeller Transkriptionsblocker. In sorgfältig gewählten niedrigen Konzentrationen veränderte kontinuierliche Exposition vor allem, wie EWS::FLI1 an seinen Zielstellen die Transkription initiiert. Einige EWS::FLI1-Peaks auf der DNA wurden schwächer, andere stärker, aber in beiden Fällen war die nachgelagerte Wirkung, das Programm zu „vergiften“: Gene, die normalerweise durch die Fusion angeschaltet werden, wurden herunterreguliert, und solche, die normalerweise unterdrückt sind, wurden freigesetzt. Bei höheren Konzentrationen begann Mithramycin jedoch die Fähigkeit der RNA-Polymerase II — des Enzyms, das DNA in RNA kopiert — zu beeinträchtigen, längere Gene entlang zu wandern. Dieses Stocken erzeugte breite, unspezifische Effekte und überdeckte einige der wünschenswerten Umkehrungen der EWS::FLI1-Aktivität, insbesondere bei großen Genen, bei denen die Polymerase weite Strecken vom Start bis zum Ende zurücklegen muss.
Gezielte Besetzung von DNA-Hotspots statt des gesamten Genoms
Durch Überlagerung von Bindungs- und Transkriptionskarten zeigten die Forschenden, dass Mithramycin am stärksten an genau die GGAA-reichen Regionen wirkt, von denen EWS::FLI1 abhängt. An diesen Mikrosatelliten und an isolierten GGAA-Stellen erhöhte kontinuierliches Niedrigdosis-Mithramycin häufig die EWS::FLI1-Besetzung, schaltete dennoch die produktive Transkription aus — ein anschauliches Beispiel des „Goldlöckchen“-Prinzips, bei dem sowohl zu wenig als auch zu viel Bindung eines Transkriptionsfaktors seine Funktion beeinträchtigen kann. An anderen Stellen, an denen EWS::FLI1 mit Kofaktoren wie AP-1, E2F oder RUNX2 zusammenarbeitet, neigte Mithramycin dazu, die Komplexe zu destabilisieren und die Bindung zu verringern. In all diesen Szenarien war das Nettoergebnis ein normaleres Genexpressionsmuster in den Krebszellen, mit deutlich weniger Störungen unbeteiligter Gene, wenn das Medikament auf einem niedrigeren, gleichmäßigen Niveau gehalten wurde.
Vom Mechanismus im Labor zur besseren Behandlungsstrategie
Das Team prüfte anschließend, ob diese mechanistische Erkenntnis in lebenden Tieren relevant ist. Bei Mäusen mit Ewing-Sarkom-Tumoren führte dieselbe Gesamtdosis an Mithramycin als sieben Tage andauernde kontinuierliche Infusion zu dramatischem Tumorschwund, während dieselbe Menge als tägliche Injektionen deutlich weniger wirksam war. Wichtig ist, dass dieser starke Effekt ohne Anzeichen zusätzlicher DNA-Schäden in den Tumoren eintrat, was dafür spricht, dass der Nutzen aus der Umprogrammierung der Transkription und nicht aus Genomverletzung resultiert. Ein neueres, weniger toxisches Mithramycin-Analogon, AIT-102, erzeugte bei kontinuierlicher Infusion in moderaten Dosen noch markantere und anhaltendere Tumorregressionen.
Was das für zukünftige Krebstherapien bedeutet
Insgesamt stellt die Studie Mithramycin als Prototyp eines „Modulators von Transkriptionsfaktoren“ dar, nicht als grobes Transkriptionsgift. Indem es selektiv an DNA-Sequenzen bindet, die von EWS::FLI1 und verwandten ETS-Faktoren genutzt werden, kann es ein durch eine Fusion getriebenes Gen-Netzwerk demontieren, das sonst nur schwer medikamentös angreifbar ist. Entscheidend ist, dass diese Spezifität nur innerhalb eines engen Fensters von Dosis und Zeitplan zum Tragen kommt, in dem eine kontinuierlich niedrige Exposition das onkogene Programm blockiert, ohne die Transkriptionsmaschinerie der Zelle breit aufzuhalten. Diese Befunde legen nahe, dass bei Wirkstoffen, die Transkription und Chromatin anvisieren, die Art der Verabreichung genauso wichtig sein kann wie das Molekül selbst, und sie stützen die erneute klinische Entwicklung von Mithramycin-Analoga für Ewing-Sarkom und andere Krebserkrankungen, die auf ETS-Transkriptionsfaktoren beruhen.
Zitation: Kaufman, R., Flores, G., Boguslawski, E.A. et al. Mithramycin alters EWS::FLI1 DNA binding and RNA polymerase II processivity to inhibit nascent transcription. Nat Commun 17, 2844 (2026). https://doi.org/10.1038/s41467-026-69488-9
Schlüsselwörter: Ewing-Sarkom, Mithramycin, EWS::FLI1, Targeting von Transkriptionsfaktoren, Arzneimitteldosierungsplan