Clear Sky Science · ja
ミスラマイシンはEWS::FLI1のDNA結合とRNAポリメラーゼIIのプロセシビティを変化させ、新生転写を抑制する
がん治療においてなぜ重要か
ユーイング肉腫は主に小児や若年成人に発症する進行性の骨肉腫であり、細胞がDNAを読み取る仕組みを書き換える強力な融合タンパク質EWS::FLI1によって駆動されています。本研究は古い抗がん剤ミスラマイシンに改めて注目し、適切な投与法を用いればこのがん駆動プログラムを選択的に遮断し、細胞の他の多くの機能を温存できることを示しています。投与量とスケジュールが、薬そのものだけでなく、広範な毒性と精密な標的化の差を生む可能性があることを明らかにしています。
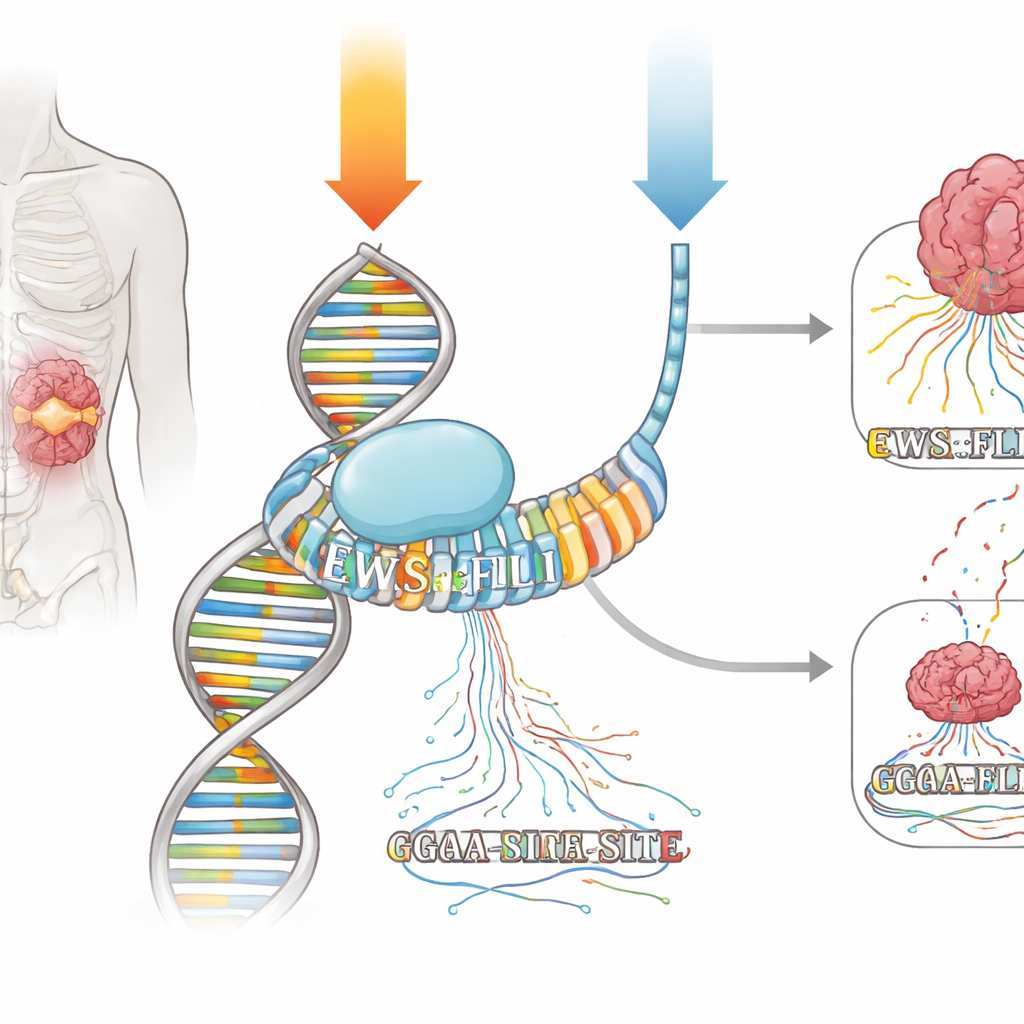
古い薬に潜む新たな特性
ミスラマイシンは天然物で、特にGとCが豊富な短い配列のDNAのマイナーグルーブに入り込む性質を持ちます。数十年にわたり、それは幅広くDNAを損傷させ転写を一律に阻害する「化学療法」と見なされてきました。しかし1960年代の臨床報告では、ミスラマイシンを7日間の持続点滴で投与した患者に完全奏効が得られた例がありました。近年、同じ薬を短時間の毎日投与で再検討したところ、効果はほとんど認められませんでした。著者らは、最新のゲノミクス手法を用いて、ミスラマイシンがEWS::FLI1に対する精密薬になり得るか、そして投与スケジュールが患者反応の顕著な差を説明するかを解明しようとしました。
融合ドライバーがオンとオフになる仕組み
EWS::FLI1はETSファミリーの転写因子に属し、「GGAA」を中心とした単純なDNA配列に結合します。ユーイング肉腫では、EWS::FLI1は特に長く繰り返されたGGAA部位(マイクロサテライト)に強く結合して、遺伝子ネットワーク全体を上げたり下げたりします。研究チームは、主要なEWS::FLI1標的遺伝子の抑制を同程度に引き起こす二つのミスラマイシン投与法――短時間の高用量パルスと、より低用量を長時間持続させる方法――を細胞に適用しました。EWS::FLI1がDNAのどこにいるかと、新しく作られているRNAがリアルタイムでどこで合成されているかを同時にマップする技術を使い、各投与法がゲノム全体で結合と転写をどう変えるかを観察しました。
転写機構の精密調整
以前のin vitro研究とは異なり、臨床で関連する濃度ではミスラマイシンは単純に普遍的な転写阻害剤として作用するわけではありませんでした。慎重に選ばれた低濃度での持続曝露は、主にEWS::FLI1が標的部位で転写を開始する仕組みを変化させました。DNA上のいくつかのEWS::FLI1ピークは弱くなり、他は強くなりましたが、いずれの場合も下流での効果は「プログラムの毒化」であり、融合タンパク質によって通常オンにされる遺伝子は抑えられ、通常抑えられている遺伝子は解放されました。しかし高濃度では、ミスラマイシンはDNAからRNAを合成する酵素であるRNAポリメラーゼIIが長い遺伝子を進行する能力を妨げ始めました。その停滞は広範で非特異的な影響を生み、特に開始点から終点までポリメラーゼの移動を要する大型遺伝子に対しては、EWS::FLI1活性の望ましい逆転効果を覆い隠してしまいました。
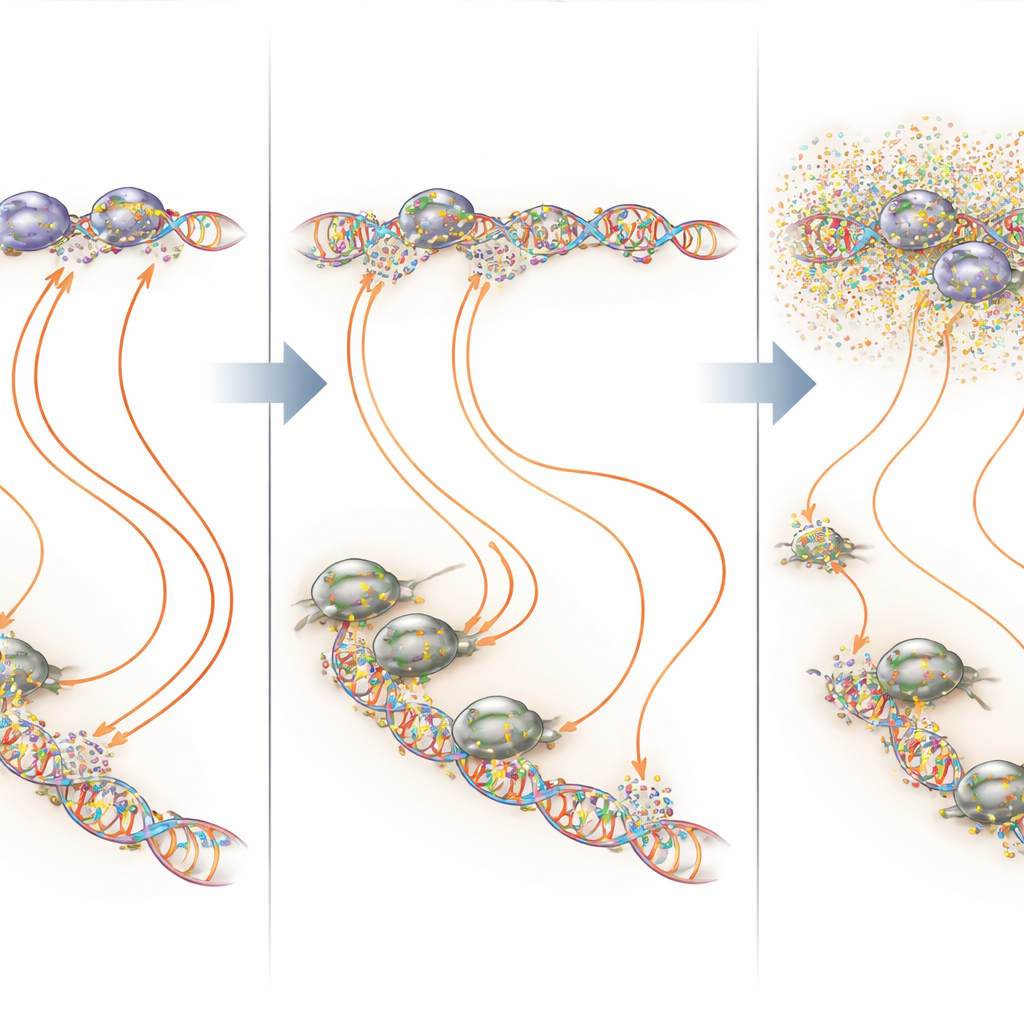
ゲノム全体ではなくDNAのホットスポットを狙う
結合マップと転写マップを重ね合わせることで、ミスラマイシンはEWS::FLI1が依存する非常にGGAAに富む領域で最も強く作用することが示されました。これらのマイクロサテライトや孤立したGGAA部位では、低用量の持続的ミスラマイシン投与がしばしばEWS::FLI1の占有率を増加させながらも生産的な転写を停止させることがあり、「ゴルディロックス」の原則の明確な例を示しています。つまり転写因子の結合が少なすぎても多すぎても機能に有害になり得るということです。AP-1、E2F、RUNX2などの補因子とEWS::FLI1が共存する他の部位では、ミスラマイシンは複合体を不安定化して結合を減少させる傾向がありました。こうしたすべてのシナリオで、総じて薬を低い安定したレベルに保つと、がん細胞の遺伝子活動はより正常なパターンに近づき、無関係な遺伝子の攪乱は大幅に少なくなりました。
実験室の機構からより良い治療戦略へ
次に研究チームは、この機序的知見が生体内で重要かどうかを検証しました。ユーイング肉腫腫瘍を移植したマウスでは、同じ総投与量のミスラマイシンを7日間の持続点滴で与えると劇的な腫瘍縮小が得られたのに対し、同量を毎日注射で投与しても効果ははるかに劣りました。重要なのは、この強力な効果は腫瘍内で過度のDNA損傷の兆候を伴わなかったことであり、利益がゲノムの損傷ではなく転写の再プログラミングから来ていることを示しています。より低毒性の新しいミスラマイシン類縁体であるAIT-102は、比較的穏やかな用量で持続点滴投与した場合に、より顕著で持続的な腫瘍退縮を示しました。
将来のがん治療にとっての意味
全体として本研究は、ミスラマイシンを粗雑な転写毒ではなく「転写因子モジュレーター」の試作モデルとして位置付けます。EWS::FLI1や関連するETS因子が利用するDNA配列に選択的に結合することで、従来は薬剤化が困難だった融合駆動の遺伝子ネットワークを解体し得ます。重要なのは、この特異性は用量と投与スケジュールの狭い窓の中でのみ現れることであり、持続的な低レベル曝露が腫瘍性プログラムを遮断しつつ細胞の転写機構を広く停滞させない点です。転写やクロマチンを標的とする薬剤においては、薬の投与方法が分子自体と同じくらい重要になり得ることを示し、ユーイング肉腫やETS転写因子に依存する他のがんに対するミスラマイシン類縁体の臨床開発の再検討を支持します。
引用: Kaufman, R., Flores, G., Boguslawski, E.A. et al. Mithramycin alters EWS::FLI1 DNA binding and RNA polymerase II processivity to inhibit nascent transcription. Nat Commun 17, 2844 (2026). https://doi.org/10.1038/s41467-026-69488-9
キーワード: ユーイング肉腫, ミスラマイシン, EWS::FLI1, 転写因子標的化, 薬剤投与スケジュール