Clear Sky Science · fr
La mithramycine modifie la liaison d’EWS::FLI1 à l’ADN et la processivité de l’ARN polymérase II pour inhiber la transcription naissante
Pourquoi cela importe pour le traitement du cancer
Le sarcome d’Ewing est un cancer osseux agressif qui touche principalement les enfants et les jeunes adultes. Il est entraîné par une puissante protéine de fusion, EWS::FLI1, qui reprogramme la lecture du génome par la cellule. Cette étude revisite un ancien médicament chimiothérapeutique, la mithramycine, et montre que — si elle est administrée de la bonne manière — elle peut éteindre sélectivement ce programme oncogénique tout en épargnant une grande partie des autres fonctions cellulaires. Le travail met en lumière que la dose et le calendrier, et pas seulement la molécule elle‑même, peuvent faire la différence entre une toxicité généralisée et un ciblage précis.
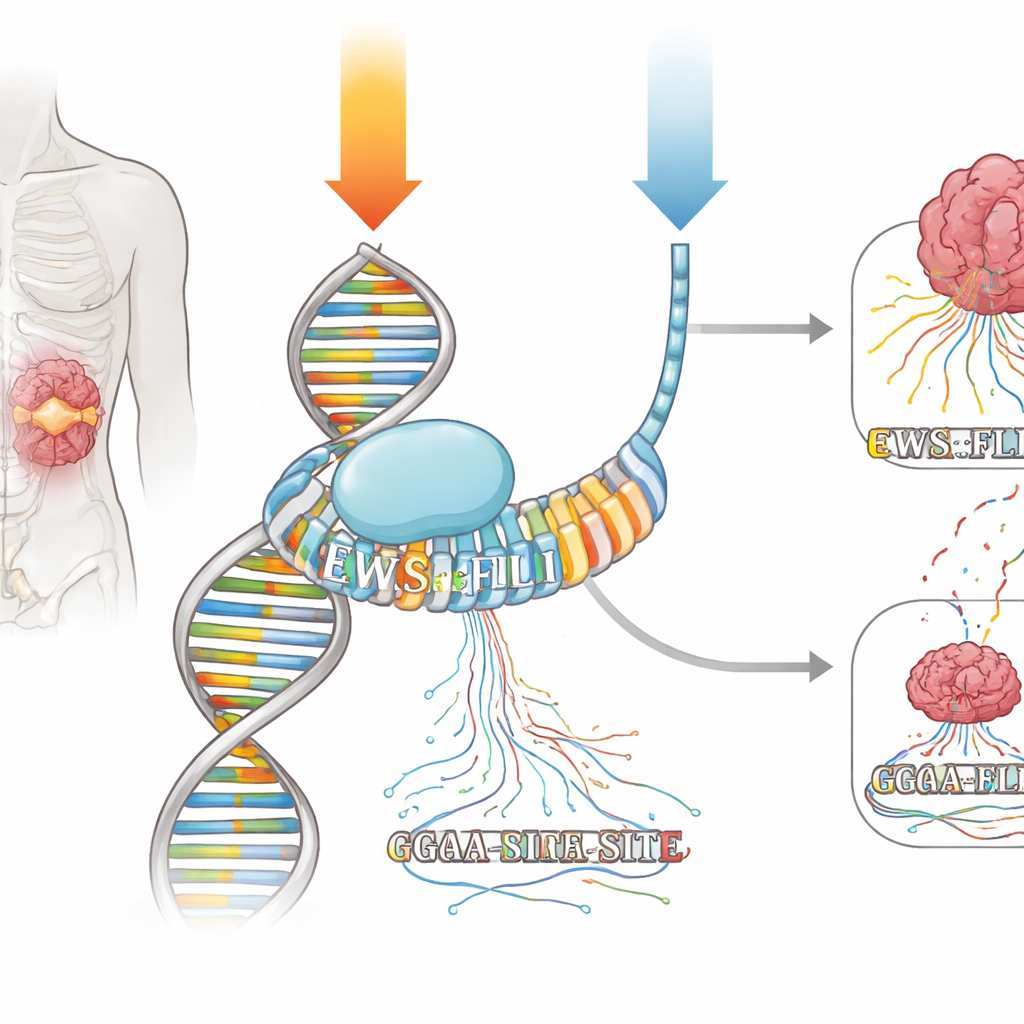
Un vieux médicament au talent caché
La mithramycine est un produit naturel qui se loge dans le sillon mineur de l’ADN, particulièrement sur de courtes séquences riches en G et C. Pendant des décennies, elle a été considérée comme un outil chimiothérapeutique grossier, censé endommager l’ADN et bloquer la transcription de façon généralisée. Pourtant, des cliniciens des années 1960 ont rapporté une rémission complète chez un patient atteint d’un sarcome d’Ewing lorsque la mithramycine a été administrée en perfusion continue de sept jours. Plus récemment, lorsque le même médicament a été réessayé sous forme de courtes doses quotidiennes, seul un bénéfice minime a été observé. Les auteurs ont cherché à comprendre, avec des outils génomiques modernes, si la mithramycine peut agir comme un médicament de précision contre EWS::FLI1 — et si son calendrier d’administration explique la différence frappante entre les réponses des patients.
Comment l’oncogène de fusion s’active et se désactive
EWS::FLI1 appartient à la famille ETS des facteurs de transcription, qui se fixent à un mot d’ADN simple centré sur « GGAA ». Dans le sarcome d’Ewing, EWS::FLI1 se lie particulièrement fort à de longues séries répétées de sites GGAA, appelées microsatellites, pour activer ou réprimer des réseaux entiers de gènes. L’équipe a exposé des cellules de sarcome d’Ewing à deux schémas de mithramycine produisant une suppression similaire des gènes cibles clés d’EWS::FLI1 : une impulsion brève à forte dose et une exposition plus faible mais beaucoup plus longue. En utilisant des techniques cartographiant à la fois où EWS::FLI1 se trouve sur l’ADN et où de nouveaux ARN sont synthétisés en temps réel, ils ont pu observer comment chaque protocole modifiait la liaison et la transcription à l’échelle du génome.
Ajuster la machinerie de la transcription
Contrairement aux anciennes études in vitro, la mithramycine n’agissait pas simplement comme un bloqueur universel de la transcription aux niveaux cliniquement pertinents. À des concentrations basses et soigneusement choisies, l’exposition continue modifiait principalement la façon dont EWS::FLI1 initie la transcription à ses sites cibles. Certains pics de liaison d’EWS::FLI1 sur l’ADN devenaient plus faibles, d’autres plus forts, mais dans les deux cas l’effet en aval était de « empoisonner » le programme : les gènes normalement activés par la fusion étaient réprimés, et ceux normalement inhibés étaient relâchés. À des concentrations plus élevées, cependant, la mithramycine commençait à gêner la capacité de l’ARN polymérase II — l’enzyme qui copie l’ADN en ARN — à parcourir les gènes longs. Cet arrêt provoquait des effets larges et non spécifiques, masquant une partie de l’inversion souhaitable de l’activité d’EWS::FLI1, en particulier pour les grands gènes nécessitant que la polymérase se déplace sur de longues distances entre le début et la fin du gène.
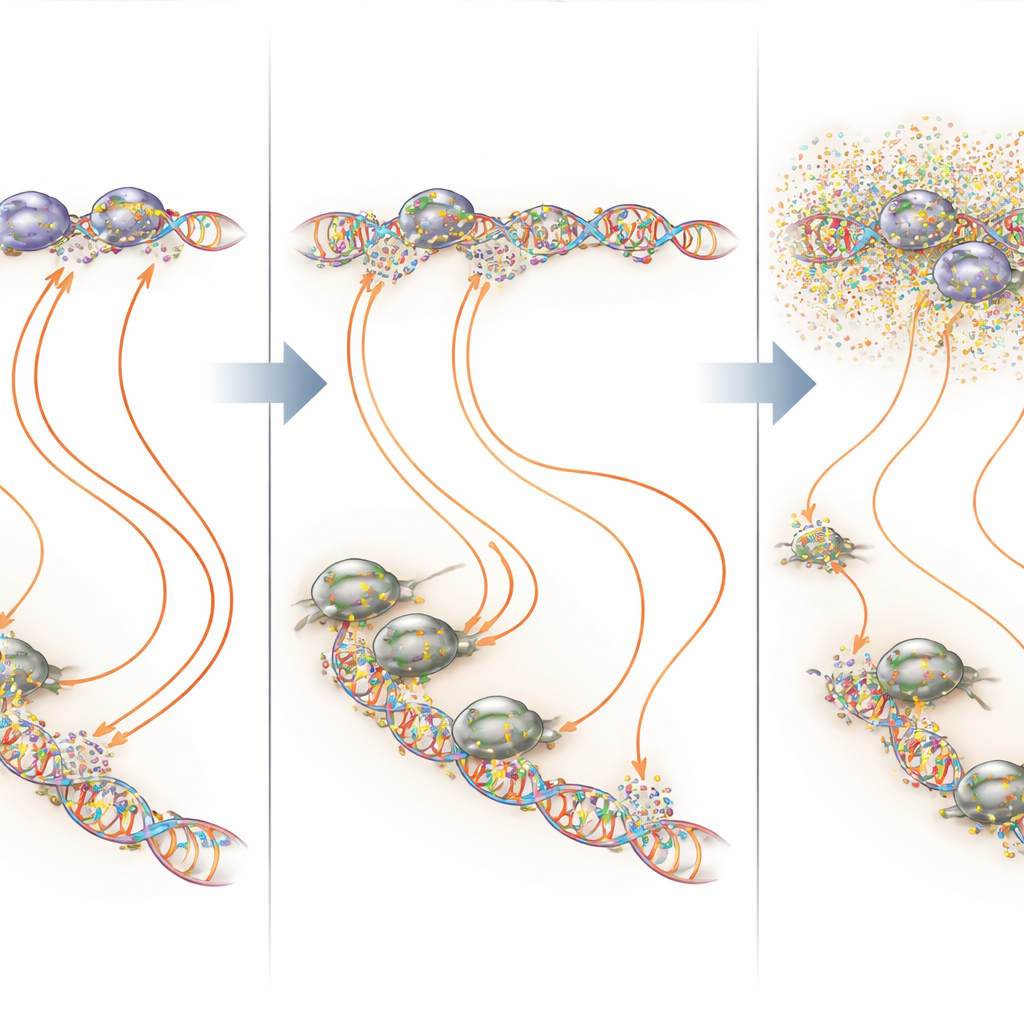
Cibler des points chauds de l’ADN plutôt que tout le génome
En superposant les cartes de liaison et de transcription, les chercheurs ont montré que la mithramycine agit le plus fortement sur les régions très riches en GGAA dont dépend EWS::FLI1. Dans ces microsatellites et sur des sites GGAA isolés, la mithramycine en perfusion continue à faible dose augmentait souvent l’occupation d’EWS::FLI1 tout en bloquant la transcription productive — une illustration claire d’un principe de « juste milieu », où à la fois un lien trop faible et un lien trop fort d’un facteur de transcription peuvent nuire à sa fonction. Sur d’autres sites où EWS::FLI1 s’associe à des cofactors tels qu’AP‑1, E2F ou RUNX2, la mithramycine avait tendance à déstabiliser les complexes et à réduire la liaison. Dans tous ces scénarios, le résultat net était un schéma d’activité génique plus normal dans les cellules tumorales, avec beaucoup moins de perturbation de gènes non liés lorsque le médicament était maintenu à un niveau bas et stable.
Du mécanisme en laboratoire à une meilleure stratégie thérapeutique
L’équipe a ensuite testé si cette compréhension mécanistique importait chez l’animal. Chez des souris porteuses de tumeurs de sarcome d’Ewing, la même dose totale de mithramycine administrée en perfusion continue de sept jours a provoqué une réduction tumorale spectaculaire, alors que la même quantité délivrée par injections quotidiennes était bien moins efficace. Fait important, cet effet puissant s’est produit sans signes de dommages ADN supplémentaires dans les tumeurs, ce qui suggère que le bénéfice provient d’un reformatage de la transcription plutôt que d’une atteinte du génome. Un analogue plus récent et moins toxique de la mithramycine, AIT‑102, a produit des régressions tumorales encore plus marquées et durables lorsqu’il a été administré par perfusion continue à des doses relativement modestes.
Ce que cela signifie pour les thérapies anticancéreuses futures
Dans l’ensemble, l’étude présente la mithramycine comme un prototype de « modulateur de facteurs de transcription » plutôt que comme un poison grossier de la transcription. En se liant de façon sélective aux séquences d’ADN utilisées par EWS::FLI1 et des facteurs ETS apparentés, elle peut démanteler un réseau génique dirigé par une fusion qui est par ailleurs très difficile à cibler pharmacologiquement. De façon cruciale, cette spécificité n’émerge que dans une fenêtre étroite de dose et de calendrier, où une exposition continue de faible amplitude bloque le programme oncogénique sans bloquer largement la machinerie transcriptionnelle de la cellule. Ces résultats plaident pour l’idée que, pour les médicaments ciblant la transcription et la chromatine, la manière d’administrer le traitement peut être aussi importante que la molécule elle‑même, et soutiennent le développement clinique renouvelé d’analogues de la mithramycine pour le sarcome d’Ewing et d’autres cancers dépendant des facteurs de transcription ETS.
Citation: Kaufman, R., Flores, G., Boguslawski, E.A. et al. Mithramycin alters EWS::FLI1 DNA binding and RNA polymerase II processivity to inhibit nascent transcription. Nat Commun 17, 2844 (2026). https://doi.org/10.1038/s41467-026-69488-9
Mots-clés: sarcome d’Ewing, mithramycine, EWS::FLI1, ciblage des facteurs de transcription, calendrier d’administration des médicaments