Clear Sky Science · nl
Mithramycine verandert EWS::FLI1-DNA-binding en RNA-polymerase II-processiviteit om nascenttranscriptie te remmen
Waarom dit belangrijk is voor kankerbehandeling
Ewing-sarcoom is een agressieve botkanker die vooral kinderen en jongvolwassenen treft. De ziekte wordt aangedreven door een krachtige fusieproteïne, EWS::FLI1, die herprogrammeert hoe cellen hun DNA aflezen. Deze studie bekijkt een oud chemotherapiemiddel, mithramycine, en laat zien dat—als het op de juiste wijze wordt toegediend—het selectief dit kankerveroorzakende programma kan uitschakelen terwijl het grootste deel van de overige cellulaire machines gespaard blijft. Het werk toont aan dat dosis en schema, niet alleen het middel zelf, het verschil kunnen maken tussen brede toxiciteit en nauwkeurige targeting.
Een oud medicijn met een verborgen talent
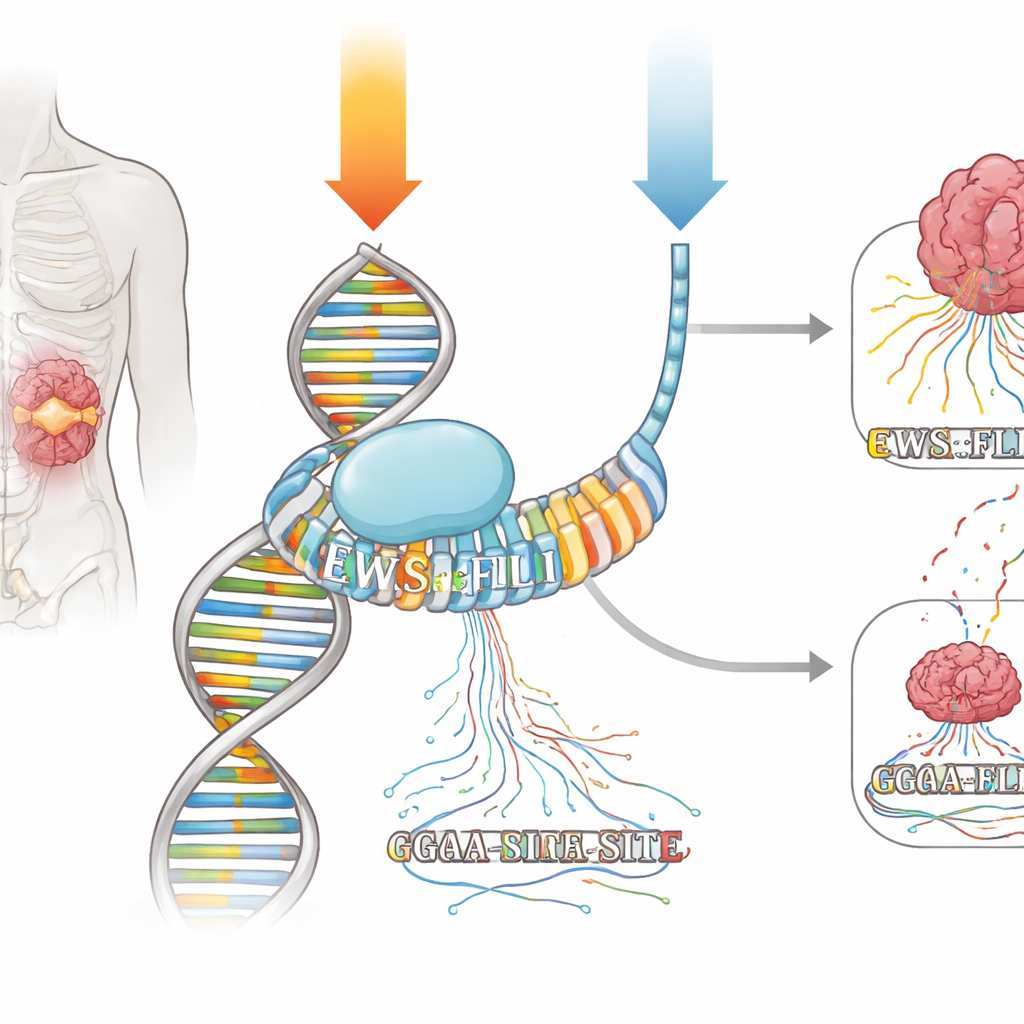
Mithramycine is een natuurlijk product dat zich nestelt in de minor groove van DNA, met name in korte reeksen rijk aan de letters G en C. Decennialang werd het gezien als een bot “chemotherapie”-middel, verondersteld DNA te beschadigen en transcriptie overal te blokkeren. Artsen meldden echter al in de jaren 1960 een volledige respons bij een patiënt met Ewing-sarcoom toen mithramycine als een continue infusie van zeven dagen werd gegeven. Recente herbeoordelingen waarbij hetzelfde middel als korte dagelijkse doses werd toegediend, lieten slechts minimale voordelen zien. De auteurs wilden met moderne genomische hulpmiddelen nagaan of mithramycine als een precisiegeneesmiddel tegen EWS::FLI1 kan werken—en of het toedieningsschema de opvallende verschillen in patiëntresponsen verklaart.
Hoe de fusiedriver aan- en uitgezet wordt
EWS::FLI1 behoort tot de ETS-familie van transcriptiefactoren, die zich hechten aan een eenvoudige DNA-sequentie opgebouwd rond “GGAA.” In Ewing-sarcoom bindt EWS::FLI1 bijzonder sterk aan lange reeksen van herhaalde GGAA-sites, zogenaamde microsatellieten, om hele netwerken van genen aan of uit te zetten. Het team stelde Ewing-sarcoomcellen bloot aan twee mithramycine-regimes die vergelijkbare onderdrukking van belangrijke EWS::FLI1-doelgenen opleverden: een korte, hoge dosispuls en een lagere dosis gegeven gedurende veel langere tijd. Met technieken die zowel in kaart brengen waar EWS::FLI1 op DNA zit als waar nieuwe RNA-moleculen realtime worden gemaakt, konden ze volgen hoe elk regime binding en transcriptie in het hele genoom veranderde.
Het fijnregelen van het transcriptieapparaat
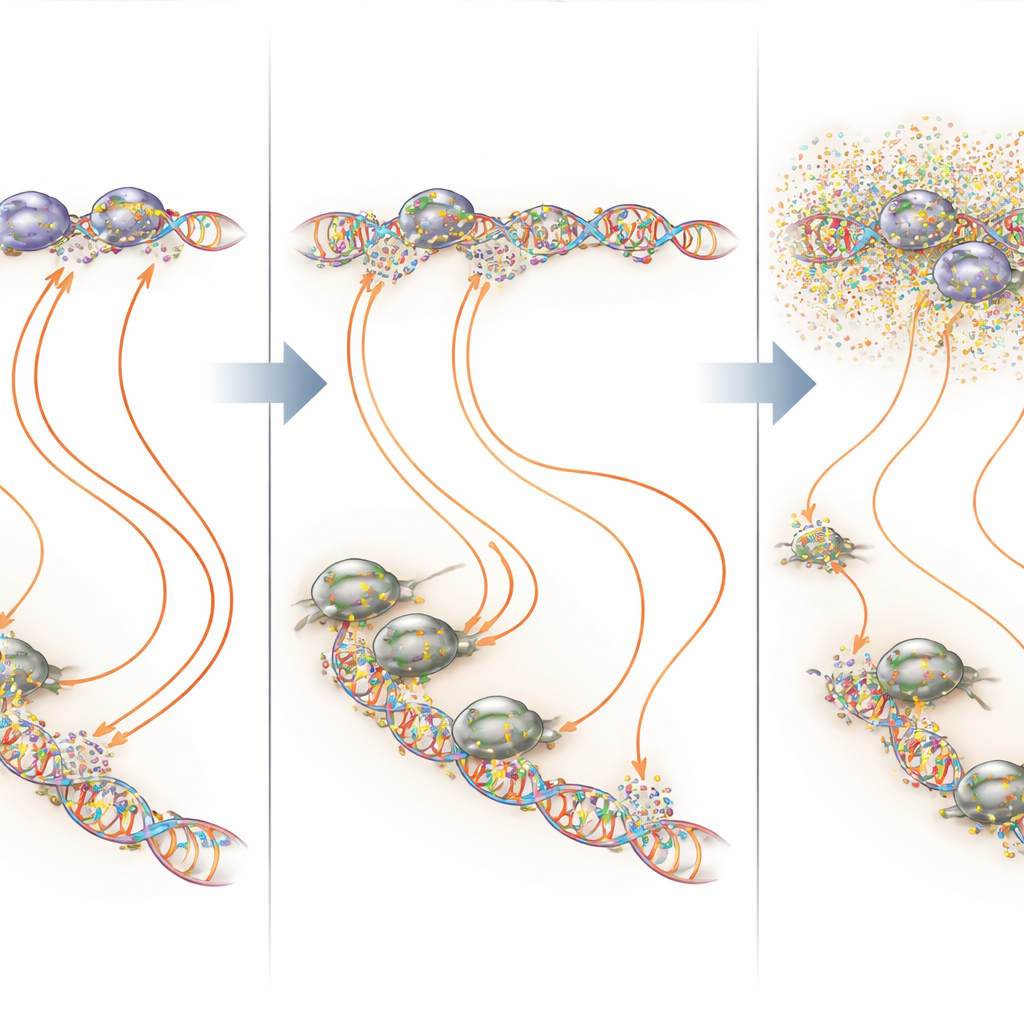
In strijd met oudere in vitro-studies handelde mithramycine bij klinisch relevante niveaus niet simpelweg als een universele transcriptieblokker. Bij zorgvuldig gekozen lage concentraties veranderde continue blootstelling voornamelijk hoe EWS::FLI1 transcriptie op zijn doelplaatsen initieert. Sommige EWS::FLI1-pieken op het DNA werden zwakker, andere sterker, maar in beide gevallen was het downstream-effect het “vergiftigen” van het programma: genen die normaal door de fusie werden aangeschakeld, werden afgezet, en genen die normaal werden onderdrukt, werden vrijgegeven. Bij hogere concentraties echter begon mithramycine het vermogen van RNA-polymerase II—het enzym dat DNA naar RNA kopieert—te verstoren om langs lange genen te reizen. Die vertraging veroorzaakte brede, niet-specifieke effecten en maskeerde enkele van de wenselijke keren van EWS::FLI1-activiteit, vooral bij grote genen waarvoor polymerase ver van het begin naar het einde van het gen moest bewegen.
DNA-hotspots targeten in plaats van het hele genoom
Door binding- en transcriptiekaarten over elkaar te leggen, toonden de onderzoekers aan dat mithramycine het sterkst werkt op de zeer GGAA-rijke regio’s waarop EWS::FLI1 afhankelijk is. Op deze microsatellieten en op geïsoleerde GGAA-sites verhoogde lage-dosis continue mithramycine vaak de EWS::FLI1-bezetting maar schakelde toch productieve transcriptie uit—een duidelijke illustratie van een “Goudlokjes”-principe, waarbij zowel te weinig als te veel binding van een transcriptiefactor schadelijk kan zijn voor zijn functie. Op andere locaties waar EWS::FLI1 samenwerkt met cofactoren zoals AP-1, E2F of RUNX2, had mithramycine de neiging de complexen te destabiliseren en de binding te verminderen. In al deze scenario’s was het nettoresultaat een normaler patroon van genactiviteit in de kankercellen, met veel minder verstoring van niet-gerelateerde genen wanneer het middel op een lagere, constante concentratie werd gehouden.
Van laboratoriummethode naar betere behandelingsstrategie
Het team testte vervolgens of dit mechanistische inzicht in levende dieren van belang was. Bij muizen met Ewing-sarcoomtumoren veroorzaakte dezelfde totale dosis mithramycine gegeven als een continue infusie van zeven dagen dramatische tumorkrimp, terwijl dezelfde hoeveelheid toegediend als dagelijkse injecties veel minder effectief was. Belangrijk was dat dit krachtige effect optrad zonder aanwijzingen voor extra DNA-schade in de tumoren, wat erop wijst dat het voordeel voortkomt uit het herprogrammeren van transcriptie in plaats van het beschadigen van het genoom. Een nieuwere, minder toxische mithramycine-analoog, AIT-102, gaf nog opvallender en duurzamer tumorreducties wanneer het via continue infusie bij relatief bescheiden doses werd gegeven.
Wat dit betekent voor toekomstige kankertherapieën
Samengevat onthult de studie mithramycine als een prototype van een “modulator van transcriptiefactoren” in plaats van een ruw transcriptiegif. Door selectief te binden aan DNA-sequenties die door EWS::FLI1 en verwante ETS-factoren worden gebruikt, kan het een fusiegedreven genennetwerk ontmantelen dat anders moeilijk te behandelen is. Cruciaal is dat deze specificiteit zich alleen openbaart binnen een nauwe marge van dosis en schema, waarbij continue lage blootstelling het oncogene programma blokkeert zonder het transcriptieapparaat van de cel op brede schaal te laten vastlopen. Deze bevindingen maken duidelijk dat voor middelen die transcriptie en chromatine targeten, de toedieningswijze net zo belangrijk kan zijn als het molecuul zelf, en ze ondersteunen hernieuwde klinische ontwikkeling van mithramycine-analogen voor Ewing-sarcoom en andere kankers die afhankelijk zijn van ETS-transcriptiefactoren.
Bronvermelding: Kaufman, R., Flores, G., Boguslawski, E.A. et al. Mithramycin alters EWS::FLI1 DNA binding and RNA polymerase II processivity to inhibit nascent transcription. Nat Commun 17, 2844 (2026). https://doi.org/10.1038/s41467-026-69488-9
Trefwoorden: Ewing-sarcoom, mithramycine, EWS::FLI1, gericht op transcriptiefactoren, dosering en toedieningsschema