Clear Sky Science · he
מיטרמיצין משנה קשירת DNA של EWS::FLI1 ותהליךיות של RNA פולימראז II כדי לעכב שעתוק נאסנטי
מדוע זה חשוב לטיפול בסרטן
סרקומת יווינג היא סרטן עצם אגרסיבי שפוגע בעיקר בילדים ובני נוער. הוא מונע על ידי חלבון פיוז'ן רב־עוצמה, EWS::FLI1, שמחדש את אופן קריאת ה‑DNA בתא. המחקר הזה בוחן מחדש תרופת כימותרפיה ישנה, מיטרמיצין, ומראה כי—אם ניתנת בצורה נכונה—היא יכולה להשבית במבחר את התוכנית המונעת על ידי הסרטן תוך שמירה על רוב שאר מנגנוני התא. העבודה מדגימה שדחיפות המינון ולוח הזמנים, לא רק התרופה עצמה, עשויים להכריע בין רעילות רחבה ומיקוד מדויק.
תרופה ישנה עם כישרון חבוי
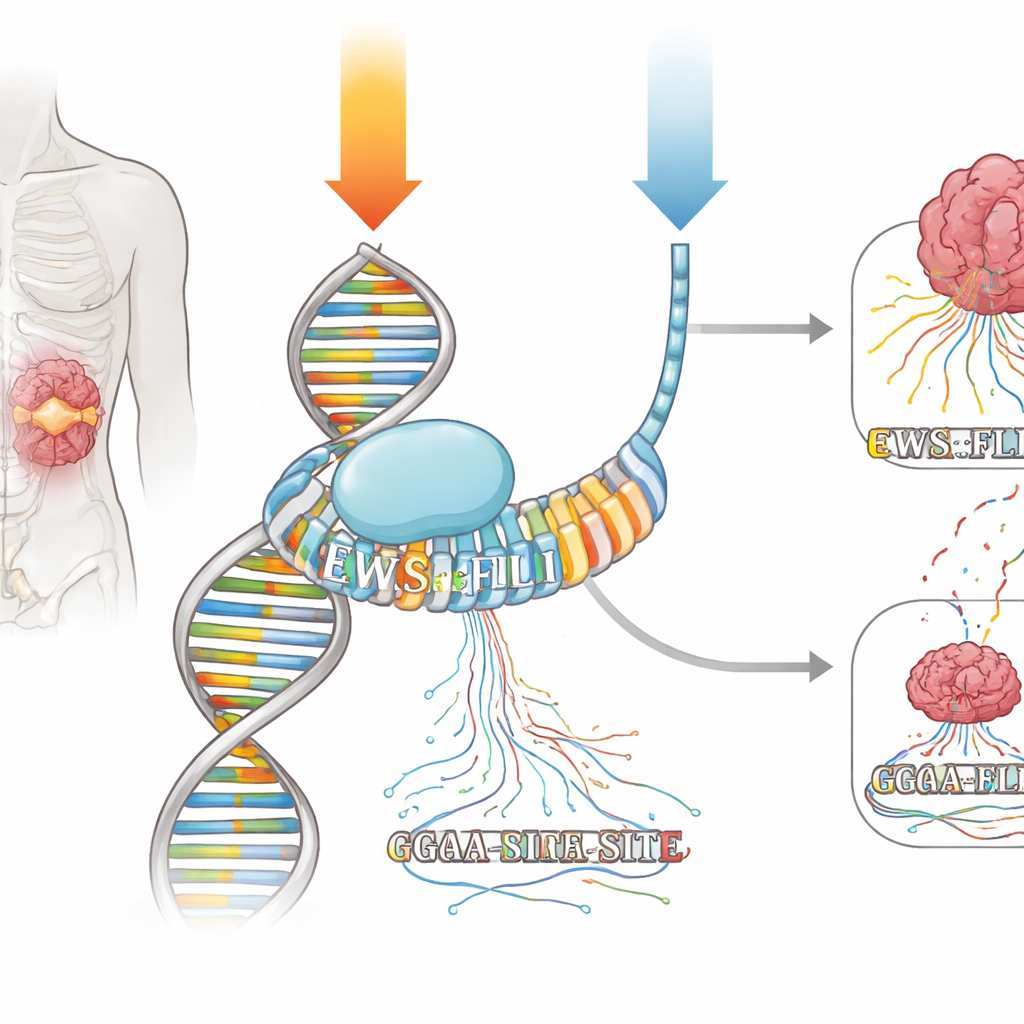
מיטרמיצין הוא מוצר טבעי שמתחכך בשקע המזערי של ה‑DNA, במיוחד ברצפים קצרים עשירים ב‑G ו‑C. במשך עשורים סווגה כ״כלי כימותרפי״ גס, שנתפס כגורם לנזק ל‑DNA ולחסימת שעתוק באופן כללי. עם זאת, רופאים בשנות ה‑60 דיווחו על תגובה מלאה בחולה עם סרקומת יווינג כאשר מיטרמיצין ניתן כמתן רציף למשך שבעה ימים. בשנים האחרונות, כאשר אותה תרופה נבדקה שוב אך ניתנה במנות יומיות קצרות, נצפה תועלת מינימלית בלבד. החוקרים שאפו להבין, בעזרת כלים גנומיים מודרניים, האם מיטרמיצין יכול לפעול כתרופה מדויקת נגד EWS::FLI1 — והאם לוח המינון מסביר את ההבדל הבולט בתגובות החולים.
כיצד מפעילים וכיבוי את הנהג פיוזיוני
EWS::FLI1 משתייך למשפחת גורמי השעתוק ETS, הנקשרים למילה פשוטה ב‑DNA המבוססת על ״GGAA״. בסרקומת יווינג, EWS::FLI1 נקשר בחוזקה לרצפים ארוכים של אתרי GGAA חוזרים, שמכונים מיקרוסטליטים, כדי להפעיל או לכבות רשתות גנים שלמות. הצוות חשף תאי סרקומת יווינג לשני פרוטוקולי מיטרמיצין שהניבו דיכוי דומה של גנים מרכזיים המופעלים על ידי EWS::FLI1: פולס קצר במנה גבוהה ומנה נמוכה שניתנה לפרק זמן ארוך יותר. באמצעות שיטות שממפות גם היכן EWS::FLI1 יושב על ה‑DNA וגם היכן מולקולות RNA חדשות נוצרות בזמן אמת, הם יכלו לעקוב כיצד כל פרוטוקול שינה את הקשירה והשעתוק ברחבי הגנום.
כיוונון עדין של מכונת השעתוק
בניגוד למחקרים ותאיים ישנים, מיטרמיצין לא פעל כסותם חסם שעתוק אוניברסלי ברמות הקליניות הרלוונטיות. בריכוזים נמוכים שנבחרו בזהירות, חשיפה רציפה שינתה בעיקר כיצד EWS::FLI1 מפעיל שעתוק באתרי היעד שלו. חלק מהפסגות של EWS::FLI1 על ה‑DNA החלישו, אחרות התחזקו, אך בשני המקרים ההשפעה הסופית הייתה ״הרעלת״ התוכנית: גנים שלרוב מופעלים על ידי הפיוז׳ן הושתקו, ואלו שהושתקו בדרך כלל שוחררו. בריכוזים גבוהים יותר, לעומת זאת, מיטרמיצין החל להפריע ליכולת של RNA פולימראז II — האנזים שמעביר DNA ל‑RNA — לנסוע לאורך גנים ארוכים. העיכוב הזה יצר אפקטים רחבים ולא ספציפיים, שמסגירים חלק מההיפוך הרצוי של פעילות EWS::FLI1, במיוחד לגבי גנים גדולים שדורשים תזוזה משמעותית של הפולימראז מקצה ההתחלה לקצה הסיום של הגן.
מיקוד בחוממות DNA במקום בכל הגנום
על ידי חפיפת מיפויי קשירה ושעתוק, החוקרים הראו שמיטרמיצין פועל בעוצמה המרבית באזורים העשירים ב‑GGAA שעליהם EWS::FLI1 תלוי. באותם מיקרוסטליטים ובאתרי GGAA מבודדים, מיטרמיצין במינון נמוך וברציפות לעתים הגדיל את תפוסת EWS::FLI1 אך עדיין עצר שעתוק פרודוקטיבי — המחשה ברורה לעקרון ״גולדילוקס״, שבו גם קשירה מועטה מדי וגם קשירה רבה מדי של גורם שעתוק עלולות לפגוע בפונקצייתו. באתרים אחרים שבהם EWS::FLI1 משתף פעולה עם גורמים סייעים כגון AP‑1, E2F או RUNX2, מיטרמיצין נטה לייצב פחות את המורכבים ולהפחית קשירה. בכל התרחישים הללו, התוצאה הסופית הייתה תבנית פעילות גנים נורמלית יותר בתאי הסרטן, עם הרבה פחות הפרעה לגנים שאינם קשורים כאשר התרופה נשמרה ברמה נמוכה ויציבה.
מהמנגנון במעבדה לאסטרטגיית טיפול טובה יותר
הצוות בדק אז האם התובנה המנגנונית חשובה גם בחיות חיות. בעכברים נשאים גידולי סרקומת יווינג, אותה המנה הכוללת של מיטרמיצין שניתנה כמתן רציף למשך שבעה ימים גרמה להתכווצות גידול דרמטית, בעוד שאותה כמות שניתנה בהזרקות יומיות הייתה הרבה פחות יעילה. באופן משמעותי, האפקט החזק הזה הופיע ללא סימנים לנזק DNA נוסף בגידולים, מה שמרמז כי היתרון נובע מתכנות מחודש של השעתוק ולא מפגיעה בגנום. אנלוג של מיטרמיצין חדש יותר ופחות רעיל, AIT‑102, הניב נסיגות גידול עוד יותר מרשימות ועמידות כאשר ניתן בהזנה רציפה במנות מתונות יחסית.
מה משמעות הדבר עבור טיפולים עתידיים בסרטן
בסך הכול, המחקר מציג את מיטרמיצין כפרוטוטיפ של ״מוודד גורמי שעתוק״ ולא כרעל שעתוק גס. על ידי קשירה סלקטיבית לרצפים ב‑DNA שבהם משתמשים EWS::FLI1 וגורמי ETS קשורים, היא יכולה לפרק רשת גנטית מונעת פיוז'ן שקשה מאוד לתקוף בתרופות רגילות. קריטי שהספציפיות הזו צצה רק בתוך חלון צר של מינון ולוח זמנים, שבו חשיפה רציפה ברמה נמוכה חוסמת את התוכנית האונקוגנית בלי לעכב באופן רחב את מכונת השעתוק של התא. הממצאים תומכים בכך שעבור תרופות שממוקדות לשעתוק וכרומטין, אופן המינה יכול להיות חשוב לא פחות מהמולקולה עצמה, והם תומכים בפיתוח קליני מחודש של אנלוגים של מיטרמיצין עבור סרקומת יווינג וסרטנים אחרים התלויים בגורמי שעתוק ממשפחת ETS.
ציטוט: Kaufman, R., Flores, G., Boguslawski, E.A. et al. Mithramycin alters EWS::FLI1 DNA binding and RNA polymerase II processivity to inhibit nascent transcription. Nat Commun 17, 2844 (2026). https://doi.org/10.1038/s41467-026-69488-9
מילות מפתח: סרקומת יווינג, מיטרמיצין, EWS::FLI1, מיקוד גורם שעתוק, לוח זמני מינון תרופתי