Clear Sky Science · ar
الميثراميسين يغيّر ارتباط EWS::FLI1 بالحمض النووي وقابلية بوليميراز الرنا II للتقدّم لكبح النسخ الوليد
لماذا هذا الأمر مهم لعلاج السرطان
سرطان إيوينغ هو سرطان عظم عدواني يصيب بشكل رئيسي الأطفال والشباب البالغين. يحركه بروتين اندماجي قوي، EWS::FLI1، يعيد توصيل طريقة خلية لقراءة حمضها النووي. تعيد هذه الدراسة النظر في دواء كيماوي قديم، الميثراميسين، وتظهر أن—إذا عُطي بالطريقة المناسبة—يمكنه كبح هذا البرنامج المحفز للسرطان بشكل انتقائي مع الحفاظ على جزء كبير من آلات الخلية الأخرى. تكشف الدراسة كيف أن الجرعة والجدول الزمني، وليس الدواء وحده، يمكن أن يصنعا الفرق بين السمية العامة والاستهداف الدقيق.
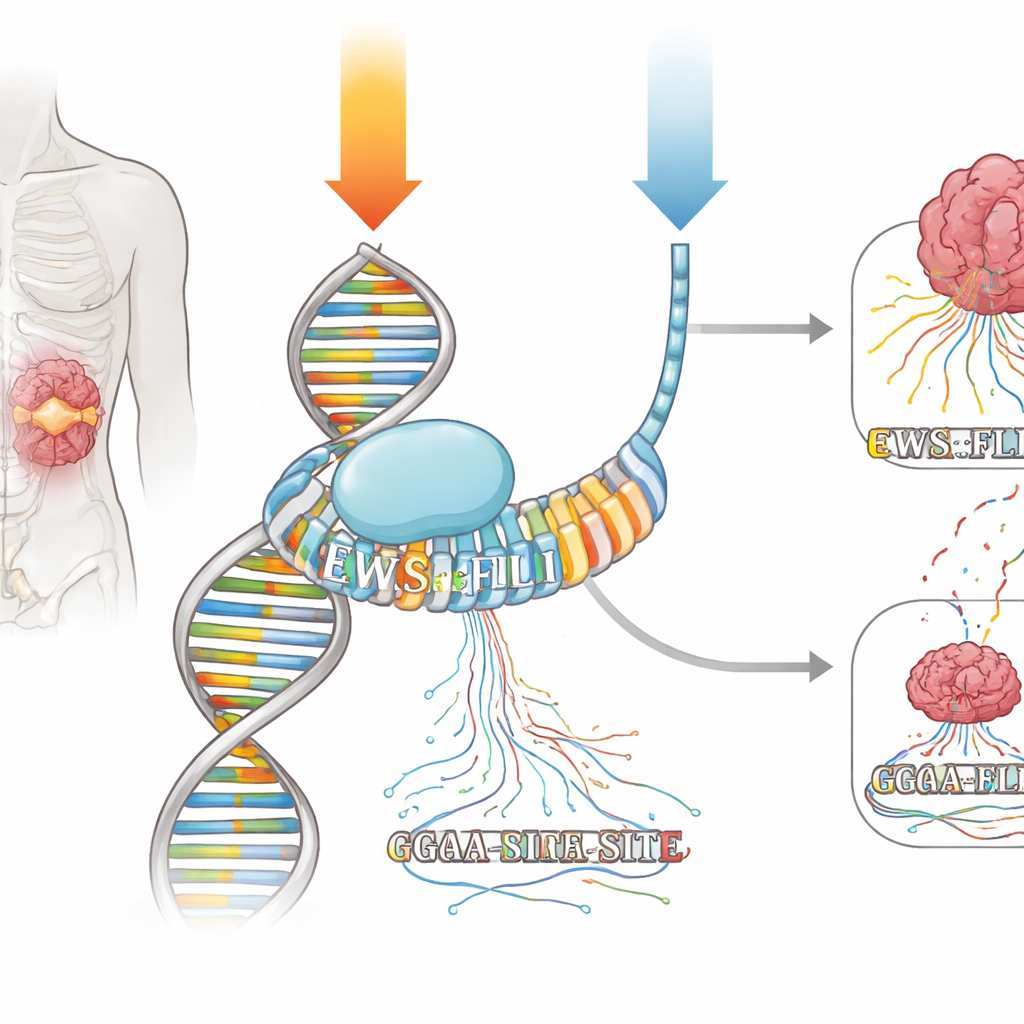
دواء قديم بموهبة خفية
الميثراميسين هو منتج طبيعي يتكئ في الأخدود الثانوي للـDNA، خصوصًا على مقاطع قصيرة غنية بالحروف G وC. لعقود اعتُبر أداة «كيماوية» خام، مفترَض أن تُلحق ضررًا بالـDNA وتمنع النسخ على نطاق واسع. مع ذلك، أفاد الأطباء في الستينيات عن استجابة كاملة لمريض مصاب بسرطان إيوينغ عندما أُعطي الميثراميسين بالتسريب المستمر لمدة سبعة أيام. وفي الآونة الأخيرة، عندما جُرِّب الدواء نفسه ولكن أُعطي على جرعات يومية قصيرة، لوحظت فوائد ضئيلة فقط. سعى المؤلفون لفهم، باستخدام أدوات جينومية حديثة، ما إذا كان الميثراميسين يمكن أن يعمل كدواء دقيق ضد EWS::FLI1—وما إذا كان جدول إعطائه يفسر الفارق اللافت في استجابات المرضى.
كيف يُشغّل ويُطفأ المحرك الاندماجي
ينتمي EWS::FLI1 إلى عائلة ETS من عوامل النسخ، التي تلتصق بكلمة DNA بسيطة مبنية حول "GGAA." في سرطان إيوينغ، يرتبط EWS::FLI1 بقوة خاصة بمجاميع طويلة مكررة من مواقع GGAA، تُسمى متواليات دقيقة (microsatellites)، ليشغل أو يثبط شبكات كاملة من الجينات. عرض الفريق خلايا سرطان إيوينغ لنظامي ميثراميسين نتجا عنهما تثبيط مماثل لجينات هدف رئيسية لـEWS::FLI1: نبضة قصيرة ذات جرعة عالية وجرعة أقل أعطيت لفترة أطول بكثير. باستخدام تقنيات ترسم أين يجلس EWS::FLI1 على الـDNA وأين تُصنع جزيئات الرنا الجديدة في الزمن الحقيقي، تمكنوا من مراقبة كيف غيّر كل نظام الارتباط والنسخ عبر الجينوم.
ضبط دقيق لآلية النسخ
على العكس من دراسات مخبرية أقدم، لم يعمل الميثراميسين ببساطة كعامل حاجب شامل للنسخ عند المستويات السريرية ذات الصلة. عند تركيزات منخفضة مختارة بعناية، غيّر التعرض المستمر بشكل رئيسي كيفية بدء EWS::FLI1 للنسخ في مواقع هدفه. أصبحت بعض قمم ارتباط EWS::FLI1 على الـDNA أضعف، وأخرى أقوى، لكن في كلتا الحالتين كان الأثر النهائي هو "تسميم" البرنامج: انخفضت الجينات التي يفعلها الاندماج عادة، وأُطلق سراح تلك التي كان يثبطها عادة. عند تركيزات أعلى، مع ذلك، بدأ الميثراميسين يتداخل مع قدرة بوليميراز الرنا II — الإنزيم الذي ينسخ الـDNA إلى رنا — على التحرك على طول الجينات الطويلة. هذا التوقف خلق آثارًا واسعة وغير متخصصة، مما طمس بعض الانعكاسات المرغوبة لنشاط EWS::FLI1، خصوصًا للجينات الكبيرة التي تحتاج بوليميراز للانتقال لمسافات طويلة من البداية إلى نهاية الجين.
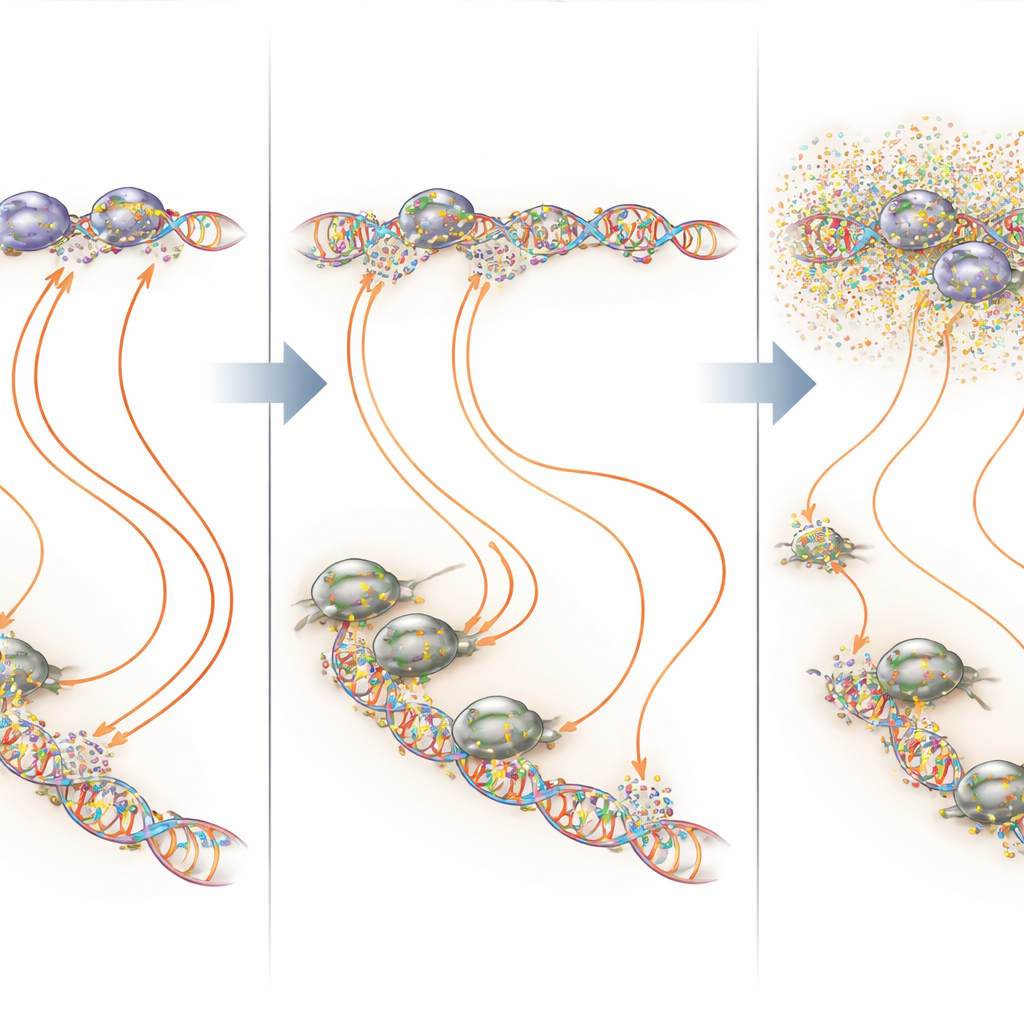
استهداف بقع ساخنة على الـDNA بدلًا من الجينوم بأكمله
عن طريق تراكب خرائط الارتباط والنسخ، أظهر الباحثون أن الميثراميسين يعمل بقوة أكبر في المناطق الغنية جدًا بـGGAA التي يعتمد عليها EWS::FLI1. في هذه المتواليات الدقيقة وفي مواقع GGAA المعزولة، غالبًا ما زاد التعرض المستمر منخفض الجرعة من شغل EWS::FLI1 لكنه مع ذلك أوقف النسخ المنتج — توضيح واضح لمبدأ "جولديلوكس"، حيث أن القليل جدًا أو الكثير جدًا من ارتباط عامل النسخ يمكن أن يضره في وظيفته. في مواقع أخرى حيث يشارك EWS::FLI1 شركاء معاونيين مثل AP-1 أو E2F أو RUNX2، كان الميثراميسين يميل إلى زعزعة استقرار هذه المعقدات وتقليل الارتباط. في كل هذه السيناريوهات، كانت النتيجة الصافية نمطًا أكثر طبيعية لنشاط الجينات في خلايا السرطان، مع إحداث اضطراب أقل بكثير للجينات غير المرتبطة عندما أُحتفظ بالدواء عند مستوى منخفض ومستمر.
من الآلية المخبرية إلى استراتيجية علاجية أفضل
اختبر الفريق بعد ذلك ما إذا كانت هذه الرؤية الميكانيكية مهمة في الحيوانات الحية. في فئران تحمل أورام سرطان إيوينغ، تسبب نفس الجرعة الإجمالية من الميثراميسين المعطاة كتسريب مستمر لمدة سبعة أيام في انكماش درامي للأورام، بينما كان نفس المقدار المقدم كحقن يومية أقل فعالية بكثير. ومن المهم أن هذا التأثير القوي حدث دون علامات لزيادة تلف الـDNA في الأورام، مما يشير إلى أن الفائدة تأتي من إعادة برمجة النسخ بدلًا من إتلاف الجينوم. أنتج نظير حديث من الميثراميسين أقل سمية، AIT-102، تراجعات أورامية أكثر إثارة وطويلة الأمد عندما أعطي بتسريب مستمر بجرعات متواضعة نسبيًا.
ماذا يعني هذا لعلاجات السرطان المستقبلية
عمومًا تكشف الدراسة عن الميثراميسين كنموذج لـ"معدّل عوامل النسخ" بدلًا من سم للنسخ خام. بالارتباط انتقائيًا بتسلسلات الـDNA التي يستخدمها EWS::FLI1 وعوامل ETS المرتبطة، يمكنه تفكيك شبكة جينية يقودها اندماج يصعب استهدافها بطرق أخرى. والأهم أن هذه الخصوصية تظهر فقط ضمن نافذة ضيقة من الجرعة والجدول، حيث يمنع التعرض المستمر منخفض المستوى البرنامج المسبب للورم دون عرقلة شاملة لآلية النسخ في الخلية. تدعم هذه النتائج فكرة أنه بالنسبة للأدوية التي تستهدف النسخ والكروماتين، يمكن أن تكون طريقة إعطاء الدواء مهمة بقدر أهمية المركب نفسه، وتؤيد تجديد التطوير السريري لنظائر الميثراميسين لسرطان إيوينغ وسرطانات أخرى تعتمد على عوامل ETS.
الاستشهاد: Kaufman, R., Flores, G., Boguslawski, E.A. et al. Mithramycin alters EWS::FLI1 DNA binding and RNA polymerase II processivity to inhibit nascent transcription. Nat Commun 17, 2844 (2026). https://doi.org/10.1038/s41467-026-69488-9
الكلمات المفتاحية: سرطان إيوينغ, الميثراميسين, EWS::FLI1, استهداف عوامل النسخ, جدول جرعات الدواء