Clear Sky Science · pl
Mithramycyna zmienia wiązanie EWS::FLI1 z DNA i procesywność polimerazy RNA II, aby zahamować transkrypcję nowo powstających RNA
Dlaczego ma to znaczenie dla terapii nowotworów
Mięsak Ewinga to agresywny nowotwór kości występujący głównie u dzieci i młodych dorosłych. Chorobę napędza silny białkowy fuzjomat EWS::FLI1, który przebudowuje sposób odczytywania DNA przez komórki. W tym badaniu ponownie zbadano stary lek chemioterapeutyczny, mithramycynę, i pokazano, że—przy odpowiednim sposobie podania—może ona selektywnie wyłączyć program napędzający ten rak, oszczędzając dużą część pozostałych mechanizmów komórkowych. Praca ujawnia, że to dawka i schemat dawkowania, a nie tylko sam lek, mogą decydować o różnicy między szeroką toksycznością a precyzyjnym celowaniem.
Stary lek z ukrytym talentem
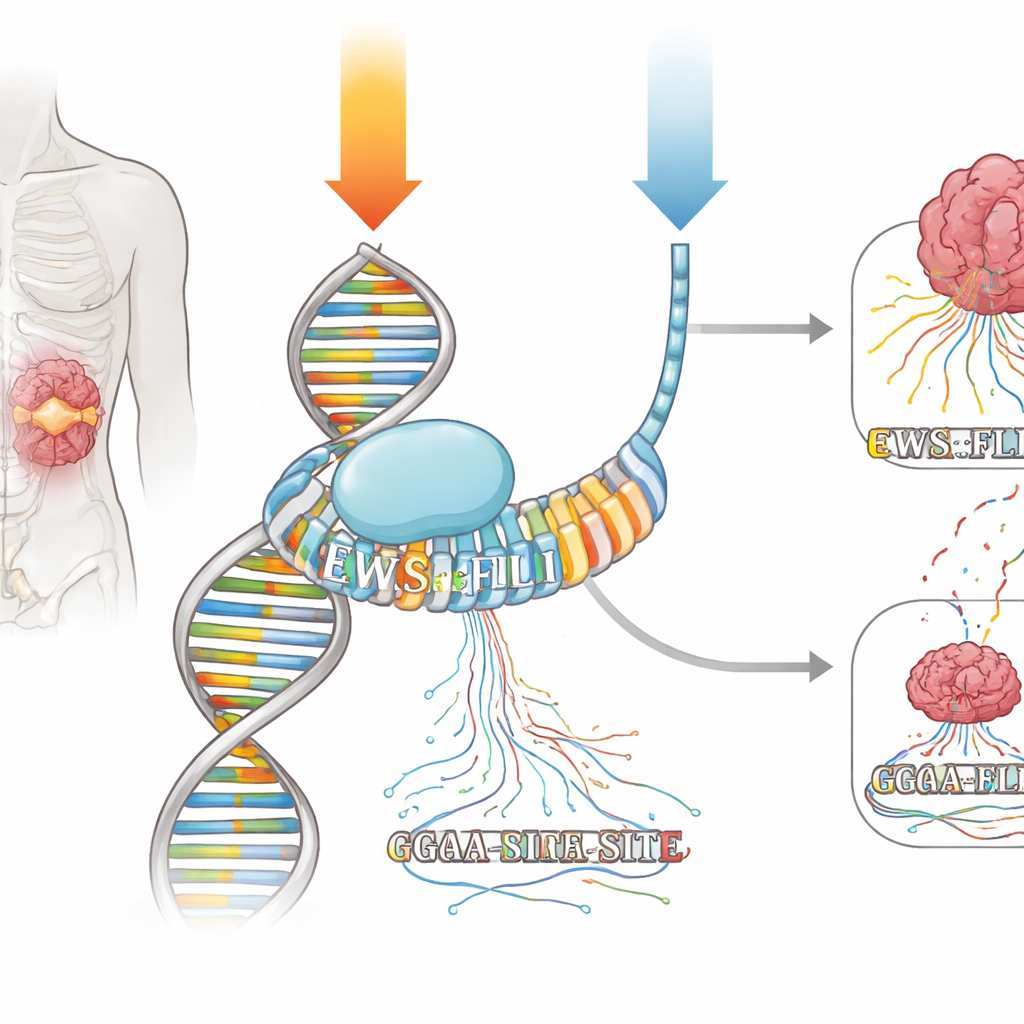
Mithramycyna jest produktem naturalnym, który wnika w rowek mniejszy podwójnej helisy DNA, szczególnie w krótkie odcinki bogate w nukleotydy G i C. Przez dekady była uznawana za tępą „chemioterapię”, zakładaną jako powodująca uszkodzenia DNA i blokująca transkrypcję na szeroką skalę. Jednak w latach 60. XX wieku lekarze opisali całkowitą remisję u pacjenta z mięsakem Ewinga, gdy mithramycyna była podawana jako ciągła, siedmiodniowa infuzja. Niedawniej, gdy ten sam lek testowano ponownie, ale jako krótkie, codzienne dawki, obserwowano jedynie minimalne korzyści. Autorzy postanowili zrozumieć, przy użyciu współczesnych narzędzi genomowych, czy mithramycyna może działać jako lek precyzyjny przeciw EWS::FLI1 — i czy harmonogram podawania wyjaśnia uderzającą różnicę w odpowiedziach pacjentów.
Jak włączany i wyłączany jest czynnik fuzji
EWS::FLI1 należy do rodziny czynników transkrypcyjnych ETS, które wiążą się z prostym słowem DNA opartym wokół „GGAA”. W mięsakach Ewinga EWS::FLI1 wiąże się szczególnie silnie z długimi ciągami powtarzających się miejsc GGAA, zwanymi mikrosatelitami, aby podnosić lub obniżać aktywność całych sieci genów. Zespół poddał komórki mięsaka Ewinga dwóm schematom podawania mithramycyny, które wywołały podobne tłumienie kluczowych genów docelowych EWS::FLI1: krótkiej, wysokodawkowej pulsacji oraz niższej dawki podawanej przez znacznie dłuższy czas. Korzystając z technik mapujących zarówno miejsca związania EWS::FLI1 z DNA, jak i miejsca, gdzie w czasie rzeczywistym powstają nowe cząsteczki RNA, mogli obserwować, jak każdy schemat zmieniał wiązanie i transkrypcję w całym genomie.
Dostrajanie aparatu transkrypcyjnego
Wbrew starszym badaniom in vitro, mithramycyna nie działała po prostu jako uniwersalny bloker transkrypcji przy klinicznie istotnych stężeniach. Przy starannie dobranych niskich stężeniach ciągła ekspozycja głównie zmieniała sposób, w jaki EWS::FLI1 inicjuje transkrypcję na swoich miejscach docelowych. Niektóre szczyty związania EWS::FLI1 na DNA osłabły, inne się wzmocniły, ale w obu przypadkach efekt końcowy polegał na „zatruwaniu” programu: geny zwykle aktywowane przez fuzję zostały wytłumione, a te normalnie hamowane — uwolnione. Przy wyższych stężeniach jednak mithramycyna zaczęła zakłócać zdolność polimerazy RNA II — enzymu kopiującego DNA na RNA — do przemieszczania się wzdłuż długich genów. To zatrzymanie powodowało szerokie, niespecyficzne efekty, maskując część pożądanej odwrotnej aktywności EWS::FLI1, szczególnie w przypadku dużych genów, które wymagały dalekiego przemieszczenia się polimerazy od początku do końca genu.
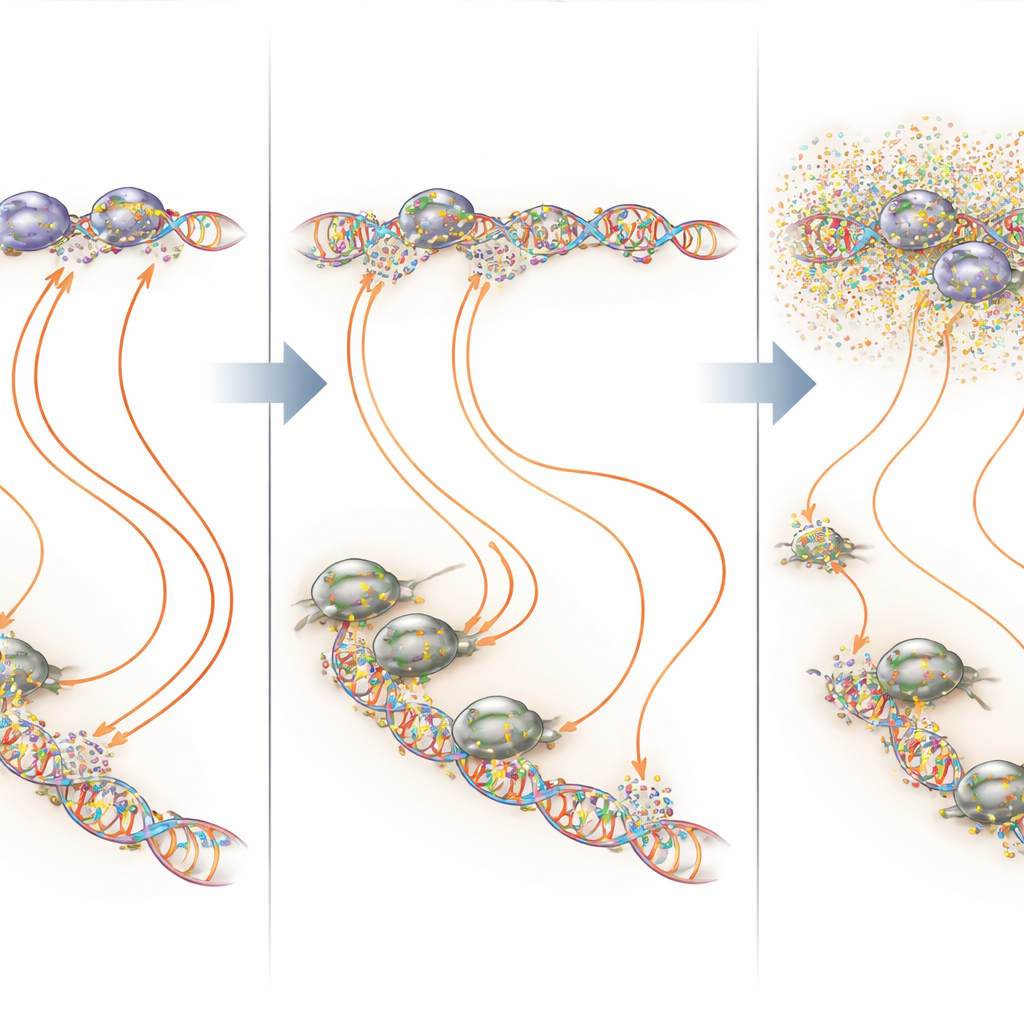
Celowanie w gorące punkty DNA zamiast całego genomu
Nakładając mapy wiązania i transkrypcji, badacze wykazali, że mithramycyna działa najsilniej w bardzo GGAA-bogatych regionach, od których zależy EWS::FLI1. W tych mikrosatelitach i w pojedynczych miejscach GGAA niskodawkowa, ciągła mithramycyna często zwiększała zajętość EWS::FLI1, ale nadal wyłączała produktywną transkrypcję — wyraźna ilustracja zasady „złotowłosej” (Goldilocks), gdzie zarówno zbyt małe, jak i zbyt intensywne wiązanie czynnika transkrypcyjnego może zaszkodzić jego funkcji. W innych miejscach, gdzie EWS::FLI1 współdziała z kofaktorami takimi jak AP-1, E2F czy RUNX2, mithramycyna miała tendencję do destabilizowania kompleksów i zmniejszania wiązania. We wszystkich tych scenariuszach wynik netto to bardziej normalny wzorzec aktywności genów w komórkach nowotworowych, przy znacznie mniejszym zakłóceniu genów niepowiązanych, gdy lek był utrzymywany na niższym, stałym poziomie.
Od mechanizmu w laboratorium do lepszej strategii leczenia
Zespół następnie sprawdził, czy ta wnikliwość mechanistyczna ma znaczenie in vivo. U myszy noszących guzy mięsaków Ewinga ta sama całkowita dawka mithramycyny podana jako siedmiodniowa ciągła infuzja spowodowała dramatyczne zmniejszenie guzów, podczas gdy ta sama ilość podana jako codzienne wstrzyknięcia była znacznie mniej skuteczna. Co ważne, silny efekt wystąpił bez oznak dodatkowych uszkodzeń DNA w guzach, co sugeruje, że korzyść wynika z przeprogramowania transkrypcji, a nie z uszkadzania genomu. Nowszy, mniej toksyczny analog mithramycyny, AIT-102, wywołał jeszcze bardziej spektakularne i trwałe regresje guzów, gdy był podawany w ciągłej infuzji w stosunkowo umiarkowanych dawkach.
Co to oznacza dla przyszłych terapii nowotworowych
Podsumowując, badanie ukazuje mithramycynę jako prototyp „modulatora czynników transkrypcyjnych”, a nie jako prymitywną truciznę transkrypcyjną. Poprzez selektywne wiązanie się z sekwencjami DNA wykorzystywanymi przez EWS::FLI1 i pokrewne czynniki ETS, może ona rozmontować sieć genów napędzaną przez fuzję, którą w przeciwnym razie trudno leczyć farmakologicznie. Kluczowe jest to, że ta specyficzność ujawnia się tylko w wąskim oknie dawki i schematu, gdzie ciągła niskopoziomowa ekspozycja blokuje onkogenny program bez szerokiego zatrzymywania aparatu transkrypcyjnego komórki. Wyniki te sugerują, że dla leków celujących w transkrypcję i chromatynę sposób podania może być równie ważny jak sama molekuła, i wspierają odnowiony rozwój kliniczny analogów mithramycyny w leczeniu mięsaka Ewinga oraz innych nowotworów zależnych od czynników transkrypcyjnych ETS.
Cytowanie: Kaufman, R., Flores, G., Boguslawski, E.A. et al. Mithramycin alters EWS::FLI1 DNA binding and RNA polymerase II processivity to inhibit nascent transcription. Nat Commun 17, 2844 (2026). https://doi.org/10.1038/s41467-026-69488-9
Słowa kluczowe: Mięsak Ewinga, mithramycyna, EWS::FLI1, celowanie w czynniki transkrypcyjne, harmonogram dawkowania leku