Clear Sky Science · ru
Митрамицин изменяет связывание EWS::FLI1 с ДНК и процессивность РНК-полимеразы II, чтобы подавить новообразующуюся транскрипцию
Почему это важно для лечения рака
Саркома Юинга — агрессивный рак кости, который в основном поражает детей и молодых взрослых. Её драйвером является мощный белок-фьюжн EWS::FLI1, который перенастраивает то, как клетки считывают свою ДНК. В этом исследовании пересматривается старое химиотерапевтическое средство — митрамицин — и показано, что при правильном режиме введения он способен селективно выключать эту онкопрограммус, при этом сохраняя большую часть остального транскрипционного аппарата клетки. Работа демонстрирует, что важна не только сама молекула, но и доза и график введения: они могут определить границу между широкой токсичностью и точечным воздействием.
Старый препарат с неожиданным талантом
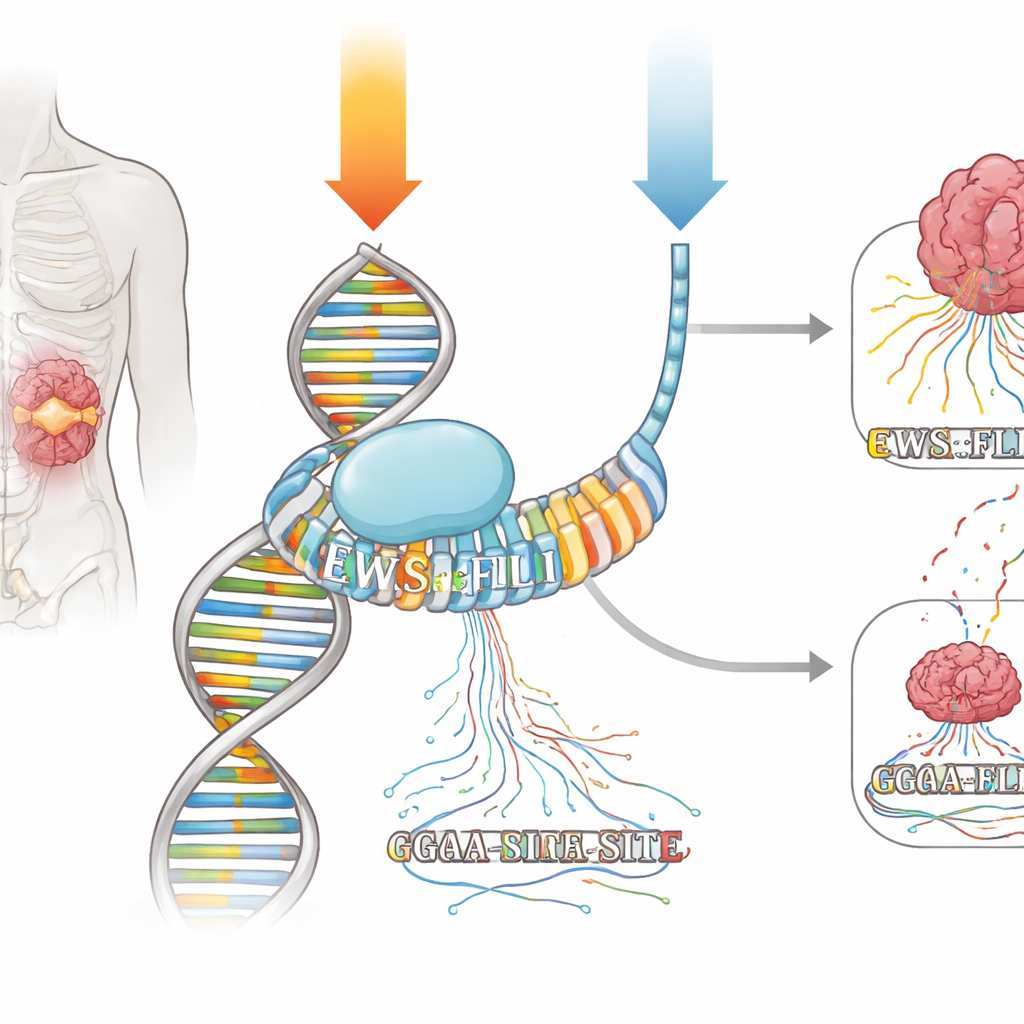
Митрамицин — природный продукт, который внедряется в малый желобок ДНК, особенно на коротких участках, богатых нуклеотидами G и C. Десятилетиями его считали грубым «химиотерапевтическим» средством, полагая, что он повреждает ДНК и повсеместно блокирует транскрипцию. Однако в 1960‑х годах клиницисты зафиксировали полный ответ у пациента с саркомой Юинга при семидневной непрерывной инфузии митрамцина. Позже, когда препарат снова тестировали в виде коротких ежедневных дозировок, польза была минимальной. Авторы поставили цель с помощью современных геномных методов выяснить, может ли митрамицин действовать как прецизионный препарат против EWS::FLI1 и объясняет ли режим введения резкую разницу в клинических ответах.
Как драйвер-фьюжн включается и выключается
EWS::FLI1 относится к семейству факторов транскрипции ETS, которые связываются с простым ДНК‑словом на основе «GGAA». В саркоме Юинга EWS::FLI1 особенно прочно связывается с длинными участками повторяющихся сайтов GGAA — так называемыми микросателлитами — чтобы включать или выключать целые сети генов. Команда обработала клетки саркомы Юинга двумя режимами митрамицина, которые давали схожее подавление ключевых генов‑мишеней EWS::FLI1: краткий высокодозный импульс и более низкая доза, введённая в течение длительного времени. С помощью методов, картирующих как места связывания EWS::FLI1 на ДНК, так и места синтеза новой РНК в реальном времени, они отслеживали, как каждый режим изменял связывание и транскрипцию по всему геному.
Тонкая настройка транскрипционного аппарата
Вопреки старым in vitro данным, при клинически релевантных уровнях митрамицин не действовал как универсальный блокатор транскрипции. При тщательно подобранных низких концентрациях непрерывное воздействие в основном меняло то, как EWS::FLI1 инициирует транскрипцию на своих мишенях. Некоторые пики связывания EWS::FLI1 на ДНК ослабевали, другие — усиливались, но в обоих случаях итогом было «отравление» онкопрограммы: гены, обычно активируемые фьюжном, подавлялись, а те, что подавлялись, освобождались. При более высоких концентрациях митрамицин начал мешать способности РНК‑полимеразы II — фермента, копирующего ДНК в РНК — продвигаться по длинным генам. Такое «застревание» вызывало широкие неспецифические эффекты, которые маскировали желаемую инверсию активности EWS::FLI1, особенно для больших генов, где полимеразе требуется пройти значительное расстояние от начала до конца транскрипта.
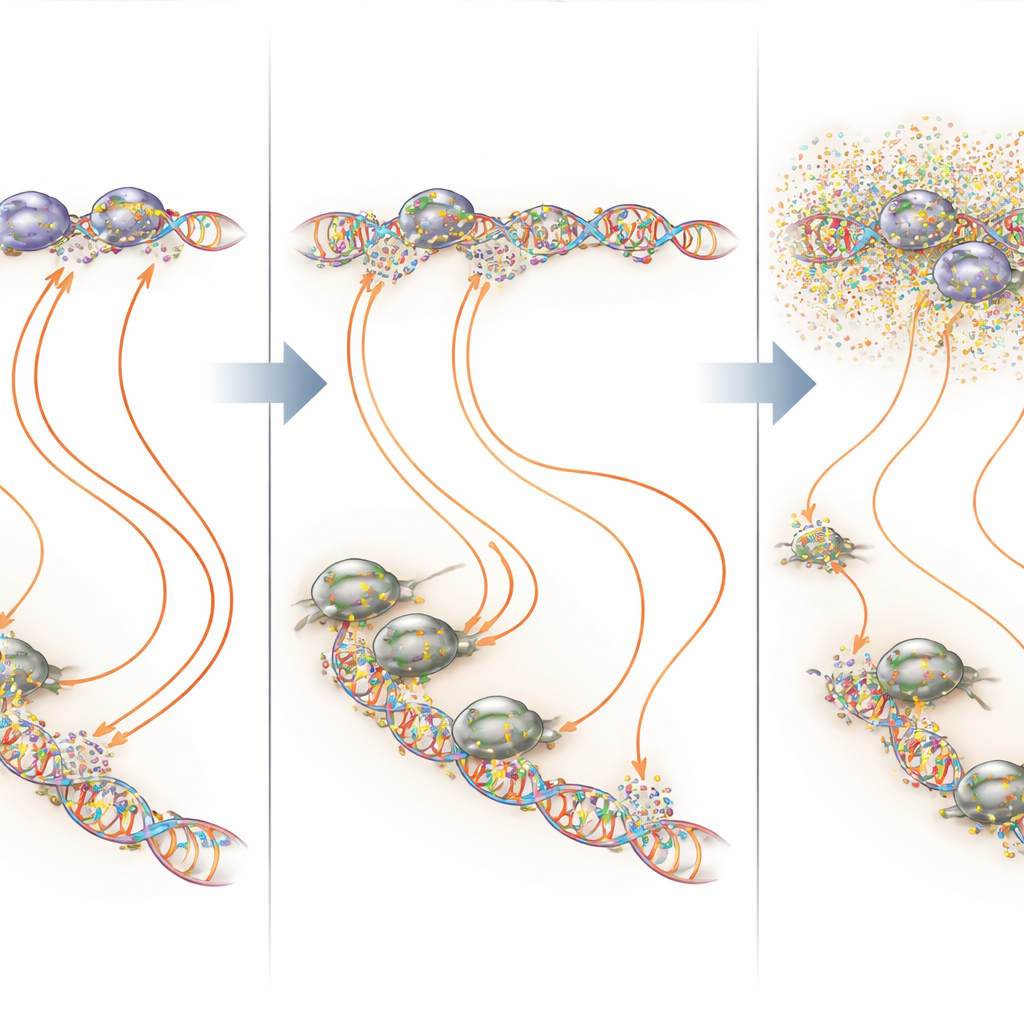
Ориентация на горячие точки ДНК вместо всего генома
Наложив карты связывания и транскрипции, исследователи показали, что митрамицин наиболее сильный в тех самых участках, богатых GGAA, от которых зависит EWS::FLI1. На этих микросателлитах и на изолированных GGAA‑сайтах низкодозовая непрерывная терапия часто увеличивала занятость EWS::FLI1, но при этом всё равно блокировала продуктивную транскрипцию — наглядная иллюстрация принципа «Златовласки», когда и слишком слабое, и слишком сильное связывание фактора транскрипции вредно для его функции. На других участках, где EWS::FLI1 работает совместно с кофакторами, такими как AP‑1, E2F или RUNX2, митрамицин склонялся к дестабилизации комплексов и уменьшению связывания. Во всех этих сценариях суммарный эффект заключался в большей нормализации паттерна активности генов в опухолевых клетках и в гораздо меньшем нарушении несвязанных генов при поддержании низкой, стабильной концентрации препарата.
От лабораторного механизма к более удачной лечебной стратегии
Далее команда проверила, имеет ли это механизмальное понимание значение в живых организмах. У мышей с опухолями саркомы Юинга та же суммарная доза митрамицина, введённая семидневной непрерывной инфузией, вызвала драматическое уменьшение размеров опухолей, тогда как тот же объём, доставленный в виде ежедневных инъекций, был гораздо менее эффективен. Важно, что этот мощный эффект наблюдался без признаков дополнительного повреждения ДНК в опухолях, что указывает на то, что польза связана с перепрограммированием транскрипции, а не с повреждением генома. Новый, менее токсичный аналог митрамицина — AIT‑102 — давал ещё более заметные и устойчивые регрессии опухолей при непрерывной инфузии в относительно умеренных дозах.
Что это значит для будущих противораковых терапий
В целом исследование выявляет митрамицин как прототип «модулятора фактора транскрипции», а не грубого «ядовитого» блокатора транскрипции. Селективно связываясь с последовательностями ДНК, используемыми EWS::FLI1 и родственными факторами ETS, он способен разрушать сеть генов, управляемую фьюжном, которую в противном случае очень трудно таргетировать лекарствами. Критически важно, что эта специфичность проявляется только в узком окне дозы и режима введения, когда непрерывное низкоуровневое воздействие блокирует онкогенную программу, не вызывая широкого торможения транскрипционного аппарата клетки. Эти выводы свидетельствуют о том, что для препаратов, нацеленных на транскрипцию и хроматин, способ введения может быть столь же важен, как и сама молекула, и поддерживают возобновление клинической разработки аналогов митрамицина для саркомы Юинга и других раков, зависящих от факторов транскрипции ETS.
Цитирование: Kaufman, R., Flores, G., Boguslawski, E.A. et al. Mithramycin alters EWS::FLI1 DNA binding and RNA polymerase II processivity to inhibit nascent transcription. Nat Commun 17, 2844 (2026). https://doi.org/10.1038/s41467-026-69488-9
Ключевые слова: Саркома Юинга, митрамицин, EWS::FLI1, мишенирование факторов транскрипции, схема дозирования лекарств