Clear Sky Science · es
Mithramycin altera la unión de EWS::FLI1 al ADN y la procesividad de la ARN polimerasa II para inhibir la transcripción naciente
Por qué esto importa para el tratamiento del cáncer
El sarcoma de Ewing es un cáncer óseo agresivo que afecta principalmente a niños y adultos jóvenes. Está impulsado por una potente proteína de fusión, EWS::FLI1, que reconfigura cómo las células leen su ADN. Este estudio revisita un fármaco de quimioterapia antiguo, la mithramicina, y muestra que —si se administra de la forma adecuada— puede apagar selectivamente este programa oncogénico mientras preserva gran parte de la maquinaria celular restante. El trabajo revela cómo la dosis y el calendario, no solo el fármaco en sí, pueden marcar la diferencia entre una toxicidad amplia y un apuntado preciso.
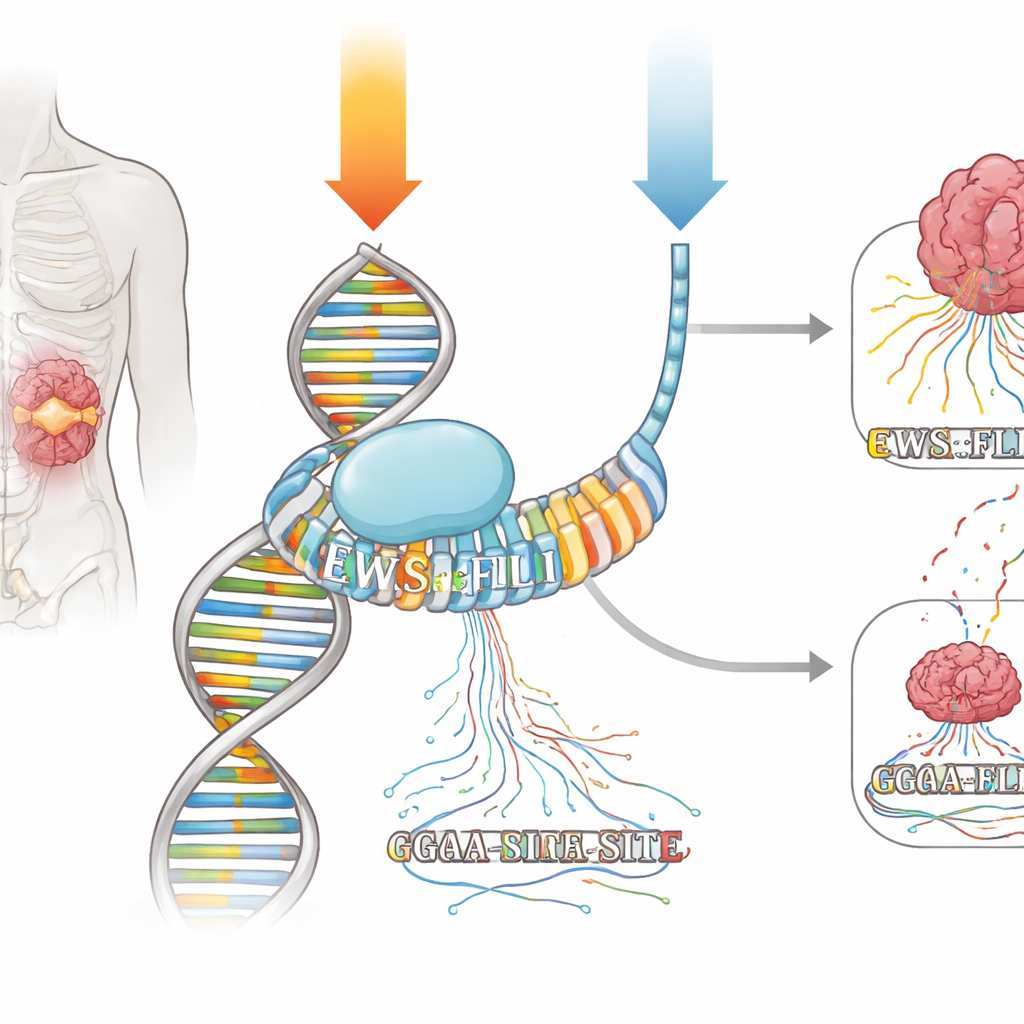
Un fármaco viejo con un talento oculto
La mithramicina es un producto natural que se encaja en la ranura menor del ADN, especialmente en secuencias cortas ricas en las letras G y C. Durante décadas se la consideró una herramienta “quimioterápica” contundente, asumida como causante de daño al ADN y bloqueadora general de la transcripción. Sin embargo, médicos en la década de 1960 informaron una respuesta completa en un paciente con sarcoma de Ewing cuando la mithramicina se administró como una infusión continua de siete días. Más recientemente, cuando el mismo fármaco se probó de nuevo pero administrado en dosis diarias cortas, solo se observó un beneficio mínimo. Los autores se propusieron entender, con herramientas genómicas modernas, si la mithramicina puede actuar como un fármaco de precisión contra EWS::FLI1 —y si su pauta de administración explica la notable diferencia en las respuestas de los pacientes.
Cómo se enciende y apaga el impulsor de fusión
EWS::FLI1 pertenece a la familia ETS de factores de transcripción, que se adhieren a una palabra simple del ADN construida alrededor de “GGAA”. En el sarcoma de Ewing, EWS::FLI1 se une especialmente con fuerza a largas series repetidas de sitios GGAA, llamadas microsatélites, para activar o reprimir redes enteras de genes. El equipo expuso células de sarcoma de Ewing a dos regímenes de mithramicina que produjeron una supresión similar de genes diana clave de EWS::FLI1: una pulsación breve de alta dosis y una dosis más baja administrada durante mucho más tiempo. Usando técnicas que mapean tanto dónde se asienta EWS::FLI1 en el ADN como dónde se están sintetizando nuevas moléculas de ARN en tiempo real, pudieron observar cómo cada régimen cambiaba la unión y la transcripción en todo el genoma.
Ajustando finamente la maquinaria de transcripción
Contrariamente a estudios in vitro antiguos, la mithramicina no actuó simplemente como un bloqueador universal de la transcripción a niveles clínicamente relevantes. A concentraciones bajas cuidadosamente elegidas, la exposición continua alteró principalmente cómo EWS::FLI1 inicia la transcripción en sus sitios diana. Algunos picos de EWS::FLI1 en el ADN se hicieron más débiles, otros más fuertes, pero en ambos casos el efecto posterior fue “envenenar” el programa: los genes normalmente activados por la fusión se redujeron, y los normalmente reprimidos se liberaron. Sin embargo, a concentraciones más altas, la mithramicina empezó a interferir con la capacidad de la ARN polimerasa II —la enzima que copia ADN en ARN— para desplazarse a lo largo de genes largos. Ese estancamiento generó efectos amplios y no específicos, enmascarando parte del deseable restablecimiento de la actividad de EWS::FLI1, en particular en genes grandes que requieren que la polimerasa se mueva lejos del inicio hasta el final del gen.
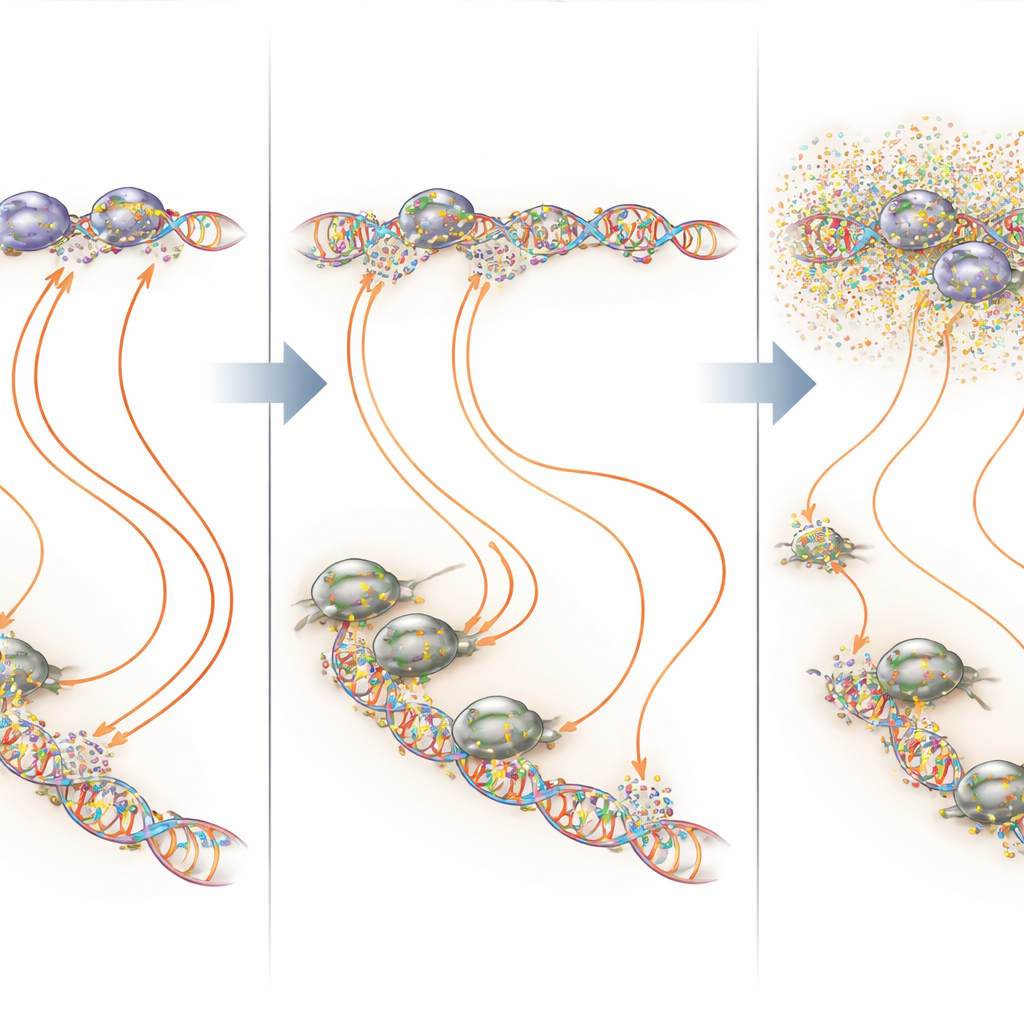
Apuntar a puntos calientes del ADN en lugar de al genoma entero
Al superponer los mapas de unión y transcripción, los investigadores mostraron que la mithramicina actúa con más fuerza en las regiones muy ricas en GGAA de las que depende EWS::FLI1. En estos microsatélites y en sitios GGAA aislados, la mithramicina continua a baja dosis con frecuencia aumentó la ocupación de EWS::FLI1 pero aún así inhibió la transcripción productiva —una ilustración clara del principio de “Ricitos de Oro”, donde tanto muy poca como demasiada unión de un factor de transcripción pueden perjudicar su función. En otros sitios donde EWS::FLI1 se asocia con cofactores como AP-1, E2F o RUNX2, la mithramicina tendió a desestabilizar los complejos y reducir la unión. En todos estos escenarios, el resultado neto fue un patrón de actividad génica más normal en las células cancerosas, con mucha menos alteración de genes no relacionados cuando el fármaco se mantuvo en un nivel bajo y constante.
Del mecanismo en el laboratorio a una mejor estrategia terapéutica
El equipo comprobó luego si este conocimiento mecanístico importaba en animales vivos. En ratones portadores de tumores de sarcoma de Ewing, la misma dosis total de mithramicina administrada como una infusión continua de siete días provocó una reducción dramática del tumor, mientras que la misma cantidad administrada como inyecciones diarias fue mucho menos efectiva. De forma importante, este efecto potente ocurrió sin señales de daño adicional al ADN en los tumores, lo que sugiere que el beneficio proviene de la reprogramación de la transcripción más que de lesionarlo genómico. Un análogo más nuevo y menos tóxico de la mithramicina, AIT-102, produjo regresiones tumorales aún más llamativas y duraderas cuando se administró por infusión continua a dosis relativamente modestas.
Qué significa esto para las terapias contra el cáncer en el futuro
En conjunto, el estudio revela a la mithramicina como un prototipo de “modulador de factores de transcripción” más que como un veneno tosco de la transcripción. Al unirse selectivamente a secuencias de ADN utilizadas por EWS::FLI1 y factores ETS relacionados, puede desmantelar una red génica impulsada por una fusión que de otro modo es muy difícil de medicar. De forma crucial, esta especificidad surge solo dentro de una ventana estrecha de dosis y esquema, donde la exposición continua a bajo nivel bloquea el programa oncogénico sin frenar ampliamente la maquinaria de transcripción de la célula. Estos hallazgos sostienen que, para fármacos que apuntan a la transcripción y la cromatina, la forma en que administramos el fármaco puede ser tan importante como la molécula misma, y respaldan el desarrollo clínico renovado de análogos de mithramicina para el sarcoma de Ewing y otros cánceres que dependen de factores de transcripción ETS.
Cita: Kaufman, R., Flores, G., Boguslawski, E.A. et al. Mithramycin alters EWS::FLI1 DNA binding and RNA polymerase II processivity to inhibit nascent transcription. Nat Commun 17, 2844 (2026). https://doi.org/10.1038/s41467-026-69488-9
Palabras clave: Sarcoma de Ewing, mithramicina, EWS::FLI1, apuntado a factores de transcripción, esquema de dosificación de fármacos