Clear Sky Science · tr
tRNA antikodon sap halkasında PUS enzimlerinin etkileşimini ortaya koyan küçük RNA psiuridinasyonunun nicel analizi
RNA üzerindeki gizli işaretlerin önemi
Her hücre, proteinleri oluşturmak ve diğer RNA’ları işlemek için küçük RNA moleküllerini kullanarak sürekli genetik talimatları okur. Bu çalışma, bu RNA’larda genetik diziyi değiştirmeden davranışlarını etkileyebilen ince bir kimyasal değişiklik olan psiuridini inceliyor. Bu değişikliklerin tam olarak nerede oluştuğunu ve hangi enzimlerin yerleştirdiğini haritalayarak, yazarlar protein üretim mekanizmasının kritik bir bölümünü ince ayarlayan beklenmedik bir enzimler arası “konuşma”yı ortaya koyuyorlar.
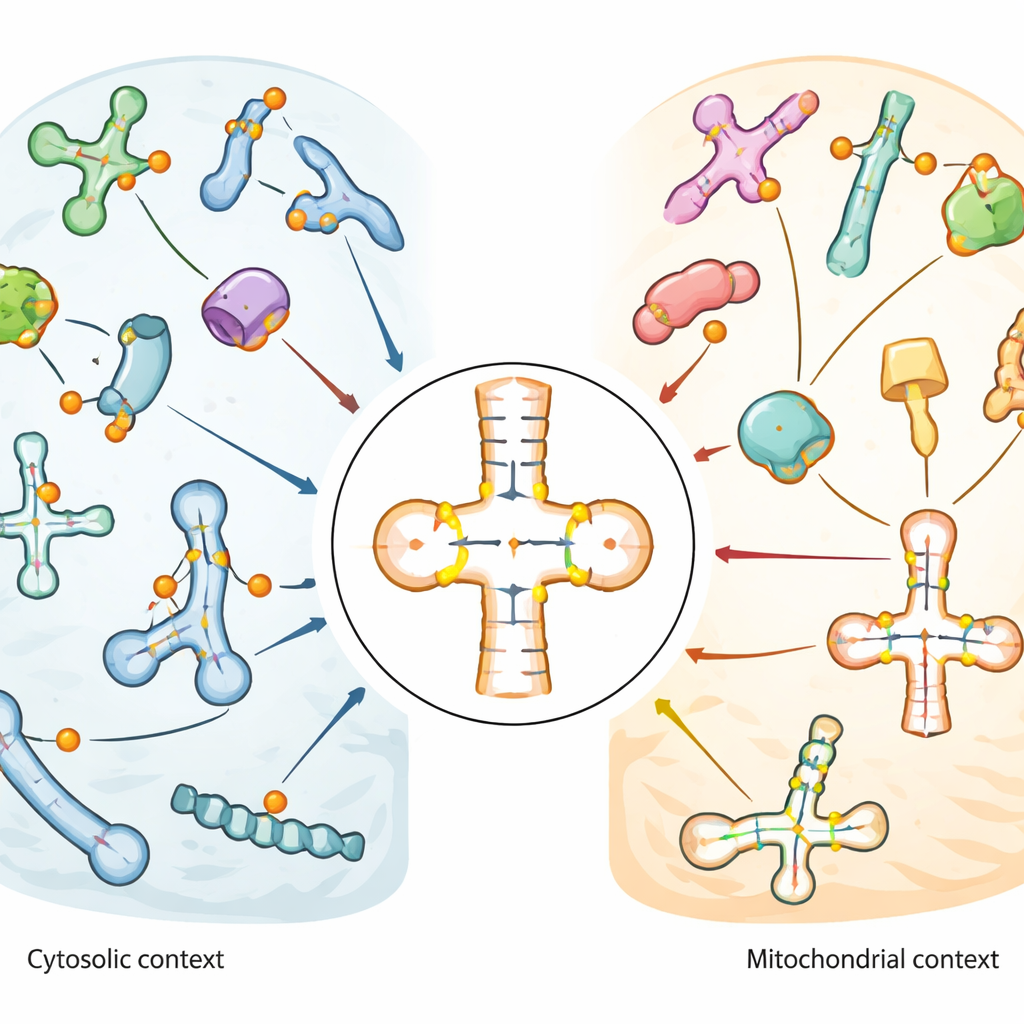
Hücrenin iş yapan RNA’larındaki kimyasal düzenlemeler
Hücreler birçok tür küçük RNA’ya, özellikle genetik koddaki üç harfli kelimeleri okuyup protein sentezi sırasında doğru aminoasidi taşıyan adaptörler olan transfer RNA’larına (tRNA’lar) güvenir. Bu tRNA’lar ve RNA işlenmesini yönlendiren diğer küçük RNA’lar, yoğun kimyasal modifikasyonlarla süslenmiştir. Psiuridin bunların en yaygın olanlarından biridir. Sadece atom bağlantılarındaki farklılıkla sıradan uridinden ayrılır, ama bu küçük değişiklik baz eşleşmesini güçlendirir ve RNA’nın biçimini ve kararlılığını değiştirebilir. Psiuridinin stres yanıtları, beyin fonksiyonu ve kanserle ilişkisi olduğundan, bilim insanları tam olarak nerede göründüğünü ve bunlardan sorumlu olan enzimlerin —psiuridin sentetazları ya da PUS enzimleri— hangileri olduğunu bilmek istiyorlar.
Psiuridinin hassas bir haritasını oluşturmak
Geleneksel yöntemler birçok psiuridin sitesini işaretleyebilse de her bir sitede ne ölçüde modifikasyon olduğunu ölçmekte zorlanıyordu. Araştırmacılar, daha önce geliştirdikleri PRAISE adlı kimyasal‑sekanslama yöntemini küçük RNA’larda nicel olarak yapmak üzere rafine ettiler. Önce diğer engelleyici modifikasyonları gidermek için RNA’yı işlediler, sonra psiuridinin varlığını okuma çıktısında karakteristik bir delesyon sinyaline dönüştüren uzmanlaşmış bir bisülfit reaksiyonu ve sekanslama stratejisi kullandılar. Bunu insan HEK293T hücrelerine uygulayarak sitozolik ve mitokondriyal tRNA’lar ile küçük nükleer RNA’lar (snRNA’lar) ve küçük nükleolar RNA’lar (snoRNA’lar) genelinde yüksek çözünürlüklü bir psiuridin manzarası ürettiler. Yöntem son derece tekrarlanabilir çıktı verdi ve var olan tekniklerle eşleşti ya da onları aştı; ayrıca her pozisyondaki modifikasyon düzeylerinin hassas ölçümlerini ekledi.
Farklı hücresel çevrelerde ayrı desenler
Harita, psiuridinin özellikle tRNA’ların doğrudan haberci RNA ile eşleşen bölgesi olan antikodon sap‑halkasında zenginleştiğini ortaya koydu. tRNA’nın tabanına yakın evrensel olarak bulunan bir pozisyon (55. pozisyon olarak bilinir) gibi bazı pozisyonlar birçok tRNA’da neredeyse tamamen modifiye edilmişti. Diğerleri ılımlı ya da değişken seviyeler göstererek düzenleyici bir esneklik önerdi. Enerji üreten organellerin içinde çalışan mitokondriyal tRNA’lar belirgin şekilde farklı bir desen sergiledi: sitozolik tRNA’larda yaygın olan kilit pozisyonlar ya yoktu ya zayıfça modifiye olmuştu, oysa antikodona yakın diğer pozisyonlar güçlü ve tutarlı şekilde işaretlenmişti. Bu kontrast, mitokondrilerin kendi tRNA’ları için farklı bir düzenleme kuralı seti kullandığını düşündürüyor. snRNA’lar ve snoRNA’larda ise psiuridin, diğer RNA modifikasyonlarını veya splicing’i yönlendiren işlevsel bölgelerde kümelendi ve bazı siteler ısı şoku veya oksidatif stres gibi koşullara yanıt olarak değişiklik gösterdi.
İşaretleri kim yazıyor: enzimlerin sitelere atanması
Belli enzimleri belli RNA sitelerine bağlamak için ekip, vahşi tip hücreleri tek tek PUS enzimlerinden yoksun hücre hatlarıyla veya DKC1 adlı bir kılavuz enzimin azaltılmış seviyeleriyle karşılaştırdı. snoRNA işaretlerinin iki yolla oluştuğunu gösterdiler: DKC1 kullanan RNA‑kılavuzlu bir yol ve tek başına tek bir ayırt edici siteyi yazan PUS7 enzimi. tRNA’larda birçok siteyi sistematik olarak belirli enzimlere atadılar. PUS1, antikodona yakın bölgelerde hem sitozolik hem mitokondriyal tRNA’larda önemli bir işaretleyici olarak ortaya çıktı. RluA ailesinin üyeleri görevlerini paylaştı: RPUSD1 sitozolik tRNA’ların belirli pozisyonlarını, tRNA kuyruğuna yakın daha önce tanınmamış bir pozisyon da dahil olmak üzere modifiye ederken RPUSD2 mitokondriyal tRNA’lardaki yakın pozisyonları hedefledi ve RPUSD3’te tRNA aktivitesi tespit edilmedi. İlişkili enzimler PUS1L ve PUS7L ise farklı bölgelerde veya tRNA tiplerinde uzmanlaştılar; bu da yakın akraba proteinlerin şaşırtıcı derecede farklı görevler evrimleştirebileceğini gösteriyor.
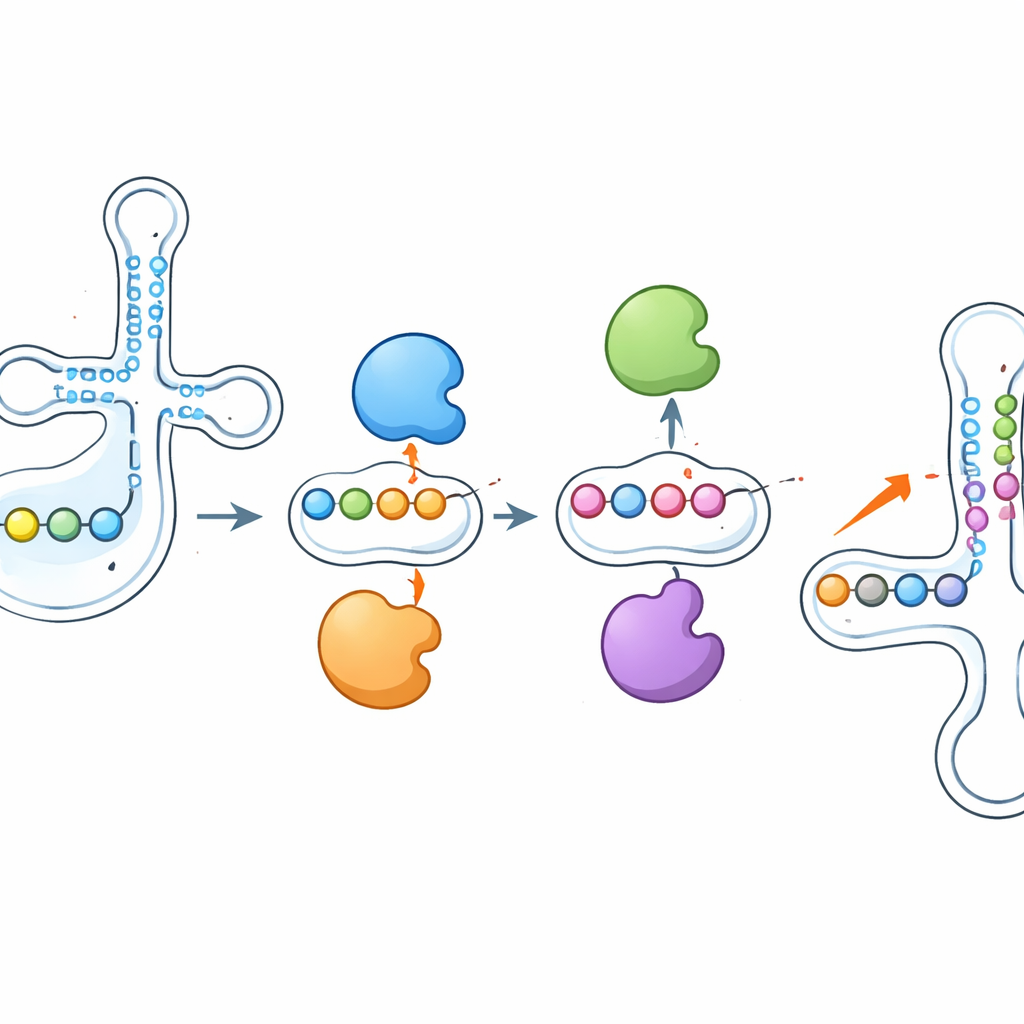
Enzimlerin birbirlerinin işini itip çekmesi
En çarpıcı bulgulardan biri, bu enzimlerin izole çalışmadıklarıydı. Araştırmacılar PUS1’i sildiklerinde, normalde antikodona yakın yazdığı psiuridin işaretleri keskin şekilde düştü—ama aynı tRNA üzerindeki RPUSD1 veya PUS7 gibi diğer enzimlerin yazdığı komşu siteler daha yoğun modifiye hale geldi. RPUSD1’in yok edilmesi örtüşen pozisyonlarda ters etkiyi verdi ve benzer terazi‑hareketleri PUS7 ile başka bir enzim olan PUS3 arasında da görüldü. Bu değişiklikler enzim veya tRNA bolluğundaki kaymalarla açıklanmadı; bunun yerine bireysel tRNA moleküller düzeyinde doğrudan bir etkileşime işaret etti. Yazarlar, enzimlerin yakın bağlanma bölgeleri için fiziksel olarak rekabet ediyor olabileceğini ya da bir psiuridinin eklenmesinin veya kaldırılmasının yerel RNA yapısını yeniden şekillendirerek komşu pozisyonları diğer enzimler için daha erişilebilir veya daha erişilemez hale getirebileceğini öne sürüyorlar.
Sağlık ve hastalık için anlamı
Uzman olmayan bir okuyucu için ana mesaj, tRNA’lardaki kimyasal işaretlerin sabit süslemeler değil, dinamik ve birbirine bağlı bir sistemin parçası olduğudur. Birden çok enzim antikodon bölgesini desenleyip buna göre işbirliği yapar ve rekabet eder; bu bölge genetik kodun doğru ve esnek şekilde okunmasında merkezidir. Bu enzimlerin birkaçındaki mutasyonların kan hastalıklarından kas zayıflığına, beyin fonksiyon bozukluklarına ve kanserlere kadar insan hastalıklarına yol açtğu düşünüldüğünde, hangi hedefleri nasıl paylaştıklarını ve ayarladıklarını anlamak, bir enzimin kaybının neden bazen beklenenden daha hafif etkiler yarattığını veya hücrelerin stres altında nasıl telafi yaptığını aydınlatabilir. Bu çalışma küçük RNA’larda psiuridinin nerelerde göründüğüne dair ayrıntılı bir harita sağlıyor ve bu işaretleri yazan enzimlerin birbirlerinin aktivitelerini modüle edebildiğini göstererek RNA temelli hataları incelemek ve nihayetinde düzeltmek için yeni giriş noktaları sunuyor.
Atıf: Liu, W., Ma, Y., Wang, L. et al. Quantitative analysis of small RNA pseudouridylation reveals interplay of PUS enzymes in tRNA anticodon stem-loop. Nat Commun 17, 2811 (2026). https://doi.org/10.1038/s41467-026-69177-7
Anahtar kelimeler: tRNA değişiklikleri, psiuridin, RNA enzimleri, mitokondriyal işlev, çeviri düzenlemesi