Clear Sky Science · it
Analisi quantitativa della pseudouridinazione dei piccoli RNA rivela l’interazione degli enzimi PUS nell’ansa anticodone del tRNA
Perché le marche nascoste sull’RNA sono importanti
Ogni cellula legge costantemente le istruzioni genetiche usando piccoli RNA che aiutano a costruire proteine e a processare altri RNA. Questo studio esamina una sottile modifica chimica su questi RNA, chiamata pseudouridina, che può cambiare il loro comportamento senza alterare il codice genetico sottostante. Mappando con precisione dove avvengono queste modifiche e quali enzimi le introducono, gli autori rivelano una inaspettata “conversazione” tra enzimi che affina una parte cruciale della macchina di sintesi proteica.
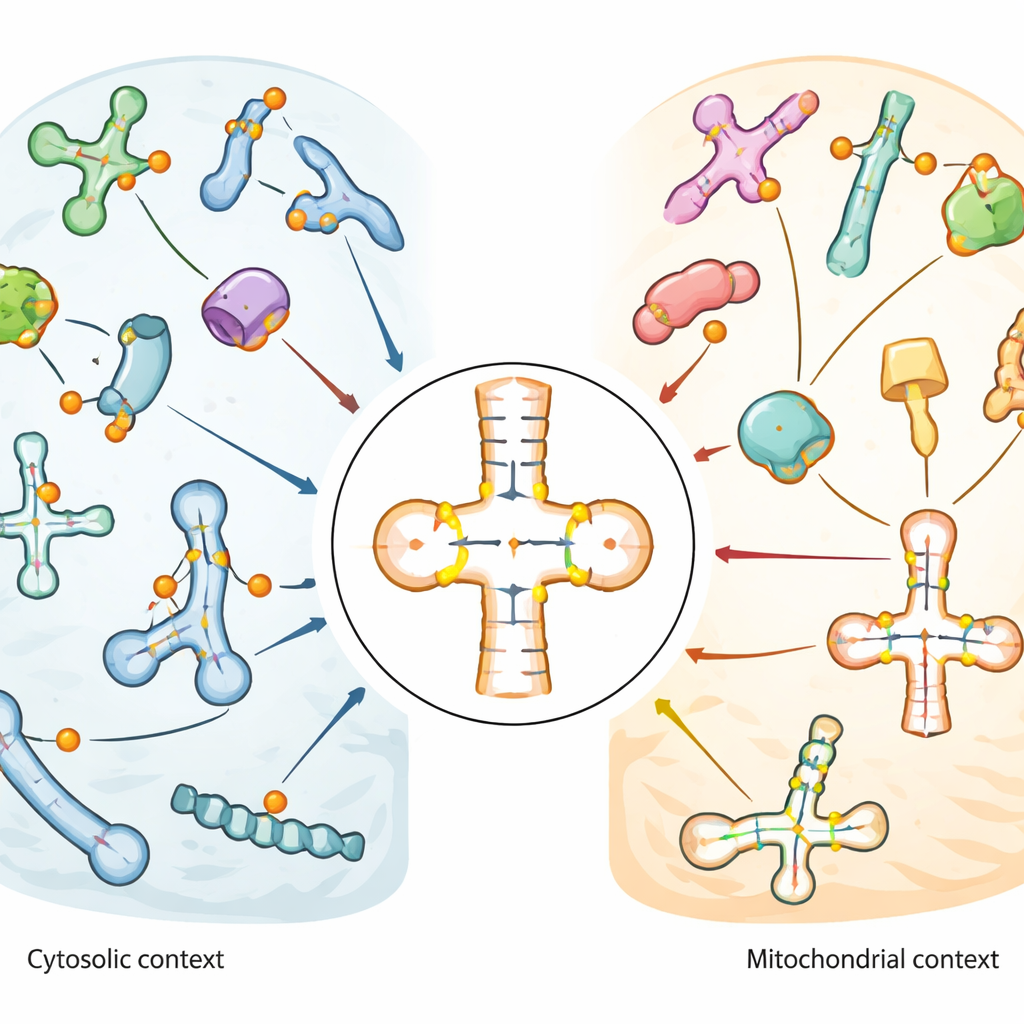
Modifiche chimiche sugli RNA operativi della cellula
Le cellule si avvalgono di molti tipi di piccoli RNA, in particolare i transfer RNA (tRNA), che fungono da adattatori leggendo le triplette del codice genetico e portando il corretto amminoacido durante la sintesi proteica. Questi tRNA, insieme ad altri piccoli RNA che guidano il processamento di RNA, sono densamente decorati da modifiche chimiche. La pseudouridina è una delle più comuni. Si differenzia dall’uridina ordinaria solo nel modo in cui gli atomi sono connessi, ma quel piccolo cambiamento rinforza l’appaiamento delle basi e può alterare forma e stabilità dell’RNA. Poiché la pseudouridina è collegata alle risposte allo stress, alla funzione cerebrale e al cancro, gli scienziati vogliono sapere esattamente dove compare e quali enzimi, detti pseudouridina sintetasi o enzimi PUS, ne sono responsabili.
Costruire una mappa precisa della pseudouridina
I metodi tradizionali potevano segnalare molti siti di pseudouridina ma faticavano a misurare quanto ciascun sito fosse modificato. I ricercatori hanno perfezionato un metodo chimico‑di sequenziamento più recente che avevano sviluppato in precedenza, chiamato PRAISE, per applicarlo quantitativamente ai piccoli RNA. Hanno prima trattato gli RNA per rimuovere altre modifiche che ostacolano l’analisi, quindi usato una reazione bisolfito specializzata e una strategia di sequenziamento che converte la presenza di pseudouridina in un segnale caratteristico di delezione nell’esito della lettura. Applicando questo approccio a cellule umane HEK293T, hanno generato un panorama ad alta risoluzione della pseudouridina nei tRNA citosolici e mitocondriali, così come negli snRNA e snoRNA. Il metodo si è dimostrato altamente riproducibile e ha eguagliato o superato le tecniche esistenti, aggiungendo misure precise dei livelli di modifica in ogni posizione.
Pattern distinti in diversi quartieri cellulari
La mappa ha rivelato che la pseudouridina è particolarmente arricchita nell’ansa anticodone dei tRNA, la regione che si appaia direttamente con l’mRNA durante la traduzione. Alcune posizioni, come un sito universalmente presente vicino alla base del tRNA (conosciuto come posizione 55), risultavano quasi completamente modificate in molti tRNA. Altre mostravano livelli moderati o variabili, suggerendo flessibilità regolatoria. I tRNA mitocondriali, che operano all’interno degli organelli produttrici di energia, mostravano un modello marcatamente diverso: siti chiave comuni nei tRNA citosolici erano assenti o debolmente modificati, mentre altre posizioni vicino all’anticodone erano fortemente e costantemente marcate. Questo contrasto implica che i mitocondri usino un insieme distinto di regole di editing per i propri tRNA. In snRNA e snoRNA, la pseudouridina si concentrava in regioni funzionali che aiutano a guidare altre modifiche dell’RNA o lo splicing, e alcuni siti cambiavano in risposta a shock termico o stress ossidativo.
Chi scrive le marche: assegnare enzimi ai siti
Per collegare enzimi specifici a siti specifici, il gruppo ha confrontato cellule di tipo selvatico con una serie di linee cellulari prive di singoli enzimi PUS o con livelli ridotti di un enzima guida chiamato DKC1. Hanno mostrato che le marche nei snoRNA derivano da due vie: una via guidata dall’RNA che usa DKC1 e un enzima autonomo, PUS7, che scrive un singolo sito distintivo. Nei tRNA hanno assegnato sistematicamente molti siti a enzimi particolari. PUS1 è emerso come uno scrittore principale di modifiche vicino all’anticodone sia nei tRNA citosolici sia in quelli mitocondriali. I membri della famiglia RluA hanno diviso i loro compiti: RPUSD1 modificava certi siti nei tRNA citosolici, includendo un sito precedentemente non riconosciuto vicino alla coda del tRNA, mentre RPUSD2 mirava a posizioni vicine nei tRNA mitocondriali, e RPUSD3 non ha mostrato attività osservabile sui tRNA. Enzimi correlati, PUS1L e PUS7L, si sono rivelati specializzarsi in regioni o tipi di tRNA distinti, indicando che proteine strettamente correlate possono evolvere compiti sorprendentemente diversi.
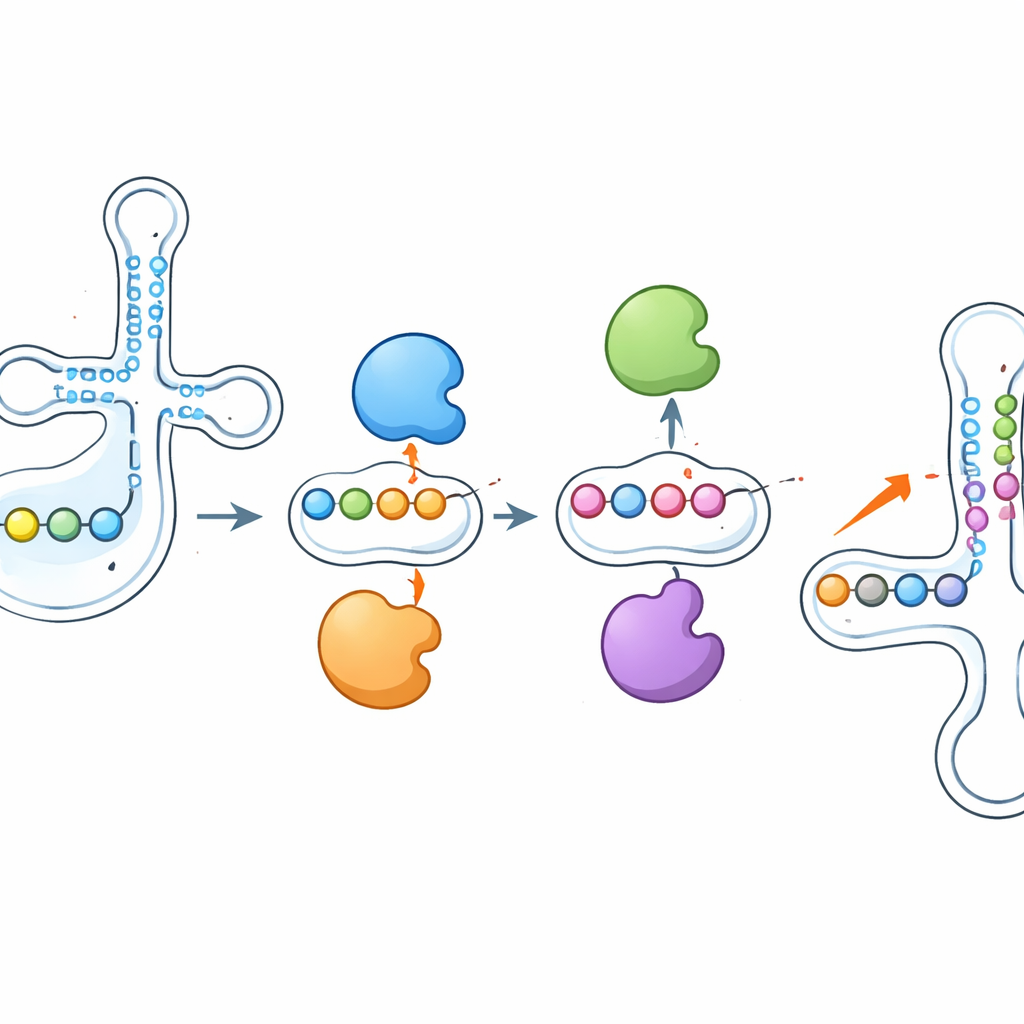
Enzimi che si spingono e si contrastano a vicenda
Una delle scoperte più sorprendenti è che questi enzimi non agiscono in isolamento. Quando i ricercatori hanno eliminato PUS1, le marche di pseudouridina che normalmente installa vicino all’anticodone sono diminuite drasticamente—ma siti vicini, modificati da altri enzimi come RPUSD1 o PUS7, sono diventati più intensamente modificati sullo stesso tRNA. L’eliminazione di RPUSD1 ha prodotto l’immagine speculare nelle posizioni sovrapposte, e schemi a bilanciere simili sono apparsi tra PUS7 e un altro enzima, PUS3. Questi cambiamenti non si spiegavano con variazioni nell’abbondanza degli enzimi o dei tRNA, indicando un’interazione diretta a livello delle singole molecole di tRNA. Gli autori suggeriscono che gli enzimi possano competere fisicamente per siti di legame vicini o che l’aggiunta o la rimozione di una pseudouridina rimodelli la struttura locale dell’RNA, rendendo le posizioni adiacenti più o meno accessibili ad altri enzimi.
Cosa significa per salute e malattia
Per un non specialista, il messaggio chiave è che le marche chimiche sui tRNA non sono decorazioni fisse ma fanno parte di un sistema dinamico e interconnesso. Molti enzimi collaborano e competono per creare il pattern nell’area anticodone, centrale per leggere il codice genetico in modo accurato e flessibile. Poiché mutazioni in diversi di questi enzimi causano malattie umane—da disordini del sangue e debolezza muscolare a disfunzioni cerebrali e cancro—capire come condividono e regolano i loro bersagli può chiarire perché la perdita di un enzima talvolta ha effetti meno gravi del previsto, o come le cellule compensano sotto stress. Questo studio fornisce una mappa dettagliata di dove compare la pseudouridina nei piccoli RNA e mostra che gli enzimi che scrivono queste marche possono modulare l’attività reciproca, offrendo nuovi punti di accesso per esplorare e, in futuro, correggere difetti dell’RNA rilevanti per la salute umana.
Citazione: Liu, W., Ma, Y., Wang, L. et al. Quantitative analysis of small RNA pseudouridylation reveals interplay of PUS enzymes in tRNA anticodon stem-loop. Nat Commun 17, 2811 (2026). https://doi.org/10.1038/s41467-026-69177-7
Parole chiave: modifiche del tRNA, pseudouridina, enzimi dell’RNA, funzione mitocondriale, regolazione della traduzione