Clear Sky Science · ru
Количественный анализ псевдоуридилирования малых РНК выявляет взаимодействие ферментов PUS в антикодонной петле тРНК
Почему скрытые метки на РНК важны
Каждая клетка постоянно считывает генетические инструкции с помощью малых РНК, которые помогают собирать белки и обрабатывать другие РНК. В этом исследовании рассматривается тонкая химическая правка на этих РНК, называемая псевдоуридином, которая может изменить их поведение, не меняя при этом сам код ДНК. Проследив точно, где появляются эти правки и какие ферменты их ставят, авторы показывают неожиданную «переписку» между ферментами, которая тонко настраивает ключевую часть аппарата синтеза белка.
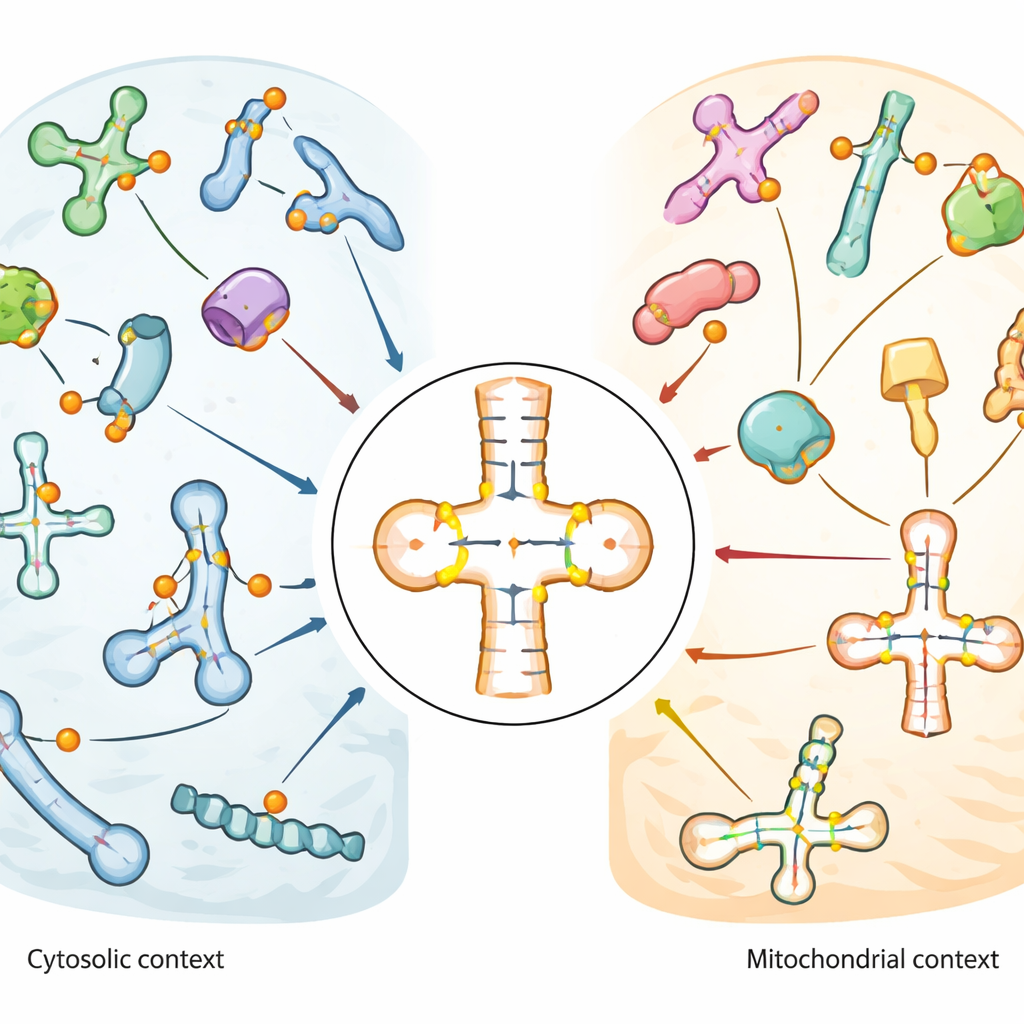
Химические правки на рабочих РНК клетки
Клетки полагаются на многие типы малых РНК, особенно на транспортные РНК (тРНК), которые действуют как адаптеры: читают трехбуквенные слова генетического кода и доставляют соответствующую аминокислоту во время синтеза белка. Эти тРНК, а также другие малые РНК, участвующие в обработке РНК, богато украшены химическими модификациями. Псевдоуридин — одна из самых распространённых. Он отличается от обычного уридина только связями между атомами, но это небольшое изменение укрепляет комплементарное спаривание и может изменить структуру и стабильность РНК. Поскольку псевдоуридин связан с ответом на стресс, функцией мозга и раком, учёные стремятся узнать, где именно он появляется и какие ферменты, называемые псевдоуридинсинтетазами или PUS, за это отвечают.
Построение точной карты псевдоуридина
Традиционные методы могли обнаруживать многие позиции с псевдоуридином, но им было трудно измерить, насколько широко каждая позиция модифицирована. Исследователи усовершенствовали более новый химико‑секвенирующий метод, который они ранее разработали — PRAISE — чтобы выполнять количественный анализ малых РНК. Сначала они обрабатывали РНК для удаления других мешающих модификаций, затем применяли специализированную бисульфитную реакцию и стратегию секвенирования, которая превращает наличие псевдоуридина в характерный сигнал делеции в результатах чтения. Применив это к человеческим клеткам HEK293T, они получили детализированную карту псевдоуридина в цитозольных и митохондриальных тРНК, а также в малых ядерных РНК (snRNA) и малых нуклеолярных РНК (snoRNA). Метод показал высокую воспроизводимость и сравнимые или лучшие характеристики по сравнению с существующими подходами, при этом добавив точные измерения уровня модификации на каждой позиции.
Различные паттерны в разных клеточных округах
Карта показала, что псевдоуридин особенно обогащён в антикодонной петле тРНК — области, которая напрямую спаривается с мРНК во время трансляции. Некоторые позиции, например универсально присутствующая позиция около основания тРНК (известная как позиция 55), были почти полностью модифицированы во многих тРНК. Другие демонстрировали умеренные или переменные уровни, что указывает на регуляторную гибкость. Митохондриальные тРНК, работающие внутри энергетических органелл клетки, показали заметно иной рисунок: ключевые сайты, общие для обычных (цитозольных) тРНК, отсутствовали или были слабо модифицированы, тогда как другие позиции около антикодона были сильно и стабильно отмечены. Это контрастное распределение подразумевает, что митохондрии используют собственные правила редакции для своих тРНК. В snRNA и snoRNA псевдоуридин группировался в функциональных областях, которые помогают направлять другие модификации РНК или сплайсинг, а некоторые сайты менялись в ответ на тепловой шок или окислительный стресс.
Кто ставит метки: сопоставление ферментов с сайтами
Чтобы связать конкретные ферменты с конкретными сайтами РНК, команда сравнила дикого типа клетки с панелью клеточных линий, лишённых отдельных ферментов PUS или с пониженным уровнем направляющего фермента DKC1. Они показали, что метки в snoRNA возникают двумя путями: РНК‑направляемым механизмом с участием DKC1 и автономной синтетазой PUS7, которая ставит одну характерную метку. В тРНК они систематически отнесли многие позиции к конкретным ферментам. PUS1 оказался основным «писцом» меток около антикодона как в цитозольных, так и в митохондриальных тРНК. Члены семейства RluA разделили обязанности: RPUSD1 модифицировал определённые сайты в цитозольных тРНК, включая ранее не распознанную позицию около хвоста тРНК, тогда как RPUSD2 нацеливался на близкие позиции в митохондриальных тРНК, а RPUSD3 не показал обнаруживаемой активности по тРНК. Родственные ферменты PUS1L и PUS7L оказались специализированы на разных регионах или типах тРНК, что указывает на то, что близкородственные белки могут эволюционно приобретать удивительно разные функции.
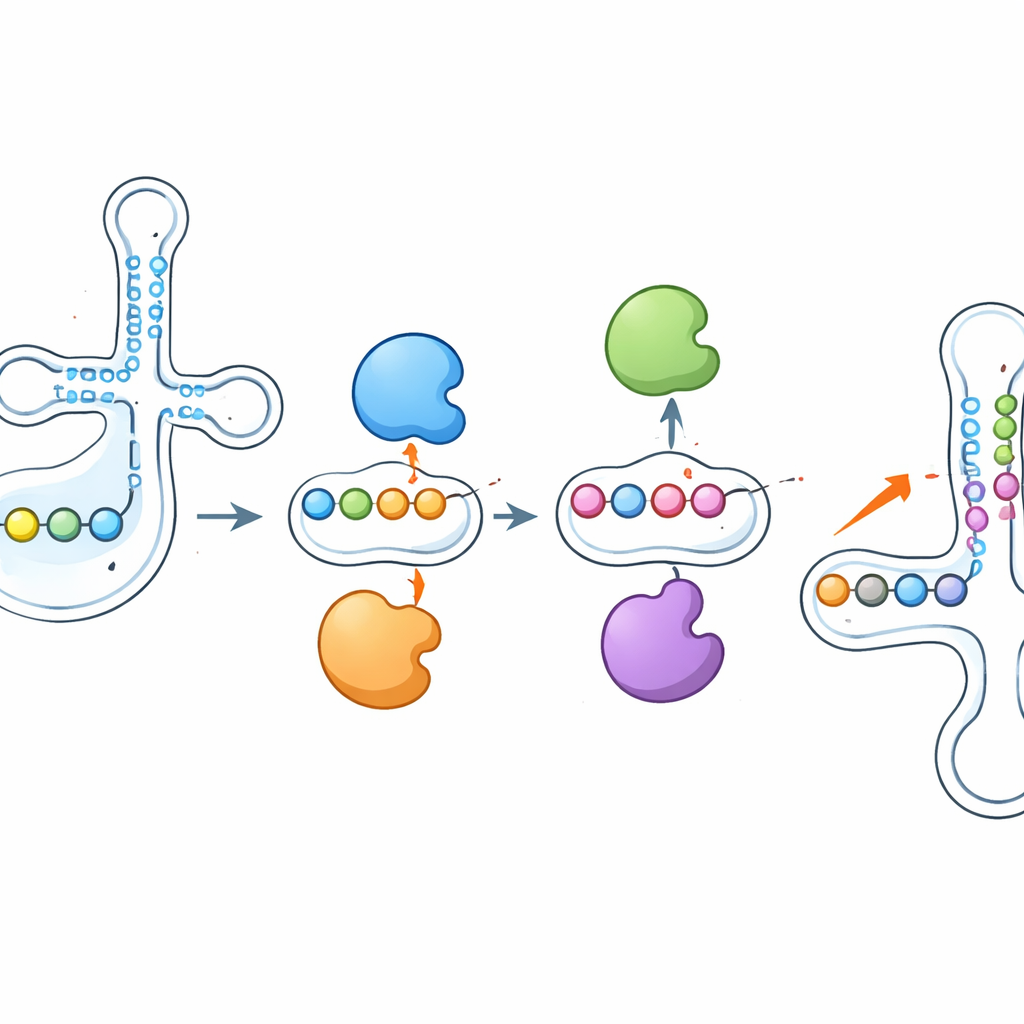
Ферменты, которые влияют друг на друга
Одно из наиболее впечатляющих наблюдений — то, что эти ферменты не действуют в изоляции. Когда исследователи удали PUS1, псевдоуридиновые метки, которые он обычно устанавливает около антикодона, резко уменьшились — но соседние позиции, модифицируемые другими ферментами, такими как RPUSD1 или PUS7, стали более интенсивно модифицированы в той же тРНК. Удаление RPUSD1 давало зеркальный эффект в перекрывающихся позициях, и похожие качели наблюдались между PUS7 и другим ферментом PUS3. Эти изменения нельзя было объяснить сдвигами в уровне ферментов или абундантности тРНК, что указывает на прямое взаимодействие на уровне отдельных молекул тРНК. Авторы предполагают, что ферменты могут физически конкурировать за близлежащие сайты связывания или что добавление или удаление псевдоуридина перестраивает локальную структуру РНК, делая соседние позиции более или менее доступными для других ферментов.
Что это значит для здоровья и болезней
Для неспециалиста основное послание таково: химические метки на тРНК — это не статичные украшения, а часть динамичной, взаимосвязанной системы. Несколько ферментов сотрудничают и конкурируют, формируя рисунок в антикодонной области, которая имеет ключевое значение для точного и гибкого считывания генетического кода. Поскольку мутации в нескольких из этих ферментов вызывают человеческие заболевания — от нарушений крови и мышечной слабости до нарушений работы мозга и рака — понимание того, как они делят и корректируют свои цели, может прояснить, почему потеря одного фермента иногда даёт менее тяжёлые последствия, чем ожидалось, или как клетки компенсируют стресс. Это исследование предоставляет подробную карту расположения псевдоуридина в малых РНК и показывает, что ферменты, создающие эти метки, могут модулировать активность друг друга, открывая новые пути для изучения и, в перспективе, корректировки нарушений, связанных с РНК, в человеческом здоровье.
Цитирование: Liu, W., Ma, Y., Wang, L. et al. Quantitative analysis of small RNA pseudouridylation reveals interplay of PUS enzymes in tRNA anticodon stem-loop. Nat Commun 17, 2811 (2026). https://doi.org/10.1038/s41467-026-69177-7
Ключевые слова: модификации тРНК, псевдоуридин, ферменты РНК, митохондриальная функция, регуляция трансляции