Clear Sky Science · sv
Kvantiativ analys av pseudouridinering i små RNA avslöjar samspel mellan PUS-enzym i tRNA:s antikodstam-öga
Varför dolda märken på RNA spelar roll
Varje cell läser ständigt genetiska instruktioner med hjälp av små RNA-molekyler som hjälper till att bygga proteiner och bearbeta andra RNA. Denna studie undersöker en subtil kemisk ändring på dessa RNA, kallad pseudouridin, som kan förändra deras beteende utan att ändra den underliggande genetiska koden. Genom att kartlägga exakt var dessa modifieringar förekommer och vilka enzymer som sätter dem visar författarna upp en oväntad "konversation" bland enzymer som finjusterar en avgörande del av maskineriet för proteinsyntes.
Kemiska redigeringar på cellens arbets-RNA
Celler förlitar sig på många typer av små RNA, särskilt transfer-RNA (tRNA), som fungerar som adaptrar som läser trebokstavsord i den genetiska koden och levererar rätt aminosyra under proteinsyntesen. Dessa tRNA, tillsammans med andra små RNA som styr RNA-bearbetning, är tätt dekorerade med kemiska modifieringar. Pseudouridin är en av de vanligaste. Det skiljer sig från vanlig uridin bara i hur dess atomer är bundna, men den lilla skillnaden stärker basparning och kan förändra RNA:s form och stabilitet. Eftersom pseudouridin kopplats till stressrespons, hjärnfunktion och cancer vill forskare veta exakt var det förekommer och vilka enzymer — kallade pseudouridinsyntaser eller PUS-enzym — som är ansvariga.
Att bygga en precis karta över pseudouridin
Traditionella metoder kunde identifiera många pseudouridinställen men hade svårt att kvantifiera hur omfattande varje plats var modifierad. Forskarna förbättrade en nyare kemisk sekvenseringsmetod de tidigare utvecklat, kallad PRAISE, för att göra detta kvantitativt på små RNA. De behandlade först RNA för att ta bort andra blockerande modifieringar, och använde sedan en specialiserad bisulfitreaktion och sekvenseringsstrategi som omvandlar närvaron av pseudouridin till en karakteristisk deletionssignal i avläsningen. Genom att tillämpa detta på humana HEK293T-celler skapade de ett högupplöst landskap av pseudouridin över cytosoliska och mitokondriella tRNA samt små nukleära RNA (snRNA) och små nukleolära RNA (snoRNA). Metoden visade sig vara mycket reproducerbar och matchade eller överträffade befintliga tekniker, samtidigt som den lade till precisa mått på modifieringsnivåer i varje position.
Skilda mönster i olika cellulära miljöer
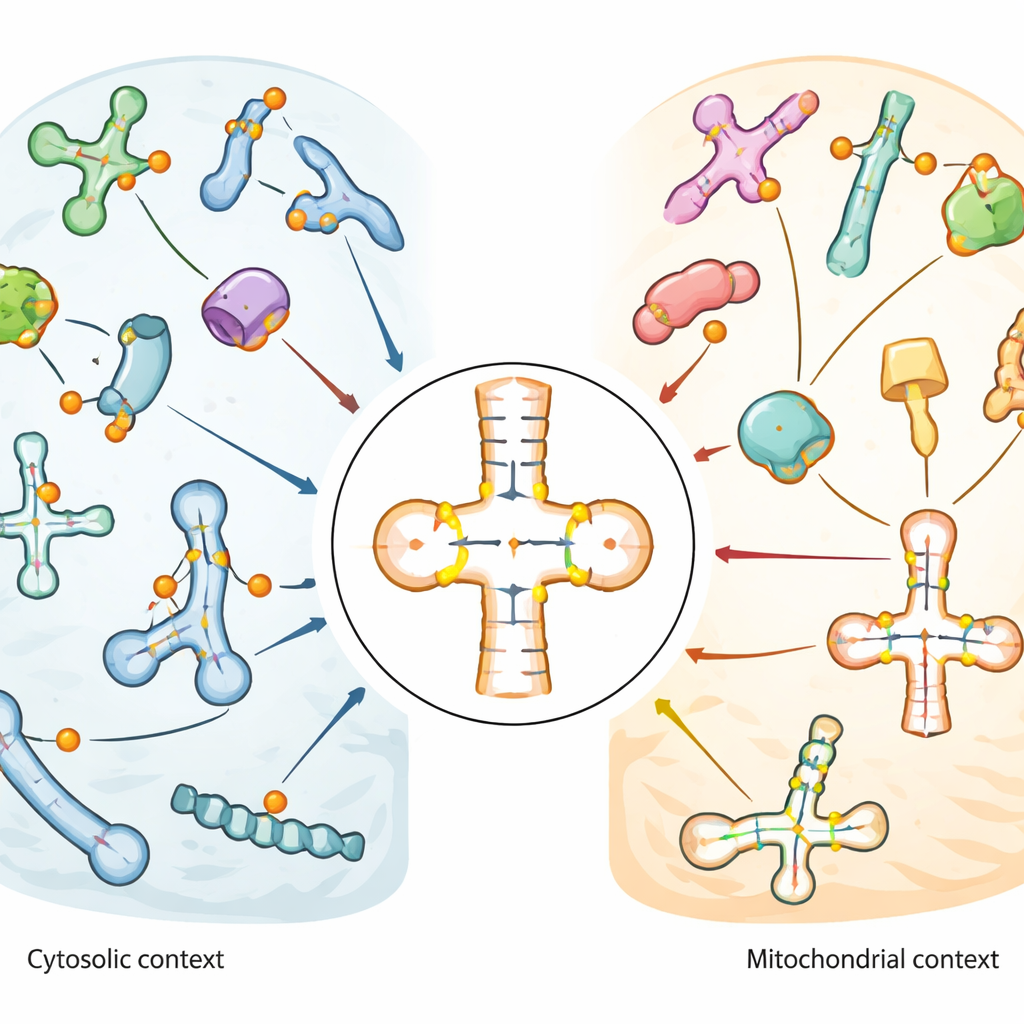
Kartan avslöjade att pseudouridin är särskilt rikt förekommande i antikod-stam-ögat hos tRNA, den region som direkt parar med budbärar-RNA under translation. Vissa positioner, som en universellt närvarande plats nära tRNA:s bas (känd som position 55), var nästan fullständigt modifierade i många tRNA. Andra visade måttliga eller varierande nivåer, vilket antyder regulatorisk flexibilitet. Mitokondriella tRNA, som verkar inne i cellens energiproducerande organeller, visade ett markant annorlunda mönster: nyckelställena som är vanliga i vanliga (cytosoliska) tRNA saknades eller var svagt modifierade, medan andra positioner nära antikoden var starkt och konsekvent märkta. Denna kontrast tyder på att mitokondrier använder ett eget uppsättning redigeringsregler för sina tRNA. I snRNA och snoRNA klustrade pseudouridin i funktionella regioner som hjälper till att styra andra RNA-modifikationer eller splitsning, och vissa platser förändrades vid värmechock eller oxidativ stress.
Vem skriver märkena: att koppla enzymer till platser
För att koppla specifika enzymer till specifika RNA-platser jämförde teamet vildtypceller med en panel cellinjer som saknade individuella PUS-enzym eller med reducerade nivåer av ett guideenzym kallat DKC1. De visade att snoRNA-märken kommer från två vägar: en RNA-ledd väg med DKC1 och ett fristående enzym PUS7 som skriver en enda distinkt plats. I tRNA tilldelade de systematiskt många platser till särskilda enzymer. PUS1 framträdde som en huvudskrivare av märken nära antikoden i både cytosoliska och mitokondriella tRNA. Medlemmar av RluA-familjen delade upp sina uppgifter: RPUSD1 modifierade vissa platser i cytosoliska tRNA, inklusive en tidigare oidentifierad plats nära tRNA-änden, medan RPUSD2 riktade sig mot närliggande positioner i mitokondriella tRNA, och RPUSD3 uppvisade ingen påtaglig tRNA-aktivitet. Besläktade enzymer PUS1L och PUS7L visade sig specialisera sig på olika regioner eller tRNA-typer, vilket indikerar att nära besläktade proteiner kan utveckla förvånansvärt olika uppgifter.
Enzymer som påverkar varandras arbete
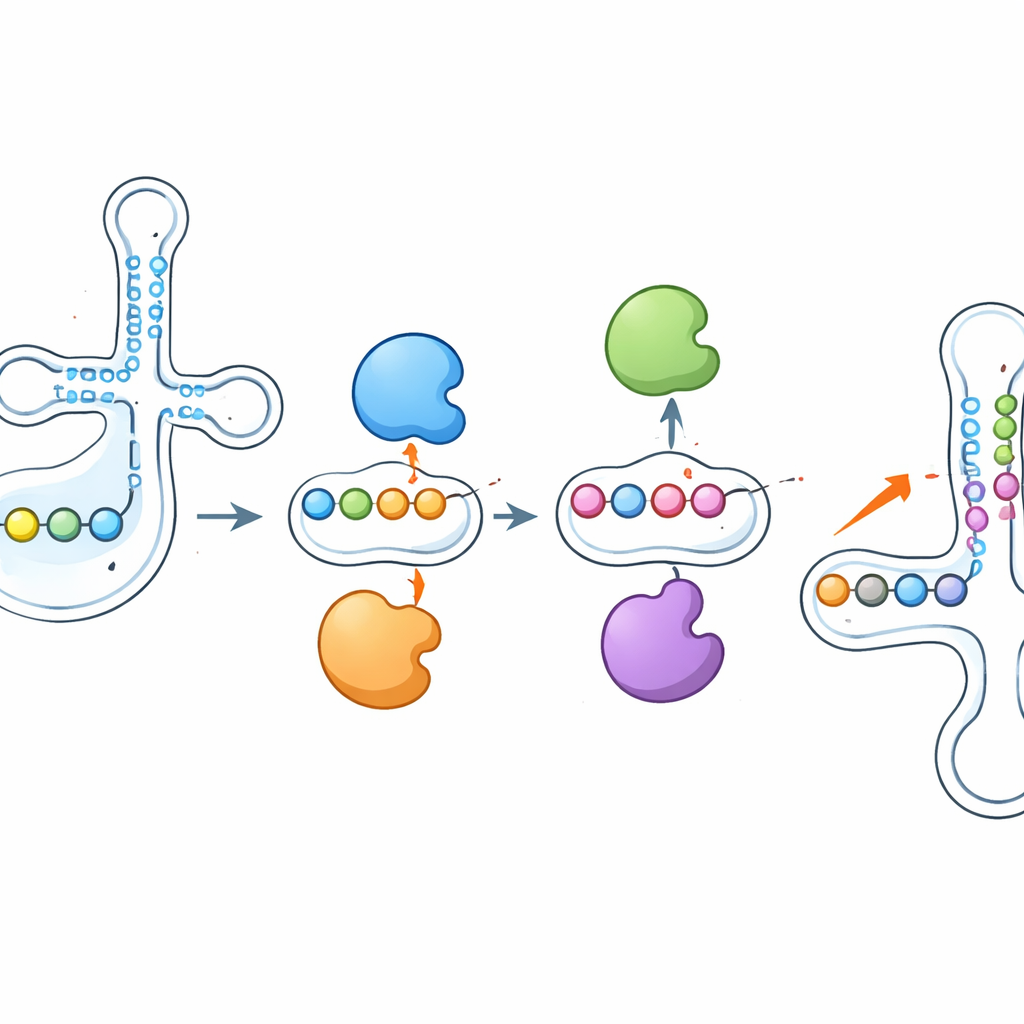
En av de mest iögonfallande upptäckterna var att dessa enzymer inte verkar isolerat. När forskarna tog bort PUS1 sjönk pseudouridinmärkena som det normalt installerar nära antikoden kraftigt — men närliggande platser, skrivna av andra enzymer som RPUSD1 eller PUS7, blev mer kraftigt modifierade på samma tRNA. Att slå ut RPUSD1 gav den spegelvända bilden vid överlappande positioner, och liknande gungbrädemönster uppträdde mellan PUS7 och ett annat enzym, PUS3. Dessa förändringar förklarades inte av skift i enzym- eller tRNA-abundans, vilket pekar på ett direkt samspel på nivån av individuella tRNA-molekyler. Författarna föreslår att enzymer kan konkurrera fysiskt om närliggande bindningsställen eller att tillförsel eller borttagning av en pseudouridin omformar lokal RNA-struktur och gör intilliggande positioner mer eller mindre åtkomliga för andra enzymer.
Vad detta betyder för hälsa och sjukdom
För en icke-specialist är huvudbudskapet att de kemiska märkena på tRNA inte är fasta dekorationer utan en del av ett dynamiskt, sammankopplat system. Flera enzymer samarbetar och konkurrerar för att forma antikodregionen, som är central för att läsa den genetiska koden korrekt och flexibelt. Eftersom mutationer i flera av dessa enzymer orsakar mänsklig sjukdom — från blodstörningar och muskelsvaghet till hjärndysfunktion och cancer — kan förståelsen för hur de delar och justerar sina mål kasta ljus över varför förlust av ett enzym ibland har mildare effekter än väntat, eller hur celler kompenserar under stress. Denna studie ger en detaljerad karta över var pseudouridin förekommer på små RNA och visar att enzymerna som skriver dessa märken kan modulera varandras aktivitet, vilket öppnar nya ingångspunkter för att utforska och så småningom korrigera RNA-baserade defekter i människors hälsa.
Citering: Liu, W., Ma, Y., Wang, L. et al. Quantitative analysis of small RNA pseudouridylation reveals interplay of PUS enzymes in tRNA anticodon stem-loop. Nat Commun 17, 2811 (2026). https://doi.org/10.1038/s41467-026-69177-7
Nyckelord: tRNA-modifikationer, pseudouridin, RNA-enzym, mitokondriell funktion, reglering av translation