Clear Sky Science · pl
Analiza ilościowa pseudourydylacji małych RNA ujawnia współdziałanie enzymów PUS w pętli antykodonowej tRNA
Dlaczego ukryte znaki na RNA mają znaczenie
Każda komórka nieustannie odczytuje instrukcje genetyczne przy pomocy małych cząsteczek RNA, które pomagają budować białka i przetwarzać inne RNA. W tym badaniu przyjrzano się subtelnej chemicznej modyfikacji tych RNA, zwanej pseudourydyną, która może zmieniać ich zachowanie bez naruszania kodu genetycznego. Mapując precyzyjnie miejsca tych modyfikacji i ustalając, które enzymy je wprowadzają, autorzy ujawniają nieoczekiwaną „rozmowę” pomiędzy enzymami, która dopracowuje kluczowy element aparatu translacyjnego.
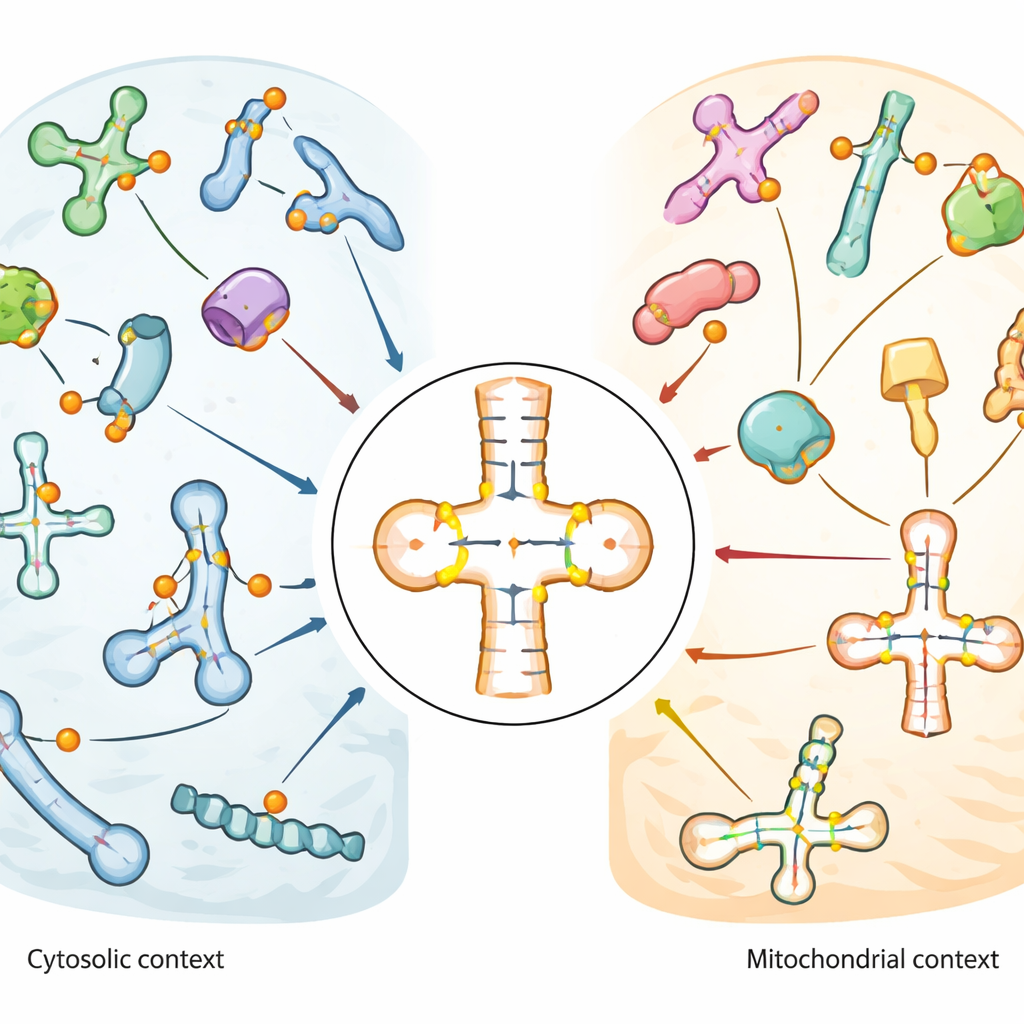
Chemiczne poprawki na RNA pełniących główną rolę w komórce
Komórki polegają na różnych małych RNA, zwłaszcza na transferowych RNA (tRNA), które działają jak adaptery — odczytują trójliterowe słowa w kodzie genetycznym i dostarczają odpowiedni aminokwas podczas syntezy białka. Te tRNA, podobnie jak inne małe RNA biorące udział w obróbce RNA, są gęsto ozdobione modyfikacjami chemicznymi. Pseudourydyna jest jedną z najczęstszych. Różni się od zwykłej urydyny jedynie sposobem połączenia atomów, ale ta drobna zmiana wzmacnia parowanie zasad i może zmieniać kształt oraz stabilność RNA. Ponieważ pseudourydyna wiązana jest z reakcjami na stres, funkcjonowaniem mózgu i rakiem, naukowcy chcą wiedzieć dokładnie, gdzie się pojawia i które enzymy, zwane syntazami pseudourydylowymi (enzymy PUS), za to odpowiadają.
Budowanie precyzyjnej mapy pseudourydyny
Tradycyjne metody potrafiły wykryć wiele miejsc pseudourydylacji, lecz miały trudności z określeniem, w jakim stopniu każde z nich jest zmodyfikowane. Badacze udoskonalili nowszą metodę chemiczno-sekwencyjną, którą wcześniej opracowali, nazwaną PRAISE, aby wykonać ilościowe oznaczenia na małych RNA. Najpierw potraktowali RNA, aby usunąć inne blokujące modyfikacje, a następnie zastosowali specjalną reakcję bisulfitem i strategię sekwencjonowania, która przemienia obecność pseudourydyny w charakterystyczny sygnał delecji w odczycie. Stosując tę metodę do ludzkich komórek HEK293T, uzyskali wysokorozdzielczą mapę pseudourydyny w tRNA cytoplazmatycznych i mitochondrialnych oraz w małych RNA jądrowych (snRNA) i nukleolarnych (snoRNA). Metoda okazała się wysoce odtwarzalna i dorównywała lub przewyższała istniejące techniki, a dodatkowo dostarczała precyzyjnych pomiarów poziomów modyfikacji na każdej pozycji.
Odwarte wzorce w różnych „sąsiedztwach” komórkowych
Mapa wykazała, że pseudourydyna jest szczególnie wzbogacona w pętli antykodonowej tRNA, obszarze, który bezpośrednio paruje się z mRNA podczas translacji. Niektóre pozycje, jak powszechnie występujące miejsce w pobliżu trzonu tRNA (znane jako pozycja 55), były niemal całkowicie zmodyfikowane w wielu tRNA. Inne wykazywały umiarkowane lub zmienne poziomy, co sugeruje elastyczność regulacyjną. Mitochondrialne tRNA, działające wewnątrz organelli wytwarzających energię, miały wyraźnie inny wzorzec: kluczowe miejsca spotykane w tRNA cytoplazmatycznych były nieobecne lub słabo zmodyfikowane, podczas gdy inne pozycje w pobliżu antykodonu były silnie i konsekwentnie oznaczone. Ten kontrast sugeruje, że mitochondria stosują odrębne zasady edycji dla swoich tRNA. W snRNA i snoRNA pseudourydyna skupiała się w regionach funkcyjnych, które pomagają kierować inne modyfikacje RNA lub składanie (splicing), a niektóre miejsca zmieniały się w odpowiedzi na udar cieplny lub stres oksydacyjny.
Kto pisze znaki: przypisywanie enzymów do miejsc
Aby powiązać konkretne enzymy z określonymi miejscami RNA, zespół porównał komórki typu dzikiego z serią linii komórkowych pozbawionych poszczególnych enzymów PUS lub z obniżonym poziomem enzymu przewodnika DKC1. Pokazali, że modyfikacje snoRNA pochodzą z dwóch dróg: z drogi kierowanej przez RNA wykorzystującej DKC1 oraz z działania samodzielnego enzymu PUS7, który wprowadza jedną charakterystyczną modyfikację. W tRNA systematycznie przypisano wiele miejsc do konkretnych enzymów. PUS1 wyrósł na głównego „pisarza” modyfikacji w pobliżu antykodonu zarówno w tRNA cytoplazmatycznych, jak i mitochondrialnych. Członkowie rodziny RluA podzielili się zadaniami: RPUSD1 modyfikował określone miejsca w tRNA cytoplazmatycznych, w tym wcześniej nierozpoznane miejsce blisko ogona tRNA, podczas gdy RPUSD2 celował w pobliskie pozycje w tRNA mitochondrialnych, a RPUSD3 nie wykazywał wykrywalnej aktywności wobec tRNA. Powiązane enzymy PUS1L i PUS7L okazały się wyspecjalizowane w różnych regionach lub typach tRNA, co wskazuje, że blisko spokrewnione białka mogą ewoluować zaskakująco odrębne funkcje.
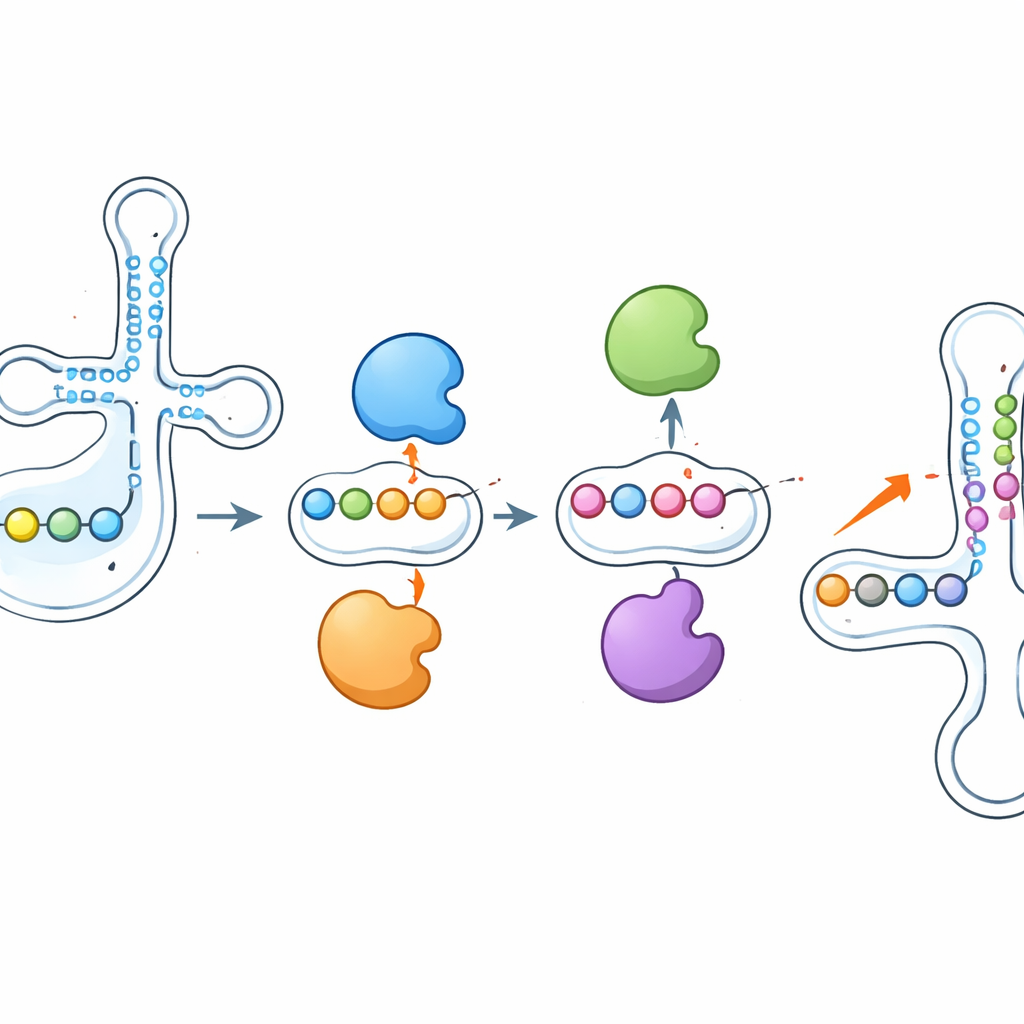
Enzymy, które wzajemnie wpływają na swoją pracę
Jednym z najbardziej uderzających odkryć było to, że te enzymy nie działają w izolacji. Gdy badacze usunęli PUS1, pseudourydynowe znaki, które normalnie instaluje w pobliżu antykodonu, gwałtownie zmalały — ale sąsiednie pozycje, zapisywane przez inne enzymy takie jak RPUSD1 lub PUS7, stały się silniej zmodyfikowane w tym samym tRNA. Wyłączenie RPUSD1 dało obraz lustrzany na nakładających się pozycjach, a podobne wzorce wahadłowe pojawiły się między PUS7 i innym enzymem, PUS3. Zmiany te nie wynikały ze zmian w obfitości enzymów czy tRNA, co wskazuje na bezpośrednie współdziałanie na poziomie pojedynczych cząsteczek tRNA. Autorzy sugerują, że enzymy mogą fizycznie konkurować o sąsiednie miejsca wiążące lub że dodanie bądź usunięcie pseudourydyny przekształca lokalną strukturę RNA, czyniąc pobliskie pozycje bardziej lub mniej dostępne dla innych enzymów.
Co to oznacza dla zdrowia i chorób
Dla osoby niezwiązanej z dziedziną istotnym przesłaniem jest to, że chemiczne znaki na tRNA nie są stałymi ozdobnikami, lecz częścią dynamicznego, powiązanego systemu. Wiele enzymów współpracuje i konkuruje, formując wzorzec w regionie antykodonowym, który jest kluczowy dla dokładnego i elastycznego odczytu kodu genetycznego. Ponieważ mutacje w kilku z tych enzymów powodują choroby u ludzi — od zaburzeń krwi i osłabienia mięśni po dysfunkcje mózgu i raka — zrozumienie, jak dzielą się i dostosowują swoje cele, może wyjaśnić, dlaczego utrata jednego enzymu czasem daje łagodniejsze skutki niż oczekiwano, lub jak komórki rekompensują to w stresie. To badanie dostarcza szczegółowej mapy miejsc występowania pseudourydyny na małych RNA i pokazuje, że enzymy je wprowadzające mogą wzajemnie modyfikować swoją aktywność, otwierając nowe możliwości badania i potencjalnej korekty defektów RNA w zdrowiu człowieka.
Cytowanie: Liu, W., Ma, Y., Wang, L. et al. Quantitative analysis of small RNA pseudouridylation reveals interplay of PUS enzymes in tRNA anticodon stem-loop. Nat Commun 17, 2811 (2026). https://doi.org/10.1038/s41467-026-69177-7
Słowa kluczowe: modyfikacje tRNA, pseudourydyna, enzymy RNA, funkcja mitochondrialna, regulacja translacji