Clear Sky Science · he
ניתוח כמותי של פסאודורידילציה ב‑RNA קטן חושף אינטראקציה בין אנזימי PUS בלולאת הגבעול‑נגד‑קודן של tRNA
מדוע סימנים נסתרים על RNA חשובים
כל תא קורא באופן שוטף הוראות גנטיות באמצעות מולקולות RNA קטנות שמסייעות לבניית חלבונים ולעיבוד RNA נוספים. המחקר בוחן תיקון כימי עדין על ה‑RNA הללו, שנקרא פסאודורידין, שיכול לשנות את התנהגותם בלי לשנות את הקוד הגנטי הבסיסי. על‑ידי מיפוי מדויק של מיקומי התיקונים ומי מהאנזימים מציבם, המחברים חושפים "שיחה" בלתי צפויה בין אנזימים שמדייקת חלק חיוני ממכונת יצירת החלבון.
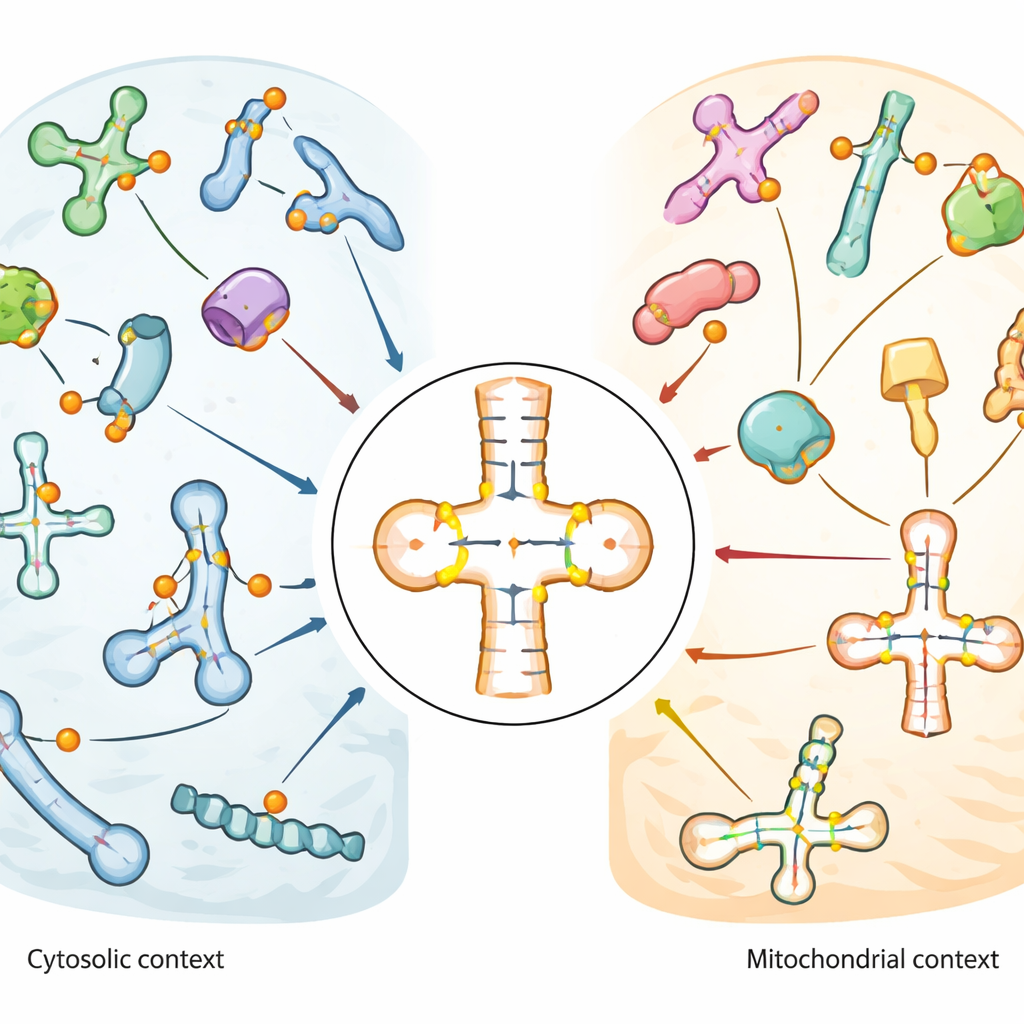
עריכות כימיות על RNA העובד של התא
תאים מסתמכים על סוגים רבים של RNA קטנים, במיוחד tRNA (RNA מעביר), ששירתים כממתגים שקוראים מילים תלת‑אותיות בקוד הגנטי ומספקים את חומצת האמינו הנכונה בזמן הסינתזה של חלבונים. ה‑tRNA האלה, יחד עם RNA קטנים אחרים שמנחים עיבוד RNA, מכוסים בצפיפות בשינויים כימיים. פסאודורידין הוא אחד הנפוצים שבהם. הוא שונה מאורידין רגיל רק באופן שבו האטומים שלו מחוברים, אך שינוי קטן זה מחזק הזיווג הבסיסי ויכול לשנות את צורת ויציבות ה‑RNA. מאחר שפסאודורידין מקושר לתגובות לחץ, לתפקוד המוח ולסרטן, המדענים מעוניינים לדעת בדיוק היכן הוא מופיע ואילו אנזימים, שנקראים פסאודורידין‑סינתאזות (PUS), אחראים עליו.
בניית מפת פסאודורידין מדויקת
שיטות מסורתיות יכלו לזהות אתרי פסאודורידין רבים אך התקשו למדוד עד כמה כל אתר מותאם. החוקרים שיפרו שיטת ריצוף כימית חדשה שפיתחו קודם, שנקראת PRAISE, כדי לבצע מדידה כמותית זו על RNA קטן. תחילה טיפלו ב‑RNA להסרת שינויים חוסמים אחרים, ואז השתמשו בתגובת ביסולפיט מיוחדת ובאסטרטגיית ריצוף שהופכת את נוכחות הפסאודורידין לאות אופייני של מחיקה בתוצאות הקריאה. יישום זה בתאי HEK293T של אדם יצר מפת רזולוציה‑גבוהה של פסאודורידין ב‑tRNA ציטוזוליים ומיטוכונדריאליים, וכן ב‑snRNA ו‑snoRNA. השיטה הוכחה כחסינת רעש מאוד והתאימה או עלתה על טכניקות קיימות, תוך הוספת מדידות מדויקות של רמות המודיפיקציה בכל מיקום.
תבניות מובחנות בשכונות תאיות שונות
המפה גילתה כי פסאודורידין מרוכז במיוחד בלולאת הגבעול‑נגד‑קודן של ה‑tRNA, האזור שמזדווג ישירות עם ה‑mRNA במהלך התרגום. מקומות מסוימים, כמו אתר שקיים אוניברסלית בסמוך לבסיס ה‑tRNA (מוכר כמיקום 55), היו כמעט מותאמים במלואם ברבים מה‑tRNA. אחרים הראו רמות בינוניות או משתנות, מה שמעיד על גמישות רגולטורית. ה‑tRNA המיטוכונדריאליים, הפועלים באברון המפיק אנרגיה של התא, הציגו דפוס שונה באופן בולט: אתרים מרכזיים הנפוצים ב‑tRNA הציטוזוליים נעדרו או הוסרגו חלש, בעוד שמיקומים אחרים בסמוך לנגד‑קודן היו מסומנים בעוצמה ובעקביות. הניגוד הזה מרמז שמיטוכונדריה משתמשת בכללי עריכה נפרדים ל‑tRNA שלה. ב‑snRNA וב‑snoRNA, פסאודורידין הצטבר באזורים פונקציונליים שעוזרים להנחות שינויים אחרים ב‑RNA או חיתוך (splicing), וחלק מהאתרים השתנו בתגובה להלם חום או לחץ חמצוני.
מי כותב את הסימנים: שיוך אנזימים לאתרים
כדי לקשר אנזימים ספציפיים לאתרים מסוימים ב‑RNA, הצוות השווה בין תאים מסוג בר‑בריא לבין סדרת תאי קו חסרי אנזימי PUS בודדים או עם רמות מופחתות של אנזים מדריך בשם DKC1. הם הראו שסימני snoRNA נוצרו משתי דרכים: מסלול מונחה RNA שמשתמש ב‑DKC1, ואנזים עצמאי PUS7 שכותב אתר אופייני יחיד. ב‑tRNA הם שיוכו באופן שיטתי אתרים רבים לאנזימים מסוימים. PUS1 עלה כבעל תפקיד מרכזי בכתיבת סימנים קרוב לנגד‑קודן הן ב‑tRNA ציטוזוליים והן במיטוכונדריאליים. חברי משפחת RluA חילקו ביניהם סמכויות: RPUSD1 שינה אתרים מסוימים ב‑tRNA ציטוזוליים, כולל אתר לא מזוהה קודם בסמוך לזנב ה‑tRNA, בעוד RPUSD2 כוון עמדות סמוכות ב‑tRNA מיטוכונדריאליים, ו‑RPUSD3 לא הראה פעילות tRNA זיהוית. אנזימים קרובים אחרים, PUS1L ו‑PUS7L, התגלו כממחים באזורים או בסוגי tRNA מובחנים, מה שמצביע על כך שחלבונים קרובים מבחינה אבולוציונית יכולים לפתח תפקידים שונים באופן מפתיע.
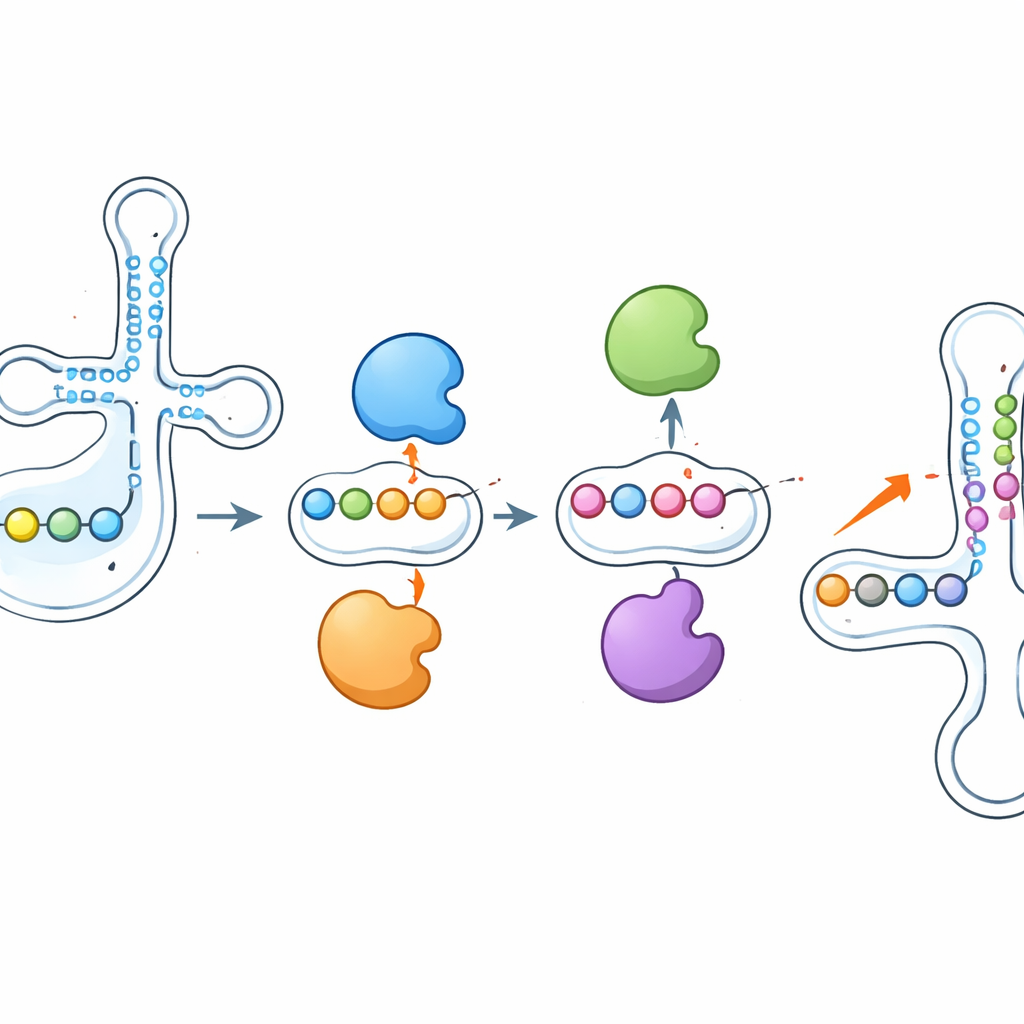
אנזימים שמתחרים ומשפיעים זה על זה
אחת הממצאים המרהיבים הייתה שהאנזימים האלה אינם פועלים בבידוד. כאשר החוקרים מחקו את PUS1, הסימנים של פסאודורידין שהוא בדרך כלל מתקין בסמוך לנגד‑קודן ירדו בעוצמה—אך אתרים שכנים, שנכתבו על‑ידי אנזימים אחרים כמו RPUSD1 או PUS7, הפכו להיות מותאמים בעוצמה רבה יותר על אותו tRNA. ניתוק RPUSD1 גרם לתמונה היפוכית במקומות חופפים, ודפוסי שעון‑נדנדה דומים הופיעו בין PUS7 לאנזים אחר, PUS3. שינויים אלה לא הוסברו על‑ידי שינויים בכמויות האנזים או ה‑tRNA, מה שמצביע על אינטראקציה ישירה ברמת מולקולות tRNA בודדות. המחברים מציעים שאנזימים עשויים להתחרות פיזית על אתרי קשירה סמוכים או שהוספה או הסרה של פסאודורידין מעצבת מחדש את המבנה המקומי של ה‑RNA, מה שהופך עמדות שכנות ליותר או פחות נגישות לאנזימים אחרים.
מתי זה חשוב לבריאות ולמחלה
ללא‑מומחה, המסר המרכזי הוא שהסימנים הכימיים על ה‑tRNA אינם קישוטים קבועים אלא חלק ממערכת דינמית ומחוברת. אנזימים מרובים משתפים פעולה ומתחרים כדי לתבנן את אזור הנגד‑קודן, שהוא מרכזי לקריאה מדויקת וגמישה של הקוד הגנטי. מאחר שמוטציות בכמה מהאנזימים הללו גורמות למחלות אנושיות—מבעיות דם והתעייפות שריר ועד תפקוד מוחי וקנֵסר—הבנת האופן שבו הם חולקים ומותאמים את היעדים שלהם עשויה להאיר מדוע איבוד של אנזים אחד לעיתים גורם להשפעות מתונות יותר מהצפוי, או כיצד תאים מפצים תחת לחץ. המחקר הזה מספק מפת פירוט של מיקומי פסאודורידין ב‑RNA קטן ומראה שהאנזימים הכותבים את הסימנים הללו יכולים לווסת זה את פעילותו של זה, מה שמציע נקודות כניסה חדשות לחקירה ובסופו של דבר לתיקון ליקויים מבוססי‑RNA בבריאות האדם.
ציטוט: Liu, W., Ma, Y., Wang, L. et al. Quantitative analysis of small RNA pseudouridylation reveals interplay of PUS enzymes in tRNA anticodon stem-loop. Nat Commun 17, 2811 (2026). https://doi.org/10.1038/s41467-026-69177-7
מילות מפתח: שינויים ב‑tRNA, פסאודורידין, אנזימי RNA, תפקוד מיטוכונדריאלי, ויסות תרגום