Clear Sky Science · es
Análisis cuantitativo de la pseudouridilación en ARN pequeños revela la interacción entre enzimas PUS en el bucle anticodeón del ARNt
Por qué importan las marcas ocultas en el ARN
Cada célula lee constantemente las instrucciones genéticas mediante moléculas pequeñas de ARN que ayudan a construir proteínas y a procesar otros ARN. Este estudio examina una modificación química sutil en esos ARN, llamada pseudouridina, que puede cambiar su comportamiento sin alterar el código genético subyacente. Al cartografiar con precisión dónde ocurren estas modificaciones y qué enzimas las colocan, los autores revelan una inesperada «conversación» entre enzimas que ajusta finamente una parte crucial de la maquinaria de síntesis de proteínas.
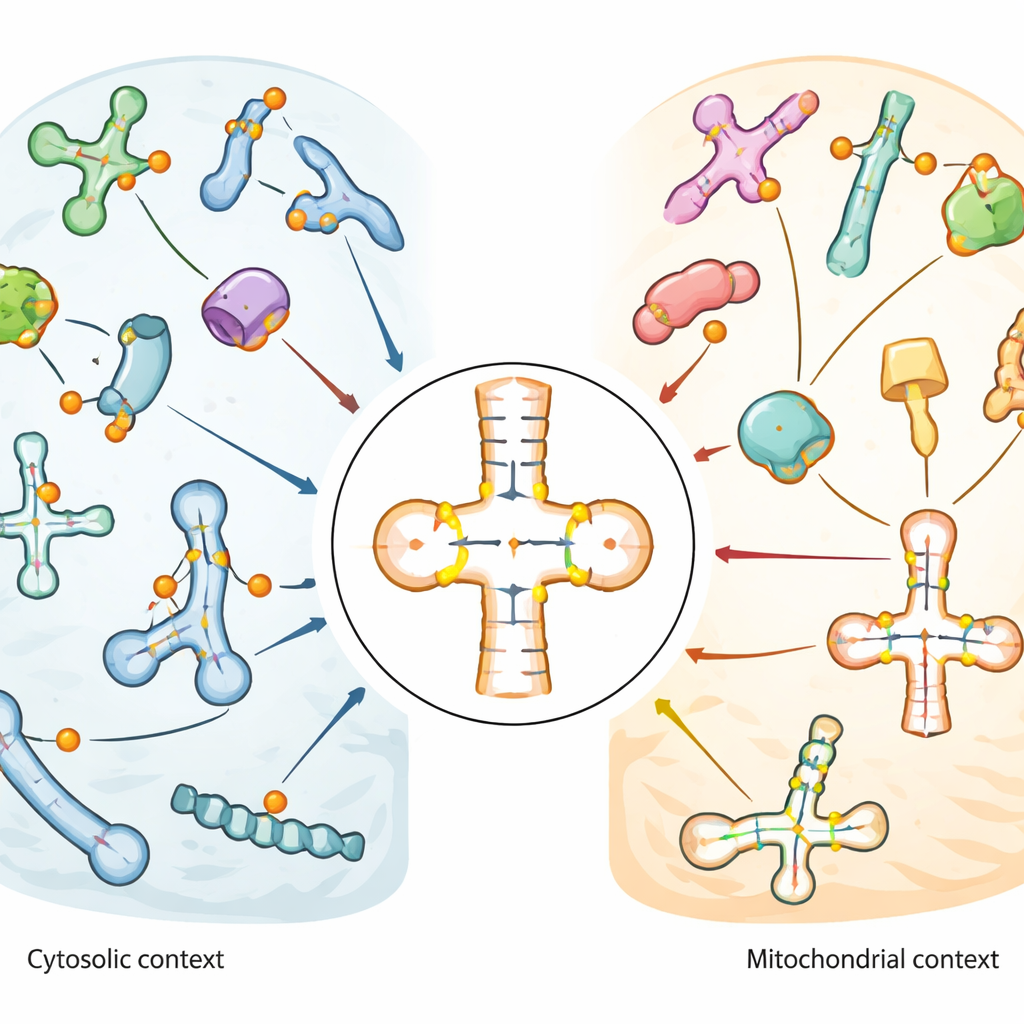
Ediciones químicas en los ARN encargados del trabajo celular
Las células dependen de muchos tipos de ARN pequeños, especialmente de los ARN de transferencia (ARNt), que actúan como adaptadores que leen las palabras de tres letras del código genético y entregan el aminoácido correcto durante la síntesis de proteínas. Estos ARNt, junto con otros ARN pequeños que guían el procesamiento del ARN, están densamente decorados con modificaciones químicas. La pseudouridina es una de las más comunes. Se diferencia de la uridina ordinaria únicamente en la conectividad de sus átomos, pero ese pequeño cambio refuerza el apareamiento de bases y puede alterar la forma y la estabilidad del ARN. Dado que la pseudouridina se asocia con respuestas al estrés, función cerebral y cáncer, los científicos quieren saber exactamente dónde aparece y qué enzimas, llamadas pseudouridina sintasas o enzimas PUS, son responsables.
Construir un mapa preciso de la pseudouridina
Los métodos tradicionales podían señalar muchos sitios de pseudouridina pero tenían dificultades para medir con qué grado cada sitio estaba modificado. Los investigadores refinaron un método químico‑de secuenciación más reciente que desarrollaron previamente, llamado PRAISE, para hacerlo de forma cuantitativa en ARN pequeños. Primero trataron el ARN para eliminar otras modificaciones que bloquean la detección, y luego emplearon una reacción de bisulfito especializada y una estrategia de secuenciación que convierte la presencia de pseudouridina en una señal característica de deleción en la lectura. Aplicado a células HEK293T humanas, generaron un paisaje de alta resolución de pseudouridina en ARNt citosólicos y mitocondriales, así como en ARN nucleares pequeños (snRNA) y ARN nucleolares pequeños (snoRNA). El método demostró ser altamente reproducible y igualó o superó a las técnicas existentes, añadiendo además mediciones precisas del nivel de modificación en cada posición.
Patrones distintos en diferentes vecindarios celulares
El mapa reveló que la pseudouridina está especialmente enriquecida en el bucle‑vástago anticodeón de los ARNt, la región que empareja directamente con el ARNm durante la traducción. Algunas posiciones, como un sitio presente de forma casi universal cerca de la base del ARNt (conocido como posición 55), estaban casi totalmente modificadas en muchos ARNt. Otras mostraron niveles moderados o variables, lo que sugiere flexibilidad regulatoria. Los ARNt mitocondriales, que operan dentro de los orgánulos productores de energía de la célula, mostraron un patrón notablemente distinto: sitios clave comunes en los ARNt citosólicos estaban ausentes o sólo débilmente modificados, mientras que otras posiciones cercanas al anticodeón estaban fuertemente y consistentemente marcadas. Este contraste sugiere que las mitocondrias usan un conjunto distinto de reglas de edición para sus propios ARNt. En snRNA y snoRNA, la pseudouridina se agrupó en regiones funcionales que ayudan a guiar otras modificaciones del ARN o el empalme, y algunos sitios variaron en respuesta a choque térmico o estrés oxidativo.
Quién escribe las marcas: asignación de enzimas a sitios
Para vincular enzimas específicas a sitios concretos del ARN, el equipo comparó células de tipo salvaje con una serie de líneas celulares carentes de enzimas PUS individuales o con niveles reducidos de una enzima guía llamada DKC1. Mostraron que las marcas en snoRNA provienen de dos vías: una vía guiada por ARN que usa DKC1 y una enzima independiente, PUS7, que escribe un sitio distintivo único. En los ARNt, asignaron sistemáticamente muchos sitios a enzimas particulares. PUS1 emergió como un escritor importante de marcas cerca del anticodeón en ARNt tanto citosólicos como mitocondriales. Miembros de la familia RluA dividieron sus funciones: RPUSD1 modificó ciertos sitios en ARNt citosólicos, incluido un sitio previamente no reconocido cerca de la cola del ARNt, mientras RPUSD2 apuntó a posiciones cercanas en ARNt mitocondriales, y RPUSD3 no mostró actividad detectable sobre ARNt. Enzimas relacionadas, PUS1L y PUS7L, resultaron especializarse en regiones o tipos de ARNt distintos, lo que indica que proteínas estrechamente relacionadas pueden evolucionar tareas sorprendentemente diferentes.
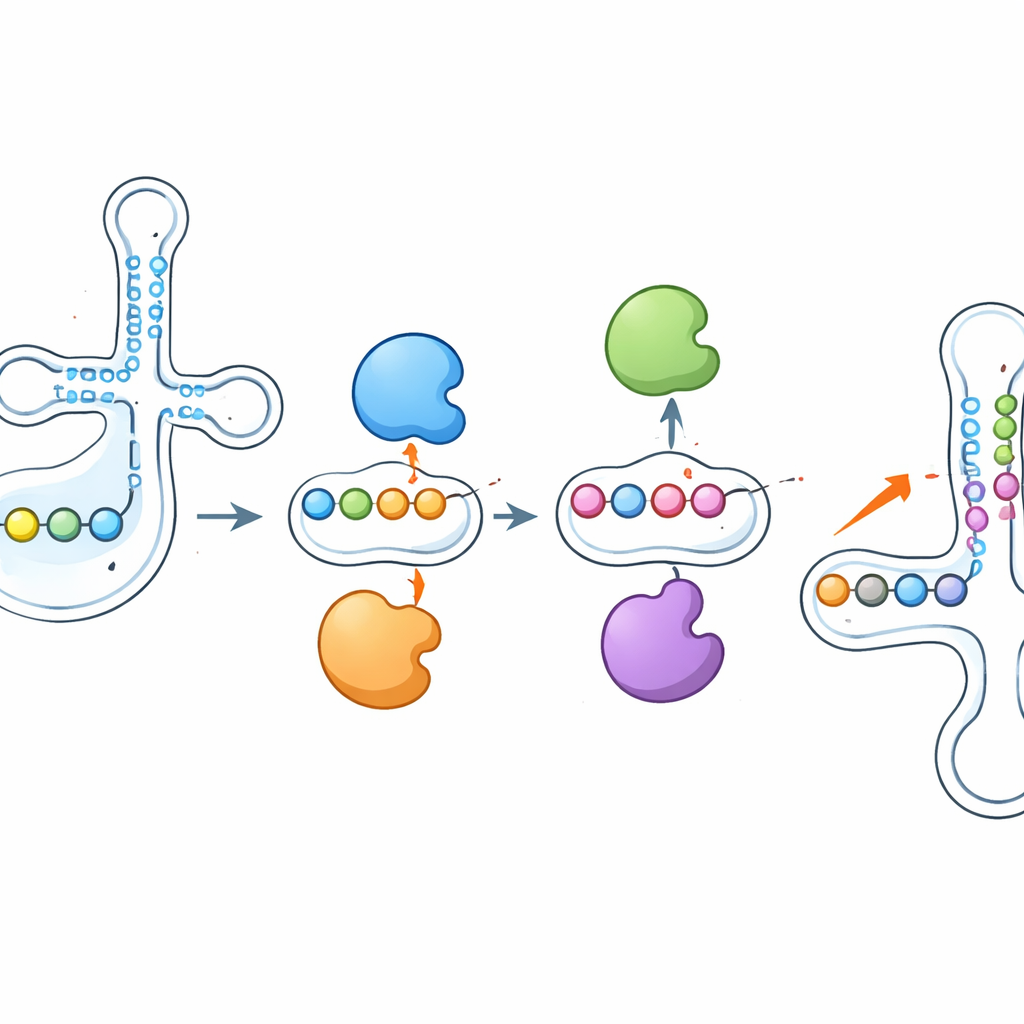
Enzimas que se empujan y se contrarrestan entre sí
Uno de los hallazgos más llamativos fue que estas enzimas no actúan de forma aislada. Cuando los investigadores eliminaron PUS1, las marcas de pseudouridina que normalmente instala cerca del anticodeón cayeron drásticamente, pero los sitios vecinos, escritos por otras enzimas como RPUSD1 o PUS7, se modificaron más intensamente en el mismo ARNt. La eliminación de RPUSD1 produjo la imagen especular en posiciones solapadas, y patrones de balancín similares aparecieron entre PUS7 y otra enzima, PUS3. Estos cambios no se explicaron por variaciones en la abundancia de enzimas o ARNt, lo que apunta a una interacción directa a nivel de moléculas individuales de ARNt. Los autores sugieren que las enzimas pueden competir físicamente por sitios de unión próximos o que añadir o quitar una pseudouridina remodela la estructura local del ARN, haciendo que posiciones vecinas sean más o menos accesibles para otras enzimas.
Qué significa esto para la salud y la enfermedad
Para un público no especialista, el mensaje clave es que las marcas químicas en los ARNt no son decoraciones fijas, sino parte de un sistema dinámico e interconectado. Múltiples enzimas colaboran y compiten para marcar la región del anticodeón, que es central para leer el código genético con precisión y flexibilidad. Dado que mutaciones en varias de estas enzimas causan enfermedades humanas —desde trastornos sanguíneos y debilidad muscular hasta disfunción cerebral y cáncer—, comprender cómo comparten y ajustan sus objetivos puede aclarar por qué la pérdida de una enzima a veces tiene efectos más leves de lo esperado, o cómo las células compensan bajo estrés. Este estudio proporciona un mapa detallado de dónde aparece la pseudouridina en ARN pequeños y muestra que las enzimas que escriben estas marcas pueden modular la actividad de otras, ofreciendo nuevas vías para explorar y, eventualmente, corregir defectos del ARN relacionados con la salud humana.
Cita: Liu, W., Ma, Y., Wang, L. et al. Quantitative analysis of small RNA pseudouridylation reveals interplay of PUS enzymes in tRNA anticodon stem-loop. Nat Commun 17, 2811 (2026). https://doi.org/10.1038/s41467-026-69177-7
Palabras clave: modificaciones del ARNt, pseudouridina, enzimas de ARN, función mitocondrial, regulación de la traducción