Clear Sky Science · ar
تحليل كمي للتزويد الوهمي في الرناّات الصغيرة يكشف تداخلَ إنزيمات PUS في الحلقة الساقية للمضادّ كودون في الرنا الناقل
لماذا تهم العلامات الخفية على الرنا
تقرأ كل خلية باستمرار التعليمات الوراثية عبر جزيئات رنا صغيرة تساعد في بناء البروتينات ومعالجة جزيئات رنا أخرى. تبحث هذه الدراسة في تعديل كيميائي دقيق على هذه الرناّات يُدعى بسودويريدين، الذي يمكن أن يغير سلوكها من دون أن يغيّر الشيفرة الوراثية الأساسية. من خلال رسم خريطة دقيقة لمواضع هذه التعديلات وتحديد الإنزيمات التي تضعها، يكشف المؤلفون عن «حوار» غير متوقع بين إنزيمات تضبط جزءًا حاسمًا من آلية تصنيع البروتينات.
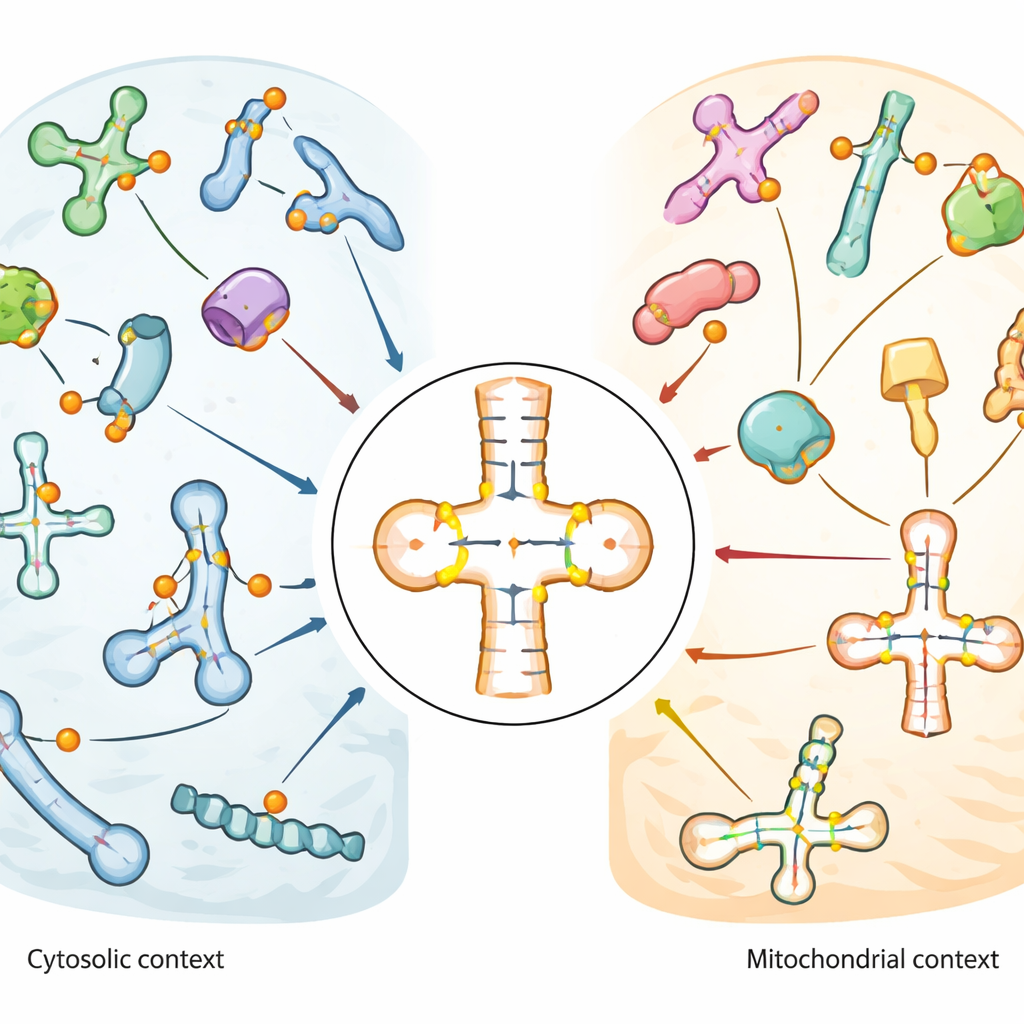
تعديلات كيميائية على رناّات عمل الخلية
تعتمد الخلايا على أنواع متعددة من الرناّات الصغيرة، وخصوصًا الرنا النّاقل (tRNA) الذي يعمل كمحور يقرأ كلماتٍ ثلاثية في الشيفرة الوراثية ويوصل الحمض الأميني المناسب أثناء تصنيع البروتين. هذه الرناّات، إلى جانب رناّات صغيرة أخرى توجه معالجة الرنا، مغطاة بتعديلات كيميائية متعددة. يُعدُّ البسودويريدين واحدًا من الأكثر شيوعًا؛ يختلف عن اليوريدين العادي فقط في ترتيب الروابط بين ذراته، لكن هذا التغيير الطفيف يقوّي الاقتران القاعدي وقد يغيّر شكل الرناّ وثباته. وبما أن البسودويريدين مرتبط باستجابات الإجهاد ووظائف الدماغ والسرطان، يسعى العلماء لمعرفة مواضعه بدقة وأيّ إنزيمات—المسماة سينثازات البسودويريدين أو إنزيمات PUS—تتحكم بها.
بناء خريطة دقيقة للبسودويريدين
كانت الطرق التقليدية قادرة على الإشارة إلى العديد من مواقع البسودويريدين لكنها كانت تواجه صعوبة في قياس مدى شيوع هذا التعديل في كل موقع. طوّر الباحثون طريقة كيميائية-تسلسلية أحدث سبق أن طوروها، مسماة PRAISE، لتعمل كمقياس كمي للرناّات الصغيرة. عالجوا الرنا أولًا لإزالة تعديلات أخرى معيّقة، ثم استخدموا تفاعل ثنائي الكبريتات الاستثنائي واستراتيجية تسلسل تحول وجود البسودويريدين إلى إشارة حذف مميزة في القراءات. بتطبيق هذا على خلايا HEK293T البشرية، أنتجوا خريطة عالية الدقة للبسودويريدين عبر الرناّات الناقلة السيتوسولية والميتوكوندرية، بالإضافة إلى الرناّات النووية الصغيرة (snRNA) والرناّات النووية الجسيمية الصغيرة (snoRNA). أظهرت الطريقة تكرارية عالية وتطابقت أو تفوقت على التقنيات الموجودة مع إضافة قياسات دقيقة لمستوى التعديل في كل موضع.
أنماط مميزة في أحياء خلوية مختلفة
أظهرت الخريطة أن البسودويريدين يتركّز بشكل خاص في الحلقة الساقية للمضادّ كودون في الرناّات الناقلة، المنطقة التي تقترن مباشرةً بالرنا الرسول خلال الترجمة. بعض المواضع، مثل موقع موجود عالميًا قرب قاعدة الرنا (المعروف بالموقع 55)، كانت معدلة تقريبًا بالكامل عبر العديد من الرناّات. أما مواضع أخرى فبدت بمستويات متوسطة أو متغيرة، مما يوحي بمرونة تنظيمية. أظهر الرناّات الناقلة الميتوكوندرية، التي تعمل داخل عضيات إنتاج الطاقة في الخلية، نمطًا مختلفًا بوضوح: مواقع رئيسية موجودة في الرناّات السيتوسولية كانت مفقودة أو ضعيفة التعديل في الميتوكوندريا، بينما كانت مواقع أخرى قرب المضاد كودون قوية ومتماثلة التعديل. يوحي هذا التباين بأن الميتوكوندريا تستخدم قواعد تعديل مميزة لرناّتها الخاصة. في snRNA وsnoRNA، تحدثت البسودويريدين في مناطق وظيفية تساعد على توجيه تعديلات رنا أخرى أو الشبيك (splicing)، وتغيرت بعض المواقع استجابةً للصدمة الحرارية أو الإجهاد التأكسدي.
من يكتب العلامات: تعيين الإنزيمات إلى المواقع
لربط إنزيمات محددة بمواقع معينة على الرنا، قارن الفريق الخلايا البرية بسلاسل خلوية متباينة تفتقر إلى كل إنزيم PUS على حدة أو ذات مستويات منقوصة لإنزيم مرشِد يُدعى DKC1. أظهروا أن علامات snoRNA تأتي عبر مسارين: مسار موجه بالرنا باستخدام DKC1 وإنزيم مستقل PUS7 يكتب موقعًا مميّزًا واحدًا. في الرناّات الناقلة، نسبوا منهجيًا العديد من المواقع إلى إنزيمات محددة. برز PUS1 ككاتب رئيسي لعلامات قرب المضاد كودون في كل من الرناّات السيتوسولية والميتوكوندرية. تفرّعت مهام عائلة RluA: عدّل RPUSD1 مواقع معينة في الرناّات السيتوسولية، بما في ذلك موقع لم يُلاحظ سابقًا قرب ذيل الرنا، بينما استهدف RPUSD2 مواقع مجاورة في الرناّات الميتوكوندرية، ولم تُظهر RPUSD3 نشاطًا واضحًا على الرناّ الناقل. تبين أن الإنزيمات ذات الصلة PUS1L وPUS7L تتخصّصان في مناطق أو أنواع رنا مختلفة، مما يدل على أن بروتينات متقاربة قد تطور مهامًا متباينة بشكل مفاجئ.
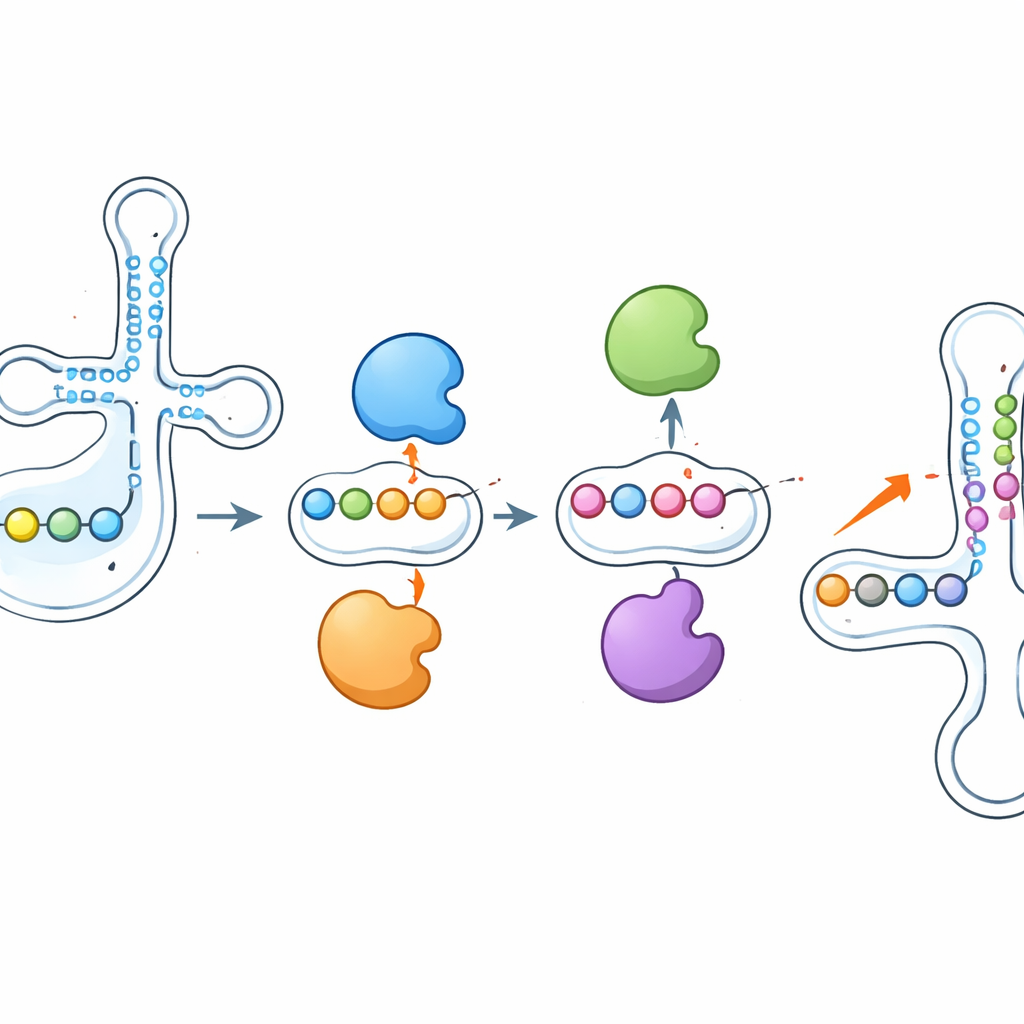
إنزيمات تدفع وتعيق عمل بعضها البعض
أحد الاكتشافات اللافتة هو أن هذه الإنزيمات لا تعمل بصورة منعزلة. عند حذف PUS1، تراجعت علامات البسودويريدين التي يضعها عادة قرب المضاد كودون بشكل حاد—لكن المواقع المجاورة، المكتوبة بواسطة إنزيمات أخرى مثل RPUSD1 أو PUS7، ازدادت شدتها على نفس الرنا. أنتج حذف RPUSD1 الصورة المعاكسة في مواقع متداخلة، وظهرت أنماط تَرجَاحية مشابهة بين PUS7 وإنزيم آخر، PUS3. لم تفسّر هذه التغيرات تحولات في كمية الإنزيم أو الرنا، مما يشير إلى تداخل مباشر على مستوى جزيئات الرنا الفردية. يقترح المؤلفون أن الإنزيمات قد تتنافس جسديًا على مواقع ارتباط قريبة أو أن إضافة أو إزالة بسودويريدين يعيد تشكيل البنية المحلية للرنا، مما يجعل مواضع قريبة أكثر أو أقل وصولًا لإنزيمات أخرى.
ما يعنيه هذا للصحة والمرض
لغير المتخصص، الرسالة الأساسية هي أن العلامات الكيميائية على الرناّات الناقلة ليست زخرفة ثابتة بل جزء من نظام ديناميكي ومترابط. تتعاون وتتنافس إنزيمات متعددة لتشكيل نمط في منطقة المضاد كودون، وهي مركزية لقراءة الشيفرة الوراثية بدقة ومرونة. وبما أن طفرات في عدة من هذه الإنزيمات تسبب أمراضًا بشرية—من اضطرابات دموية وضعف العضلات إلى اختلالات دماغية والسرطان—فإن فهم كيفية مشاركة هذه الإنزيمات وتعديلها لأهدافها قد يوضح لماذا يؤدي فقدان إنزيم واحد أحيانًا إلى تأثيرات أخف مما كان متوقعًا، أو كيف تعوّض الخلايا تحت الإجهاد. تزود هذه الدراسة خريطة مفصلة لمواضع البسودويريدين على الرناّات الصغيرة وتُظهر أن الإنزيمات التي تكتب هذه العلامات يمكن أن تُعدّل نشاط بعضها البعض، ما يفتح نقاط دخول جديدة لاستكشاف وتصحيح عيوب قائمة على الرنا في الصحة البشرية.
الاستشهاد: Liu, W., Ma, Y., Wang, L. et al. Quantitative analysis of small RNA pseudouridylation reveals interplay of PUS enzymes in tRNA anticodon stem-loop. Nat Commun 17, 2811 (2026). https://doi.org/10.1038/s41467-026-69177-7
الكلمات المفتاحية: تعديلات رنا ناقل, بسودويريدين, إنزيمات الرنا, وظيفة الميتوكوندريا, تنظيم الترجمة