Clear Sky Science · de
Quantitative Analyse der Pseudouridylierung kleiner RNAs zeigt das Zusammenspiel von PUS‑Enzymen in der Anticodon‑Stamm‑Schleife der tRNA
Warum verborgene Kennzeichnungen auf RNA wichtig sind
Jede Zelle liest ständig genetische Anweisungen mit Hilfe kleiner RNA‑Moleküle, die beim Aufbau von Proteinen und bei der Verarbeitung anderer RNAs helfen. Diese Studie untersucht eine subtile chemische Modifikation an diesen RNAs, das sogenannte Pseudouridin, das ihr Verhalten verändern kann, ohne den zugrundeliegenden genetischen Code zu verändern. Durch die exakte Kartierung, wo diese Modifikationen auftreten und welche Enzyme sie setzen, zeigen die Autorinnen und Autoren ein unerwartetes "Gespräch" zwischen Enzymen auf, das einen entscheidenden Teil der Proteinmaschine präzise abstimmt.
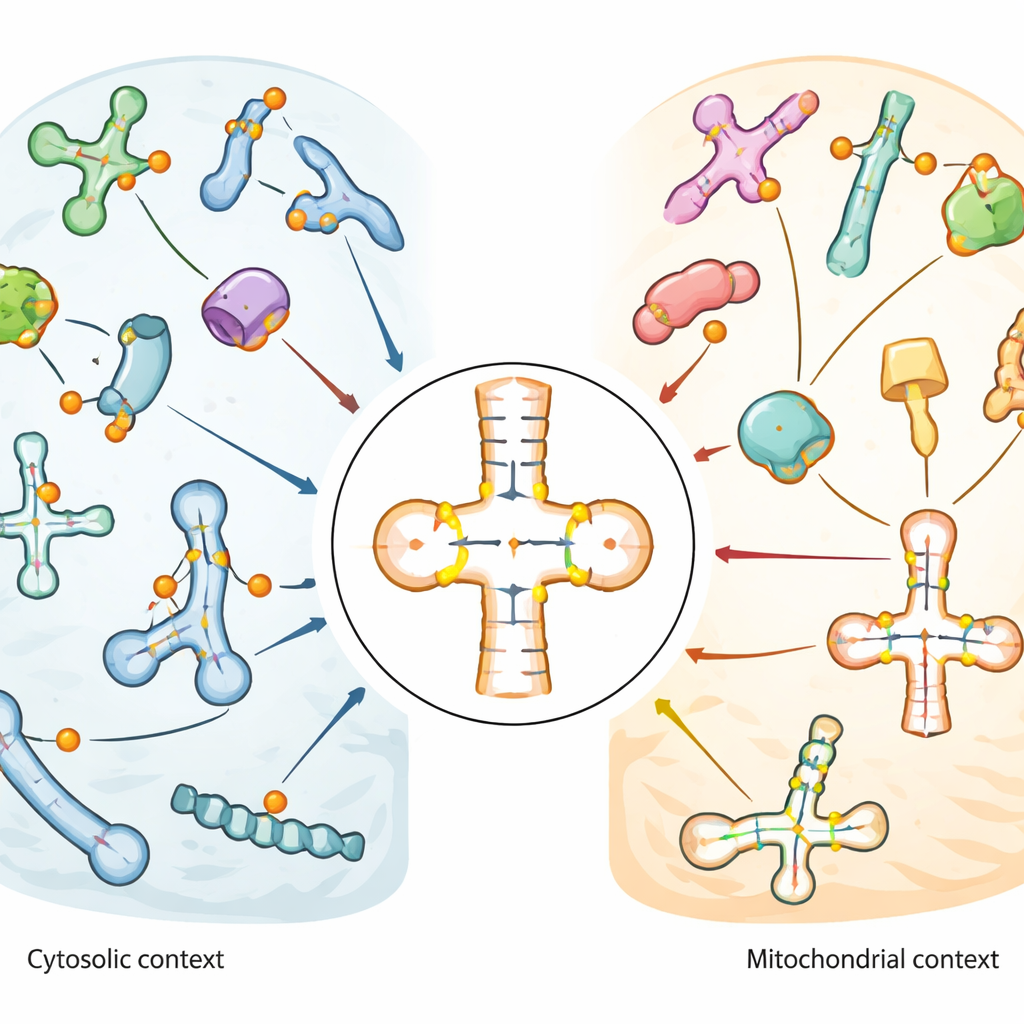
Chemische Editierungen an den Arbeitspferden der Zelle: RNAs
Zellen sind auf viele Arten kleiner RNAs angewiesen, besonders auf Transfer‑RNAs (tRNAs), die als Adapter fungieren: Sie lesen die drei‑buchstabigen Wörter im genetischen Code und bringen während der Proteinsynthese die passende Aminosäure. Diese tRNAs sowie andere kleine RNAs, die die RNA‑Verarbeitung steuern, sind dicht mit chemischen Modifikationen versehen. Pseudouridin ist eine der häufigsten. Es unterscheidet sich vom gewöhnlichen Uridin nur in der Verknüpfung seiner Atome, doch diese kleine Änderung verstärkt die Basenpaarung und kann Form und Stabilität der RNA verändern. Weil Pseudouridin mit Stressreaktionen, Gehirnfunktionen und Krebs verbunden ist, möchten Forschende genau wissen, wo es vorkommt und welche Enzyme, sogenannte Pseudouridin‑Synthetasen oder PUS‑Enzyme, dafür verantwortlich sind.
Eine präzise Karte der Pseudouridylierung erstellen
Traditionelle Methoden konnten viele Pseudouridin‑Stellen identifizieren, hatten aber Schwierigkeiten, das Ausmaß der Modifikation an einzelnen Stellen zu quantifizieren. Die Forschenden verfeinerten eine neuere chemische Sequenziermethode, die sie zuvor entwickelt hatten und PRAISE nennen, sodass sie diese quantitativ auf kleine RNAs anwenden konnten. Zunächst entfernten sie andere blockierende Modifikationen aus der RNA, dann nutzten sie eine spezielle Bisulfit‑Reaktion und Sequenzierstrategie, die das Vorhandensein von Pseudouridin in ein charakteristisches Deletionssignal im Lesergebnis verwandelt. Angewandt auf menschliche HEK293T‑Zellen erzeugten sie eine hochauflösende Landschaft der Pseudouridylierung über zytosolische und mitochondriale tRNAs sowie über kleine nukleäre RNAs (snRNAs) und kleine nukleolare RNAs (snoRNAs). Die Methode erwies sich als hoch reproduzierbar und entsprach vorhandenen Techniken oder übertraf sie, während sie präzise Messungen des Modifikationsgrades an jeder Position hinzufügte.
Unterschiedliche Muster in verschiedenen zellulären Nachbarschaften
Die Karte zeigte, dass Pseudouridin besonders in der Anticodon‑Stamm‑Schleife der tRNAs angereichert ist — dem Bereich, der direkt mit der messenger‑RNA während der Translation paart. Einige Positionen, wie eine universell vorkommende Stelle in der Nähe der tRNA‑Basis (bekannt als Position 55), waren bei vielen tRNAs nahezu vollständig modifiziert. Andere zeigten moderate oder variable Level, was auf regulatorische Flexibilität hindeutet. Mitochondriale tRNAs, die innerhalb der energieproduzierenden Organellen der Zelle arbeiten, zeigten ein auffallend anderes Muster: Schlüsselpunkte, die in regulären (zytosolischen) tRNAs üblich sind, fehlten oder waren nur schwach modifiziert, während andere Positionen in der Nähe des Anticodons stark und konsistent markiert waren. Dieser Kontrast legt nahe, dass Mitochondrien eigene Regeln für die Editierung ihrer tRNAs verwenden. In snRNAs und snoRNAs gruppierte sich Pseudouridin in funktionellen Regionen, die andere RNA‑Modifikationen oder das Spleißen steuern, und einige Stellen veränderten sich als Reaktion auf Hitzeschock oder oxidativen Stress.
Wer setzt die Markierungen: Zuordnung von Enzymen zu Stellen
Um spezifische Enzyme bestimmten RNA‑Stellen zuzuordnen, verglich das Team Wildtyp‑Zellen mit einer Reihe von Zelllinien, denen einzelne PUS‑Enzyme fehlten oder die verringerte Mengen eines leitenden Enzyms namens DKC1 aufwiesen. Sie zeigten, dass snoRNA‑Markierungen über zwei Wege entstehen: einen RNA‑geführten Weg unter Nutzung von DKC1 und ein eigenständiges Enzym PUS7, das eine einzelne charakteristische Stelle schreibt. In tRNAs ordneten sie systematisch viele Stellen bestimmten Enzymen zu. PUS1 erwies sich als ein Hauptschreiber von Markierungen in der Nähe des Anticodons sowohl in zytosolischen als auch in mitochondrialen tRNAs. Mitglieder der RluA‑Familie teilten ihre Aufgaben auf: RPUSD1 modifizierte bestimmte Stellen in zytosolischen tRNAs, darunter eine zuvor unerkannte Position in der Nähe des tRNA‑Endes, während RPUSD2 benachbarte Positionen in mitochondrialen tRNAs ansprach, und RPUSD3 zeigte keine nachweisbare tRNA‑Aktivität. Verwandte Enzyme PUS1L und PUS7L spezialisierten sich auf unterschiedliche Regionen oder tRNA‑Typen, was darauf hindeutet, dass eng verwandte Proteine überraschend verschiedene Aufgaben entwickeln können.
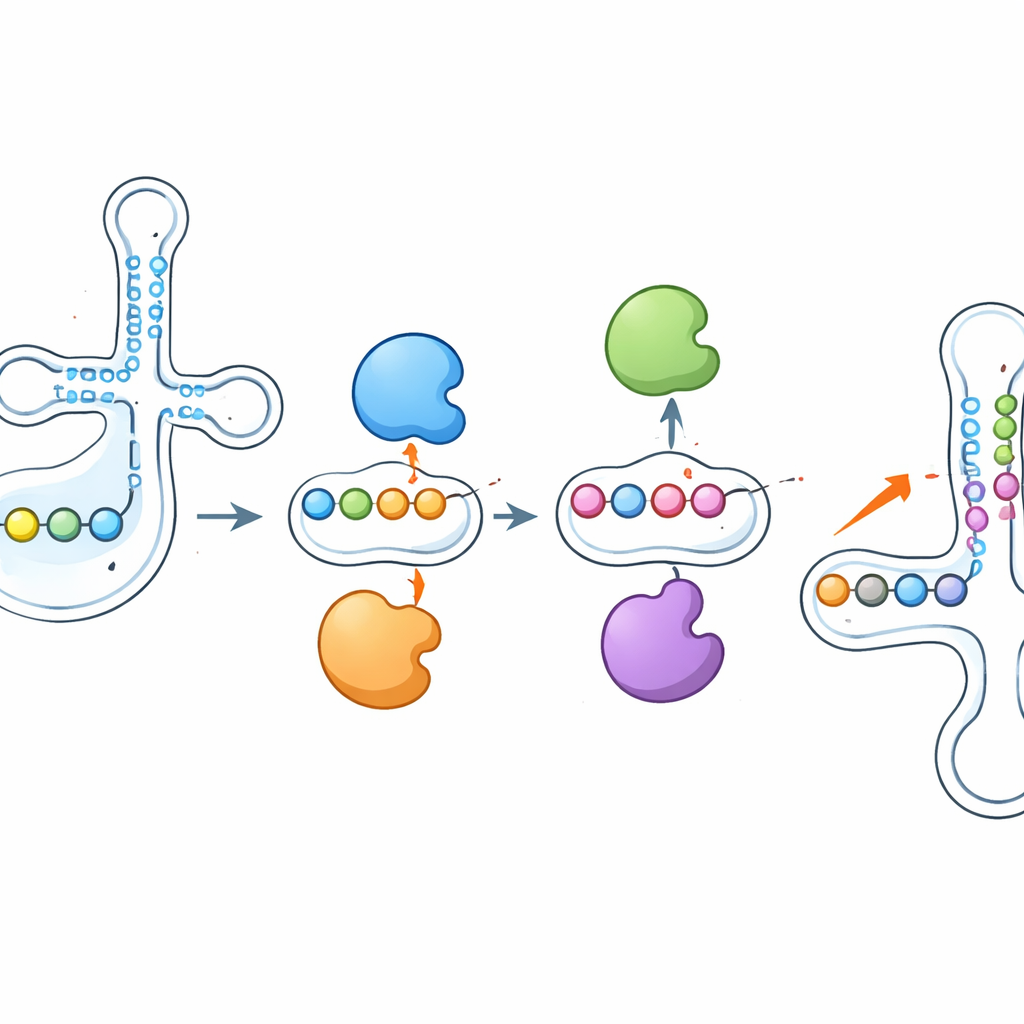
Enzyme, die sich gegenseitig beeinflussen
Eines der eindrücklichsten Ergebnisse war, dass diese Enzyme nicht isoliert wirken. Wenn die Forschenden PUS1 löschten, fielen die Pseudouridin‑Markierungen, die es normalerweise in der Nähe des Anticodons anbringt, stark ab — aber benachbarte Stellen, die von anderen Enzymen wie RPUSD1 oder PUS7 geschrieben werden, zeigten auf derselben tRNA vermehrt Modifikationen. Das Entfernen von RPUSD1 ergab das Spiegelbild an überlappenden Positionen, und ähnliche Wippe‑Muster traten zwischen PUS7 und einem anderen Enzym, PUS3, auf. Diese Veränderungen ließen sich nicht durch Verschiebungen in der Enzym‑ oder tRNA‑Abundanz erklären, was auf ein direktes Zusammenspiel auf der Ebene einzelner tRNA‑Moleküle hinweist. Die Autorinnen und Autoren schlagen vor, dass Enzyme physisch um benachbarte Bindungsstellen konkurrieren könnten oder dass das Hinzufügen oder Entfernen eines Pseudouridins die lokale RNA‑Struktur so umgestaltet, dass benachbarte Positionen für andere Enzyme besser oder schlechter zugänglich werden.
Was das für Gesundheit und Krankheit bedeutet
Für Nicht‑Spezialisten lautet die Kernbotschaft: Die chemischen Markierungen auf tRNAs sind keine festen Verzierungen, sondern Teil eines dynamischen, vernetzten Systems. Mehrere Enzyme arbeiten zusammen und konkurrieren, um die Muster in der Anticodon‑Region zu gestalten, die zentral dafür ist, den genetischen Code genau und flexibel zu lesen. Da Mutationen in mehreren dieser Enzyme beim Menschen Krankheiten hervorrufen — von Blutstörungen und Muskelschwäche bis zu Gehirnfunktionsstörungen und Krebs — kann das Verständnis, wie sie ihre Ziele teilen und anpassen, erklären, warum der Verlust eines Enzyms manchmal mildere Effekte hat als erwartet oder wie Zellen bei Stress kompensieren. Diese Studie liefert eine detaillierte Karte, wo Pseudouridin auf kleinen RNAs vorkommt, und zeigt, dass die Enzyme, die diese Markierungen setzen, sich gegenseitig modulieren können, was neue Ansatzpunkte eröffnet, um RNA‑basierte Defekte in der menschlichen Gesundheit zu erforschen und möglicherweise zu korrigieren.
Zitation: Liu, W., Ma, Y., Wang, L. et al. Quantitative analysis of small RNA pseudouridylation reveals interplay of PUS enzymes in tRNA anticodon stem-loop. Nat Commun 17, 2811 (2026). https://doi.org/10.1038/s41467-026-69177-7
Schlüsselwörter: tRNA‑Modifikationen, Pseudouridin, RNA‑Enzyme, mitochondriale Funktion, Translationsregulation