Clear Sky Science · fr
Analyse quantitative de la pseudouridylation des petits ARN révèle l’interaction des enzymes PUS dans la boucle tige‑anticodon de l’ARNt
Pourquoi les marques cachées sur l’ARN comptent
Chaque cellule lit en permanence les instructions génétiques à l’aide de petits ARN qui aident à assembler les protéines et à traiter d’autres ARN. Cette étude examine une retouche chimique subtile sur ces ARN, appelée pseudouridine, qui peut modifier leur comportement sans altérer le code génétique sous‑jacent. En cartographiant précisément où ces retouches apparaissent et quelles enzymes les déposent, les auteurs révèlent une « conversation » inattendue entre enzymes qui ajuste finement une partie cruciale de la machinerie de fabrication des protéines.
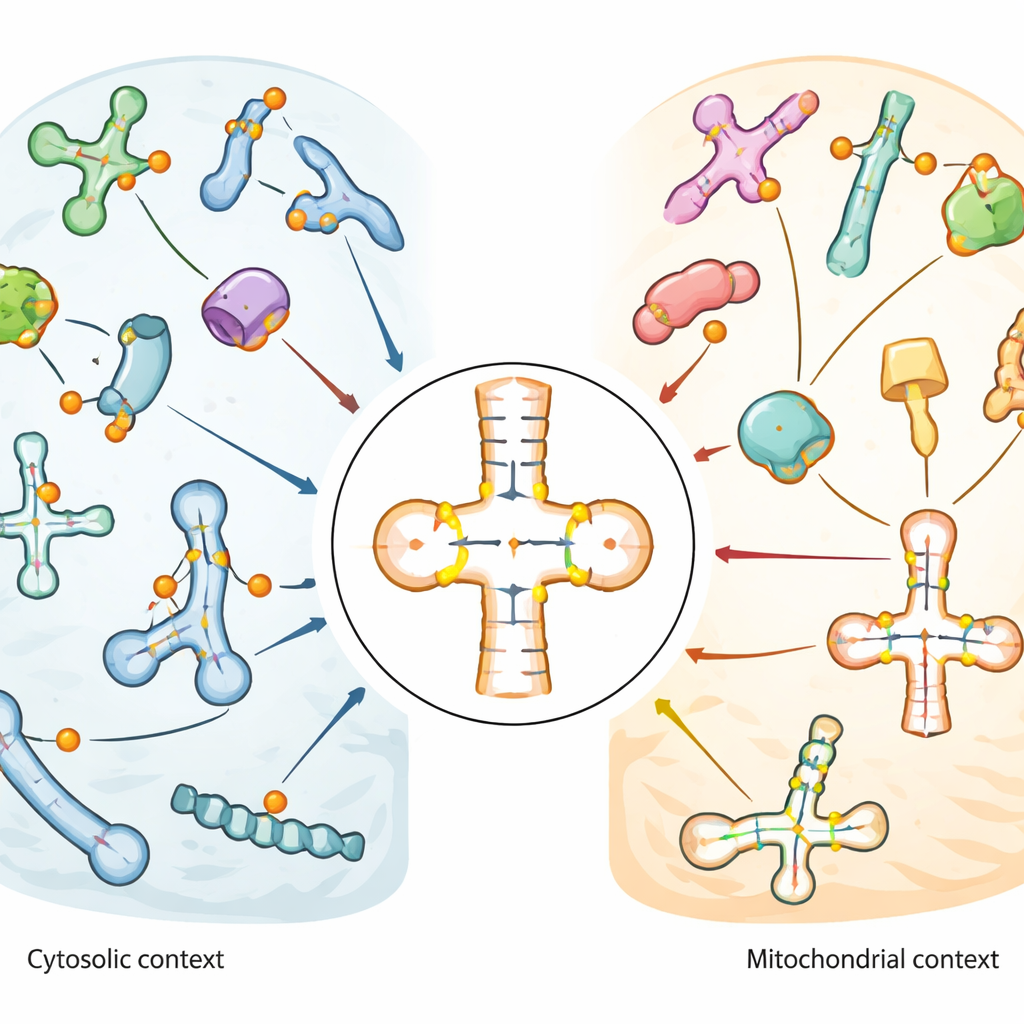
Éditions chimiques sur les ARN essentiels de la cellule
Les cellules comptent sur de nombreux types de petits ARN, en particulier les ARN de transfert (ARNt), qui servent d’adaptateurs lisant les mots de trois lettres du code génétique et apportant l’acide aminé approprié lors de la synthèse protéique. Ces ARNt, ainsi que d’autres petits ARN qui guident le traitement des ARN, sont densément décorés de modifications chimiques. La pseudouridine est l’une des plus courantes. Elle se distingue de l’uridine ordinaire uniquement par la manière dont ses atomes sont liés, mais ce petit changement renforce l’appariement des bases et peut modifier la conformation et la stabilité de l’ARN. Étant donné que la pseudouridine est liée aux réponses au stress, à la fonction cérébrale et au cancer, les chercheurs veulent savoir exactement où elle apparaît et quelles enzymes, appelées pseudouridine synthases ou enzymes PUS, en sont responsables.
Construire une carte précise de la pseudouridine
Les méthodes traditionnelles pouvaient repérer de nombreux sites de pseudouridine mais peinaient à mesurer l’étendue d’altération de chaque site. Les chercheurs ont perfectionné une méthode chimico‑séquencielle plus récente qu’ils avaient développée, appelée PRAISE, pour l’appliquer de manière quantitative aux petits ARN. Ils ont d’abord traité les ARN pour éliminer d’autres modifications bloquantes, puis utilisé une réaction bisulfite spécialisée et une stratégie de séquençage qui convertit la présence de pseudouridine en un signal de délétion caractéristique dans la lecture. En appliquant cela à des cellules HEK293T humaines, ils ont généré un paysage haute résolution de la pseudouridine sur les ARNt cytosoliques et mitochondriaux, ainsi que sur les petits ARN nucléaires (snARN) et nucléolaires (snoARN). La méthode s’est avérée hautement reproductible et a égalé ou dépassé les techniques existantes, tout en fournissant des mesures précises du niveau de modification à chaque position.
Schémas distincts selon les quartiers cellulaires
La carte a révélé que la pseudouridine est particulièrement enrichie dans la boucle tige‑anticodon des ARNt, la région qui s’apparie directement avec l’ARN messager lors de la traduction. Certaines positions, comme un site universellement présent près de la base de l’ARNt (connu sous le nom de position 55), étaient presque entièrement modifiées dans de nombreux ARNt. D’autres montraient des niveaux modérés ou variables, suggérant une flexibilité régulatrice. Les ARNt mitochondriaux, qui fonctionnent à l’intérieur des organites productrices d’énergie de la cellule, présentaient un schéma sensiblement différent : des sites clés communs aux ARNt cytosoliques étaient absents ou faiblement modifiés, tandis que d’autres positions proches de l’anticodon étaient fortement et constamment marquées. Ce contraste implique que les mitochondries appliquent un ensemble distinct de règles d’édition pour leurs propres ARNt. Dans les snARN et snoARN, la pseudouridine se regroupait dans des régions fonctionnelles aidant à guider d’autres modifications d’ARN ou l’épissage, et certains sites variaient en réponse au choc thermique ou au stress oxydatif.
Qui écrit les marques : attribuer des enzymes aux sites
Pour relier des enzymes spécifiques à des sites particuliers, l’équipe a comparé des cellules de type sauvage avec une série de lignées cellulaires dépourvues d’enzymes PUS individuelles ou avec des niveaux réduits d’une enzyme guide appelée DKC1. Ils ont montré que les marques sur les snoARN proviennent de deux voies : une voie guidée par ARN utilisant DKC1 et une enzyme indépendante, PUS7, qui écrit un site distinctif unique. Dans les ARNt, ils ont attribué systématiquement de nombreux sites à des enzymes particulières. PUS1 est apparue comme une principale rédactrice de marques près de l’anticodon, tant dans les ARNt cytosoliques que mitochondriaux. Les membres de la famille RluA ont partagé leurs tâches : RPUSD1 modifiait certains sites dans les ARNt cytosoliques, y compris un site jusqu’alors méconnu près de la queue de l’ARNt, tandis que RPUSD2 ciblait des positions voisines dans les ARNt mitochondriaux, et RPUSD3 n’a montré aucune activité détectable sur les ARNt. Les enzymes apparentées PUS1L et PUS7L se sont révélées spécialisées dans des régions ou types d’ARNt distincts, indiquant que des protéines très proches peuvent évoluer vers des fonctions étonnamment différentes.
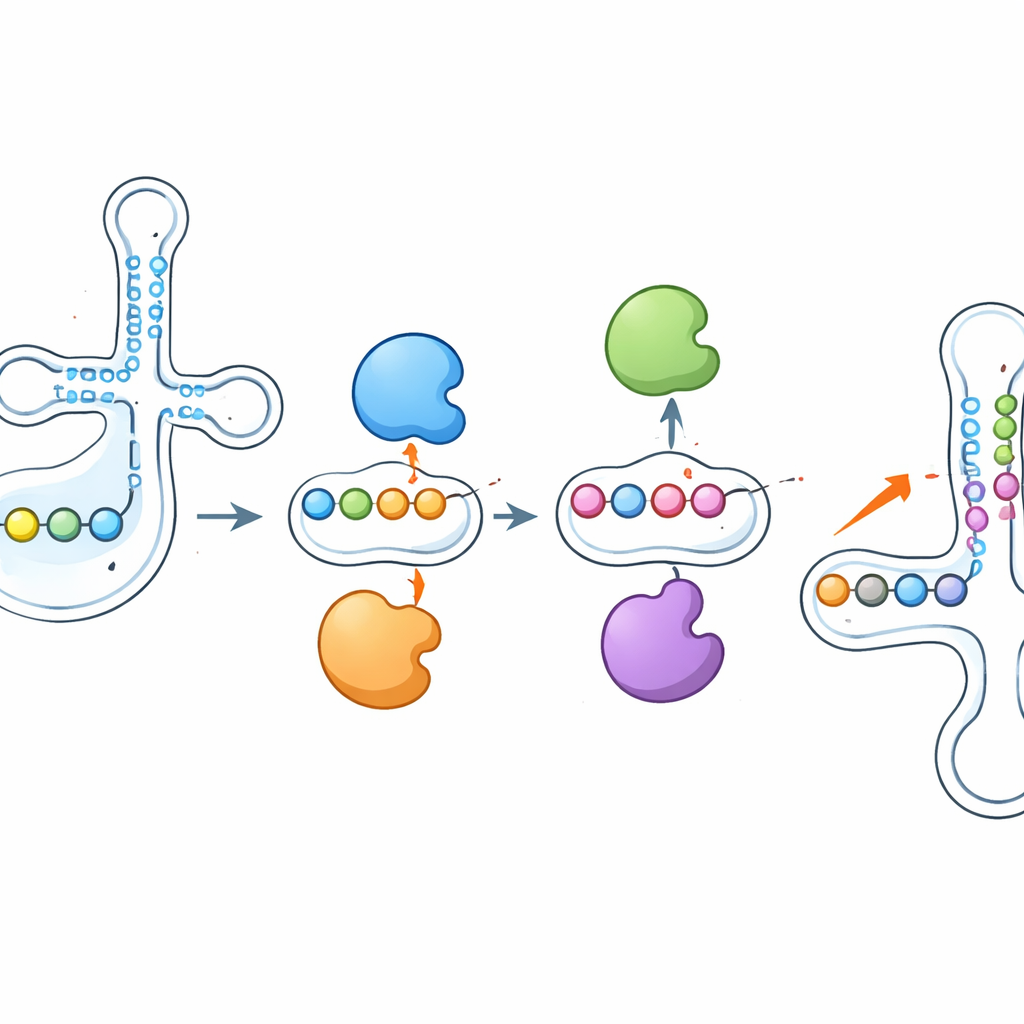
Des enzymes qui se poussent et se freinent mutuellement
Une des découvertes les plus marquantes est que ces enzymes n’agissent pas isolément. Lorsque les chercheurs ont supprimé PUS1, les marques de pseudouridine qu’elle installe normalement près de l’anticodon ont fortement diminué — mais des sites voisins, écrits par d’autres enzymes comme RPUSD1 ou PUS7, sont devenus plus fortement modifiés sur le même ARNt. L’invalidation de RPUSD1 a produit l’image miroir aux positions chevauchantes, et des schémas de bascule similaires sont apparus entre PUS7 et une autre enzyme, PUS3. Ces changements ne s’expliquaient pas par des variations d’abondance des enzymes ou des ARNt, ce qui indique une interaction directe au niveau des molécules d’ARNt individuelles. Les auteurs suggèrent que les enzymes peuvent physiquement se concurrencer pour des sites de liaison proches ou que l’ajout ou le retrait d’une pseudouridine reconfigure la structure locale de l’ARN, rendant les positions voisines plus ou moins accessibles à d’autres enzymes.
Ce que cela signifie pour la santé et la maladie
Pour un non‑spécialiste, le message clé est que les marques chimiques sur les ARNt ne sont pas de simples décorations fixes mais font partie d’un système dynamique et interconnecté. De multiples enzymes collaborent et se font concurrence pour dessiner le motif de la région anticodon, centrale pour lire le code génétique avec précision et souplesse. Parce que des mutations dans plusieurs de ces enzymes provoquent des maladies humaines — des troubles sanguins et une faiblesse musculaire aux dysfonctionnements cérébraux et au cancer — comprendre comment elles partagent et ajustent leurs cibles peut éclairer pourquoi la perte d’une enzyme a parfois des effets plus doux que prévu, ou comment les cellules compensent sous stress. Cette étude fournit une carte détaillée des sites de pseudouridine sur les petits ARN et montre que les enzymes qui écrivent ces marques peuvent moduler l’activité les unes des autres, ouvrant de nouvelles voies pour explorer et éventuellement corriger des défauts d’ARN impliqués dans la santé humaine.
Citation: Liu, W., Ma, Y., Wang, L. et al. Quantitative analysis of small RNA pseudouridylation reveals interplay of PUS enzymes in tRNA anticodon stem-loop. Nat Commun 17, 2811 (2026). https://doi.org/10.1038/s41467-026-69177-7
Mots-clés: modifications de l’ARNt, pseudouridine, enzymes ARN, fonction mitochondriale, régulation de la traduction