Clear Sky Science · ja
小さなRNAのジヌクレオチド改変の定量解析はtRNAアンチコドン幹ループにおけるPUS酵素の相互作用を明らかにする
なぜRNA上の「隠れた印」が重要か
細胞は常に小さなRNA分子を使って遺伝情報を読み取り、タンパク質合成や他のRNAの加工を助けています。本研究は、遺伝コード自体を変えずにRNAの振る舞いを変えうる微細な化学修飾、プシウリジン(pseudouridine)に注目します。修飾がどこに入り、どの酵素によって付与されるかを正確にマップすることで、著者らはタンパク質合成装置の重要な一部を微調整する酵素同士の予期せぬ“会話”を明らかにしています。
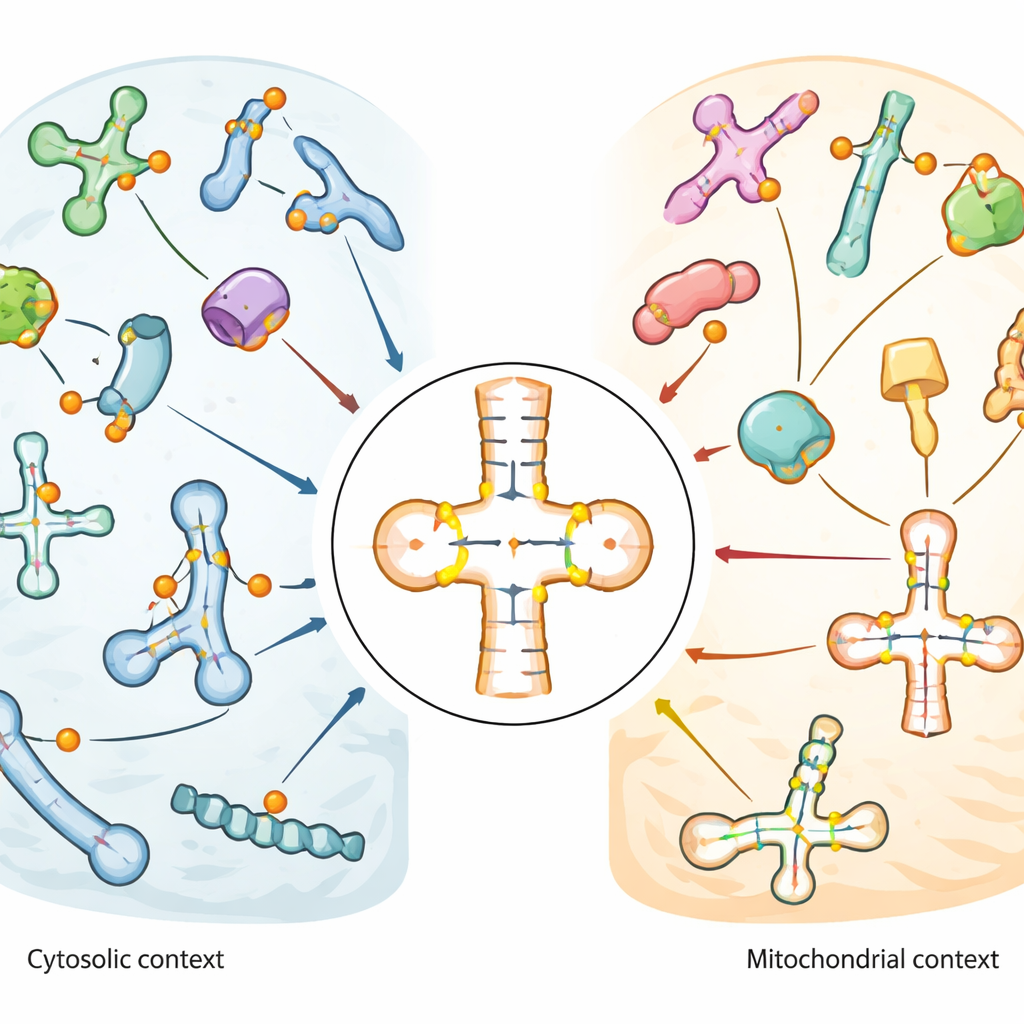
細胞の主力RNAに施される化学的手入れ
細胞は多様な小さなRNAを利用しますが、特にトランスファーRNA(tRNA)は遺伝コードの三文字語を読み取り、適切なアミノ酸を供給するアダプターとして働きます。これらのtRNAやRNA加工を導く小さなRNA群は多くの化学修飾で飾られており、プシウリジンはその代表的な一つです。プシウリジンは通常のウリジンと原子の結びつきが異なるだけですが、その差は塩基対形成を強化し、RNAの立体構造や安定性を変えます。プシウリジンはストレス応答、脳機能、がんに関連するため、どこに現れるか、どの擬似ウリジン合成酵素(PUS酵素)が関与するかを正確に知ることが望まれています。
プシウリジンの精密な地図を作る
従来法は多くのプシウリジン部位を検出できましたが、各部位がどの程度修飾されているかを測るのは難しかったです。研究者たちは以前に開発した化学―シーケンス法PRAISEを改良し、小さなRNAで定量的に解析できるようにしました。まず他の阻害的修飾を除去し、続いて特殊なビスルファイト反応と配列決定戦略を用いることで、プシウリジンの存在を配列上の特徴的な欠失シグナルとして検出します。これをヒトHEK293T細胞に適用して、細胞質およびミトコンドリアのtRNA、さらに小核RNA(snRNA)や小核小体RNA(snoRNA)にわたる高解像度のプシウリジン地図を得ました。この手法は高い再現性を示し、既存技術と同等かそれ以上の性能を持ち、各位置での修飾率を正確に測定できました。
細胞内の異なる環境で異なるパターン
地図は、プシウリジンがtRNAのアンチコドン幹ループに特に集積していることを示しました。この領域は翻訳時にメッセンジャーRNAと直接対合する部分です。基底近傍に普遍的に存在する位置(位置55として知られるような)は多くのtRNAでほぼ完全に修飾されていましたが、他の部位は中等度または可変な修飾率を示し、調節の余地を示唆しました。ミトコンドリアtRNAは、細胞のエネルギー産生小器官内で働くため、パターンが著しく異なり、細胞質性tRNAで一般的な主要部位が欠如するか弱くしか修飾されていない一方で、アンチコドン近傍の他の位置は強く一貫して修飾されていました。この対比はミトコンドリアが独自のtRNA編集規則を用いていることを示唆します。snRNAやsnoRNAでは、プシウリジンは他のRNA修飾やスプライシングを導く機能領域に集まり、熱ショックや酸化ストレスに応答して一部の部位が変化しました。
誰が印を書き込むか:酵素と部位の対応付け
特定の酵素を特定のRNA部位に結びつけるため、研究チームは野生型細胞と個々のPUS酵素を欠く細胞株やガイド酵素DKC1のレベルが低下した細胞株を比較しました。snoRNA上のマークは二つの経路から生じることを示しました。すなわちDKC1によるRNAガイド経路と、単独で特異的な一箇所を書き込むPUS7です。tRNAでは、多くの部位を系統的に特定の酵素に割り当てました。PUS1は細胞質性・ミトコンドリア両方のtRNAにおけるアンチコドン近傍の主要な書き手として浮上しました。RluAファミリーのメンバーは役割を分担しており、RPUSD1は細胞質tRNAの特定部位、以前は認識されていなかったtRNA末端近傍の部位を修飾し、RPUSD2はミトコンドリアtRNAの近接位置を標的とし、RPUSD3は検出可能なtRNA活性を示しませんでした。関連酵素のPUS1LやPUS7Lは異なる領域やtRNAタイプに特化しており、近縁タンパク質が驚くほど異なる役割に進化し得ることを示しています。
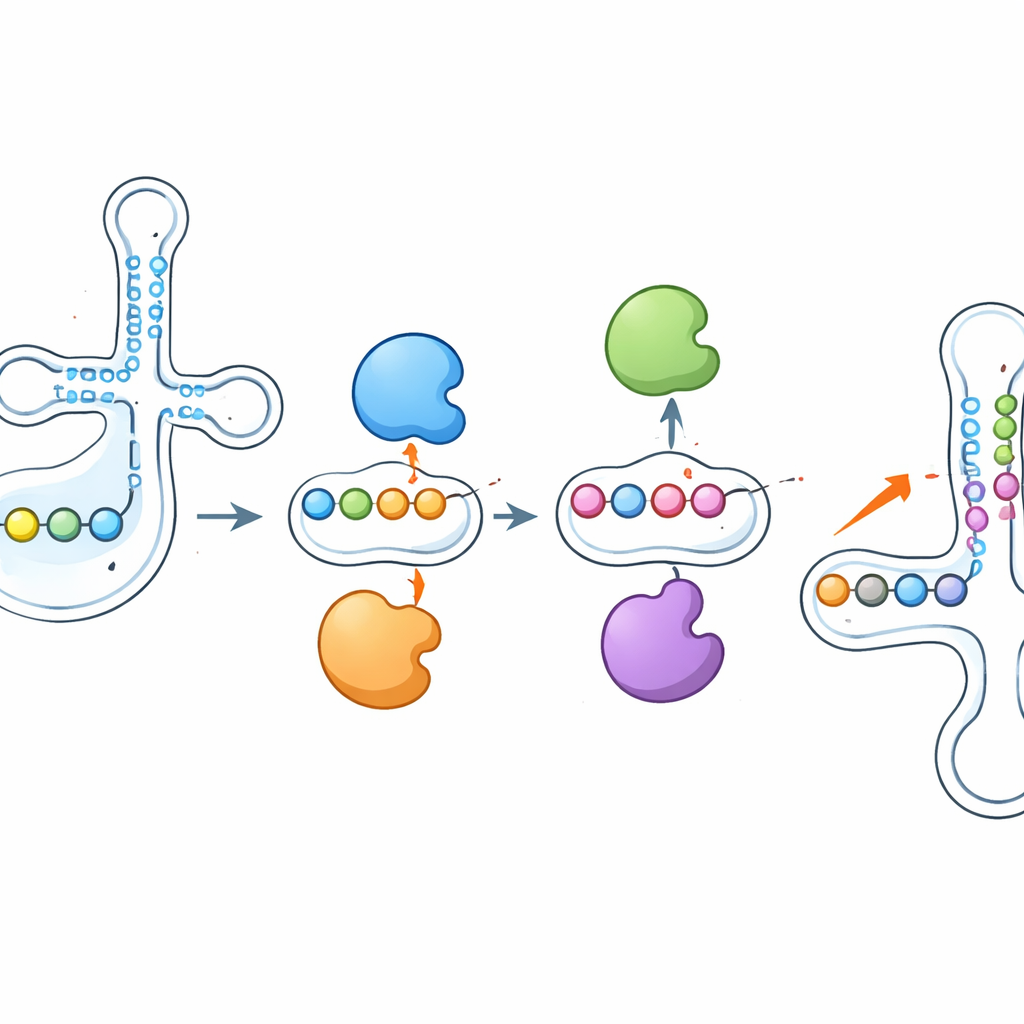
互いの働きを押し引きする酵素たち
最も注目すべき発見の一つは、これらの酵素が単独で作用するわけではないという点です。PUS1を欠損させると、通常アンチコドン近傍に付与されるプシウリジンは激減しましたが、同じtRNA上の近傍部位を修飾するRPUSD1やPUS7などの酵素による修飾が増加しました。逆にRPUSD1をノックアウトすると重なり合う位置で逆の変化が現れ、PUS7とPUS3の間でも類似したシーソー状のパターンが観察されました。これらの変化は酵素やtRNAの量の変動では説明できず、個々のtRNA分子レベルでの直接的な相互作用を示唆します。著者らは、酵素が近接する結合部位を物理的に競合しているか、あるいはプシウリジンの付加・除去が局所RNA構造を変え、近傍の部位を他の酵素に対してよりアクセスしやすくしたり難くしたりする可能性を提案しています。
健康と病気への意味
非専門家に向けた要点は、tRNA上の化学的印は固定された装飾ではなく、動的で相互に結びついたシステムの一部であるということです。複数の酵素が協働し競合してアンチコドン領域のパターンを作り出しており、この領域は遺伝コードを正確かつ柔軟に読み取る上で中心的な役割を果たします。これらの酵素のいくつかに変異が生じると、血液疾患や筋力低下、脳機能障害、がんなどのヒト疾患を引き起こすため、酵素間の標的共有や補償機構を理解することは、ある酵素の喪失が予想より軽度にとどまる理由や、ストレス下で細胞がどのように補償するかを解明する手がかりになります。本研究は小さなRNA上のプシウリジン出現の詳細な地図を提供し、これらの印を書き込む酵素が互いの活性を調節し得ることを示すことで、RNAに基づく欠陥を探り修正するための新たな出発点を示しています。
引用: Liu, W., Ma, Y., Wang, L. et al. Quantitative analysis of small RNA pseudouridylation reveals interplay of PUS enzymes in tRNA anticodon stem-loop. Nat Commun 17, 2811 (2026). https://doi.org/10.1038/s41467-026-69177-7
キーワード: tRNA修飾, ジヌクレオチド(プシウリジン), RNA酵素, ミトコンドリア機能, 翻訳制御