Clear Sky Science · pt
Análise quantitativa da pseudouridilação de pequenos RNAs revela interação entre enzimas PUS no loop de haste‑anticódon do tRNA
Por que marcas ocultas no RNA importam
Cada célula lê constantemente instruções genéticas usando pequenos RNAs que ajudam a montar proteínas e a processar outros RNAs. Este estudo examina um ajuste químico sutil nesses RNAs, chamado pseudouridina, que pode alterar seu comportamento sem mudar o código genético subjacente. Ao mapear exatamente onde essas modificações ocorrem e quais enzimas as colocam, os autores revelam uma "conversa" inesperada entre enzimas que ajustam finamente uma parte crucial da maquinaria de produção de proteínas.
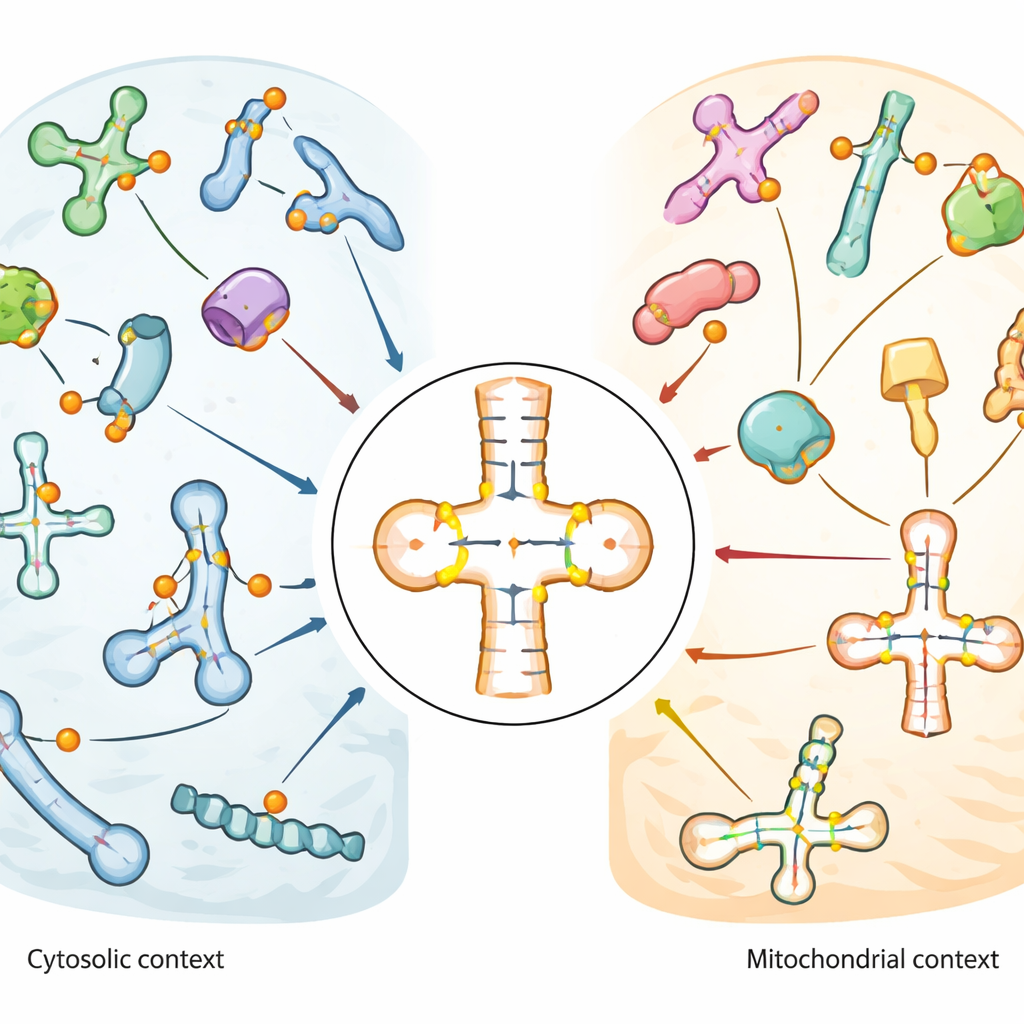
Edições químicas nos RNAs operários da célula
As células dependem de muitos tipos de pequenos RNAs, especialmente os RNAs de transferência (tRNAs), que atuam como adaptadores que leem palavras de três letras no código genético e entregam o aminoácido correto durante a síntese proteica. Esses tRNAs, junto com outros pequenos RNAs que guiam o processamento de RNA, são densamente decorados com modificações químicas. A pseudouridina é uma das mais comuns. Ela difere da uridina comum apenas na forma como seus átomos estão conectados, mas essa pequena mudança reforça o pareamento de bases e pode alterar a forma e a estabilidade do RNA. Como a pseudouridina está ligada a respostas ao estresse, função cerebral e câncer, os cientistas querem saber exatamente onde ela aparece e quais enzimas, chamadas pseudouridina sintetases ou enzimas PUS, são responsáveis.
Construindo um mapa preciso da pseudouridina
Métodos tradicionais podiam indicar muitos sítios de pseudouridina, mas tinham dificuldade em medir com que extensão cada sítio era modificado. Os pesquisadores refinaram um método químico‑de sequenciamento mais recente que haviam desenvolvido antes, chamado PRAISE, para torná‑lo quantitativo em pequenos RNAs. Primeiro trataram o RNA para remover outras modificações bloqueadoras, depois usaram uma reação especial de bisulfito e uma estratégia de sequenciamento que transforma a presença de pseudouridina em um sinal característico de deleção na leitura. Aplicando isso a células humanas HEK293T, geraram um panorama de alta resolução da pseudouridina em tRNAs citossólicos e mitocondriais, bem como em pequenos RNAs nucleares (snRNAs) e pequenos RNAs nucleolares (snoRNAs). O método mostrou‑se altamente reprodutível e igualou ou superou técnicas existentes, ao mesmo tempo em que acrescentou medições precisas dos níveis de modificação em cada posição.
Padrões distintos em diferentes bairros celulares
O mapa revelou que a pseudouridina está especialmente enriquecida no loop de haste‑anticódon dos tRNAs, a região que emparelha diretamente com o RNA mensageiro durante a tradução. Algumas posições, como um sítio praticamente universal próximo à base do tRNA (conhecido como posição 55), estavam quase totalmente modificadas em muitos tRNAs. Outras mostraram níveis moderados ou variáveis, sugerindo flexibilidade regulatória. Os tRNAs mitocondriais, que operam dentro das organelas produtoras de energia da célula, exibiram um padrão marcadamente diferente: sítios chave comuns em tRNAs citossólicos estavam ausentes ou fracamente modificados, enquanto outras posições próximas ao anticódon foram fortemente e consistentemente marcadas. Esse contraste implica que as mitocôndrias usam um conjunto distinto de regras de edição para seus próprios tRNAs. Em snRNAs e snoRNAs, a pseudouridina se concentrou em regiões funcionais que ajudam a guiar outras modificações de RNA ou o splicing, e alguns sítios mudaram em resposta a choque térmico ou estresse oxidativo.
Quem escreve as marcas: atribuição de enzimas a sítios
Para ligar enzimas específicas a sítios específicos de RNA, o grupo comparou células do tipo selvagem com uma série de linhagens celulares que faltavam enzimas PUS individuais ou com níveis reduzidos de uma enzima guia chamada DKC1. Eles mostraram que as marcas em snoRNAs provêm de duas rotas: uma via guiada por RNA usando DKC1 e uma enzima autônoma PUS7 que escreve um único sítio distintivo. Em tRNAs, atribuíram sistematicamente muitos sítios a enzimas particulares. PUS1 emergiu como um escritor importante de marcas próximas ao anticódon em tRNAs citossólicos e mitocondriais. Membros da família RluA dividiram suas funções: RPUSD1 modificou certos sítios em tRNAs citossólicos, incluindo um sítio próximo à cauda do tRNA anteriormente não reconhecido, enquanto RPUSD2 mirou posições próximas em tRNAs mitocondriais, e RPUSD3 não mostrou atividade detectável em tRNA. Enzimas relacionadas PUS1L e PUS7L especializaram‑se em regiões ou tipos de tRNA distintos, indicando que proteínas intimamente relacionadas podem evoluir tarefas surpreendentemente diferentes.
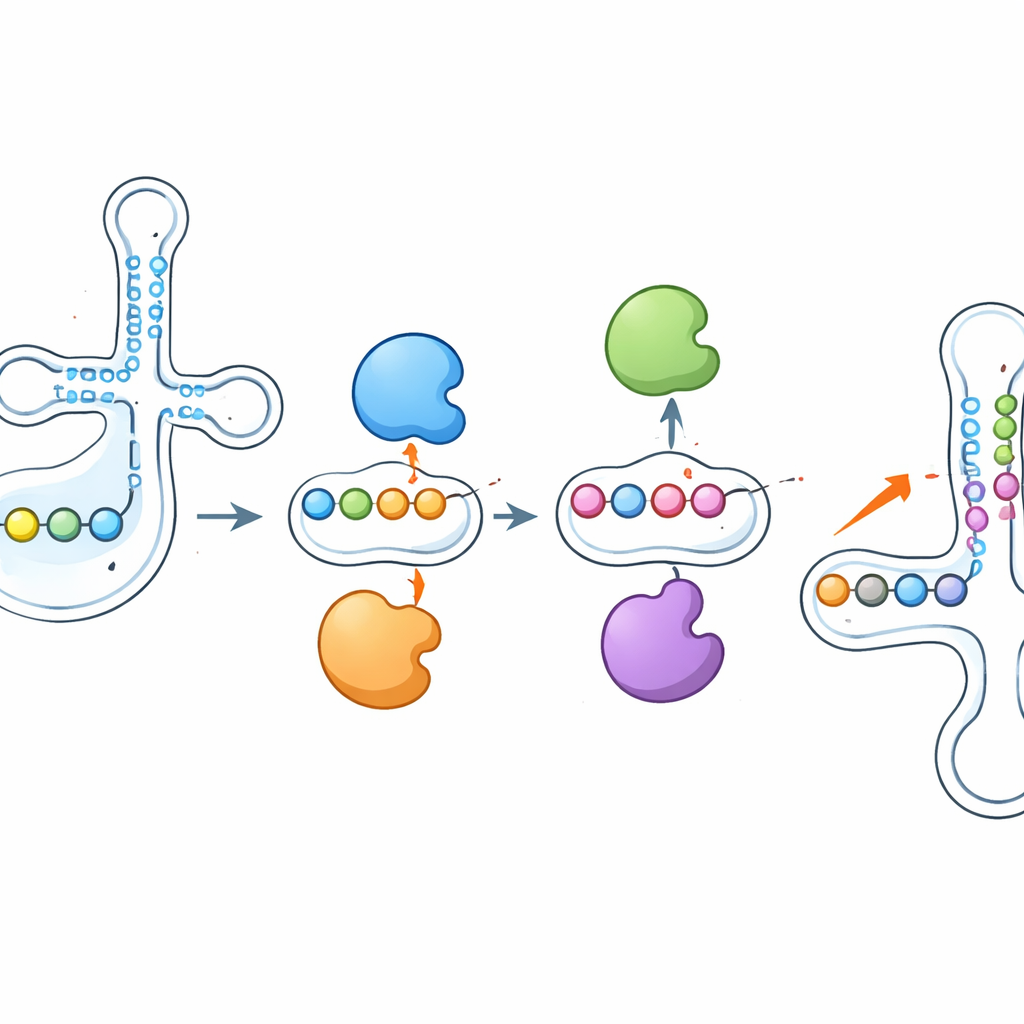
Enzimas que influenciam o trabalho umas das outras
Uma das descobertas mais marcantes foi que essas enzimas não atuam isoladamente. Quando os pesquisadores deletaram PUS1, as marcas de pseudouridina que ela normalmente instala perto do anticódon caíram acentuadamente — mas sítios vizinhos, escritos por outras enzimas como RPUSD1 ou PUS7, ficaram mais intensamente modificados no mesmo tRNA. A remoção de RPUSD1 produziu a imagem espelhada em posições sobrepostas, e padrões de gangorra semelhantes apareceram entre PUS7 e outra enzima, PUS3. Essas mudanças não foram explicadas por variações na abundância de enzimas ou de tRNA, apontando para uma interação direta ao nível de moléculas individuais de tRNA. Os autores sugerem que as enzimas podem competir fisicamente por sítios de ligação próximos ou que adicionar ou remover uma pseudouridina remodela a estrutura local do RNA, tornando posições vizinhas mais ou menos acessíveis a outras enzimas.
O que isso significa para saúde e doença
Para um leitor não especialista, a mensagem central é que as marcas químicas em tRNAs não são decorações fixas, mas parte de um sistema dinâmico e interconectado. Múltiplas enzimas colaboram e competem para padronizar a região do anticódon, que é central para ler o código genético com precisão e flexibilidade. Como mutações em várias dessas enzimas causam doenças humanas — desde desordens sanguíneas e fraqueza muscular até disfunção cerebral e câncer — entender como elas compartilham e ajustam seus alvos pode esclarecer por que a perda de uma enzima às vezes tem efeitos mais amenos do que o esperado, ou como as células se compensam sob estresse. Este estudo fornece um mapa detalhado de onde a pseudouridina aparece em pequenos RNAs e mostra que as enzimas que escrevem essas marcas podem modular a atividade umas das outras, oferecendo novos pontos de entrada para explorar e, eventualmente, corrigir defeitos baseados em RNA na saúde humana.
Citação: Liu, W., Ma, Y., Wang, L. et al. Quantitative analysis of small RNA pseudouridylation reveals interplay of PUS enzymes in tRNA anticodon stem-loop. Nat Commun 17, 2811 (2026). https://doi.org/10.1038/s41467-026-69177-7
Palavras-chave: modificações de tRNA, pseudouridina, enzimas de RNA, função mitocondrial, regulação da tradução