Clear Sky Science · nl
Kwantitatieve analyse van pseudouridylatie in klein RNA onthult interactie van PUS-enzymen in de anticodon-lus van tRNA
Waarom verborgen markeringen op RNA ertoe doen
Elke cel leest voortdurend genetische instructies met behulp van kleine RNA-moleculen die helpen bij de opbouw van eiwitten en de verwerking van andere RNA’s. Deze studie bekijkt een subtiele chemische aanpassing op deze RNA’s, pseudouridine genoemd, die hun gedrag kan veranderen zonder de onderliggende genetische code te wijzigen. Door precies in kaart te brengen waar deze aanpassingen voorkomen en welke enzymen ze aanbrengen, onthullen de auteurs een onverwachte "conversatie" tussen enzymen die een cruciaal deel van het eiwitproducerende apparaat fijnregelen.
Chemische bewerkingen op de werkpaarden van de cel
Cellen vertrouwen op vele soorten kleine RNA’s, met name transfer-RNA’s (tRNA’s), die fungeren als adaptermoleculen die drieletterwoorden in de genetische code lezen en het juiste aminozuur afleveren tijdens de eiwitsynthese. Deze tRNA’s, samen met andere kleine RNA’s die RNA-verwerking begeleiden, zijn rijkelijk voorzien van chemische modificaties. Pseudouridine is een van de meest voorkomende. Het verschilt van gewone uridine alleen in de manier waarop zijn atomen zijn verbonden, maar die kleine verandering versterkt basenparing en kan de vorm en stabiliteit van RNA beïnvloeden. Omdat pseudouridine gekoppeld is aan stressreacties, hersenfunctie en kanker, willen wetenschappers precies weten waar het voorkomt en welke enzymen, pseudouridine-synthetasen of PUS-enzymen, verantwoordelijk zijn.
Het bouwen van een precieze kaart van pseudouridine
Traditionele methoden konden veel pseudouridine-locaties aanwijzen maar hadden moeite om te meten in welke mate elke plek gemodificeerd was. De onderzoekers verfijnden een nieuwere chemische-veelvolgende methode die ze eerder ontwikkelden, PRAISE genoemd, zodat deze kwantitatief toegepast kon worden op kleine RNA’s. Ze behandelden RNA eerst om andere blokkade-modificaties te verwijderen, en gebruikten daarna een gespecialiseerde bisulfietreactie en sequencingstrategie die de aanwezigheid van pseudouridine omzet in een karakteristiek deletiesignaal in de leesuitkomst. Toegepast op menselijke HEK293T-cellen leverde dit een hoogresolutie-landschap van pseudouridine in zowel cytosolische als mitochondriale tRNA’s, evenals in kleine nucleaire RNA’s (snRNA’s) en kleine nucleolaire RNA’s (snoRNA’s). De methode bleek zeer reproduceerbaar en evenwaardig of beter dan bestaande technieken, terwijl ze bovendien precieze metingen van het modificatiepercentage op elke positie leverde.
Verschillende patronen in verschillende cellulaire buurten
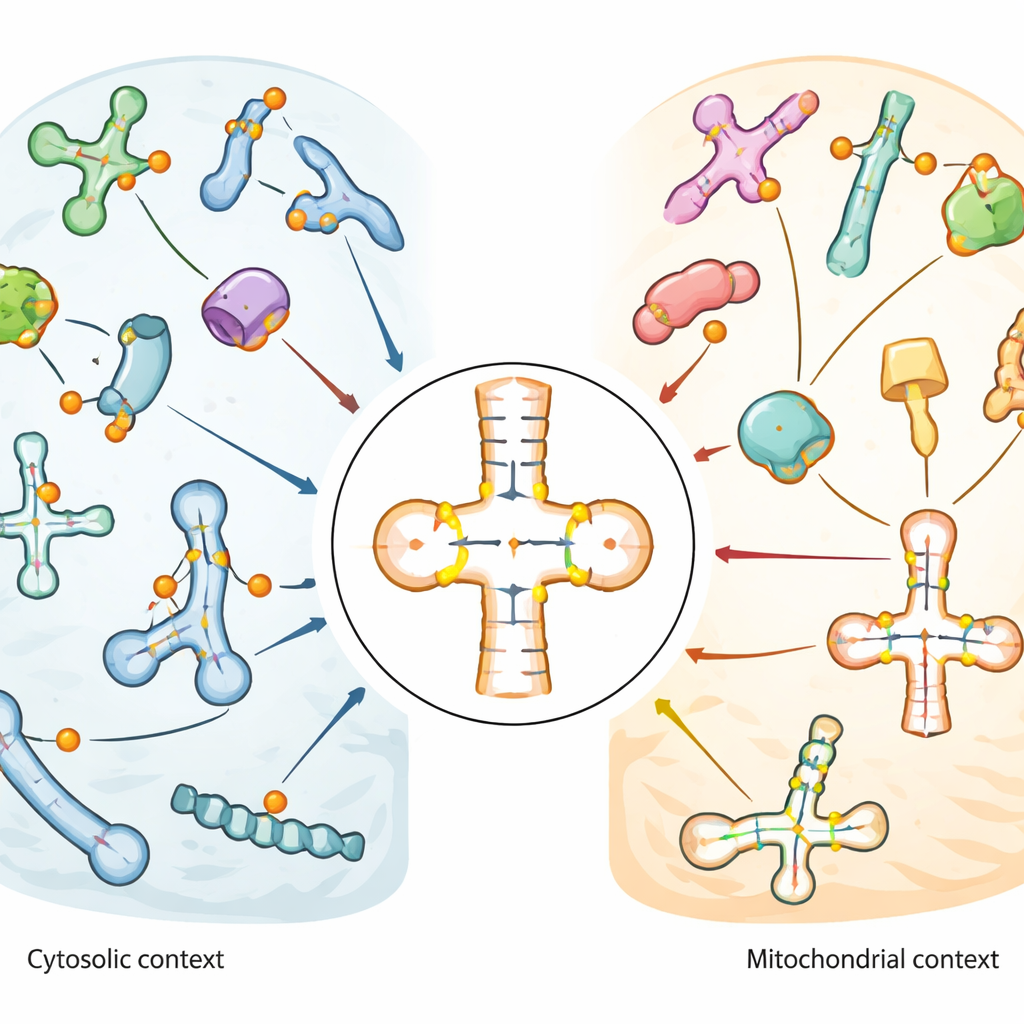
De kaart toonde aan dat pseudouridine sterk verrijkt is in de anticodon-stem-lus van tRNA’s, het gebied dat rechtstreeks paart met boodschapper-RNA tijdens de translatie. Sommige posities, zoals een universeel aanwezige plek nabij de basis van het tRNA (bekend als positie 55), waren bijna volledig gemodificeerd in veel tRNA’s. Andere lieten matige of variabele niveaus zien, wat wijst op regelgevende flexibiliteit. Mitochondriale tRNA’s, die binnen de energieproducerende organellen van de cel functioneren, vertoonden een duidelijk verschillend patroon: sleutelposities die gangbaar zijn in gewone (cytosolische) tRNA’s ontbraken of waren slechts zwak gemodificeerd, terwijl andere posities nabij het anticodon sterk en consistent gemarkeerd waren. Dit contrast suggereert dat mitochondriën een eigen set bewerkingsregels voor hun tRNA’s gebruiken. In snRNA’s en snoRNA’s clustered pseudouridine zich in functionele regio’s die andere RNA-modificaties of splicing sturen, en sommige sites veranderden als reactie op hitteschok of oxidatieve stress.
Wie schrijft de markeringen: enzymen toewijzen aan locaties
Om specifieke enzymen aan specifieke RNA-locaties te koppelen, vergeleek het team wildtype-cellen met een reeks cellijnen zonder individuele PUS-enzymen of met verlaagde niveaus van een gidsenzym genaamd DKC1. Ze toonden aan dat snoRNA-markeringen uit twee routes voortkomen: een RNA-geleid pad met DKC1 en een zelfstandige enzymroute met PUS7 die een enkel kenmerkend site schrijft. In tRNA’s wezen ze systematisch veel sites toe aan bepaalde enzymen. PUS1 bleek een belangrijke schrijver van markeringen nabij het anticodon in zowel cytosolische als mitochondriale tRNA’s. Leden van de RluA-familie verdeelden hun taken: RPUSD1 wijzigde bepaalde sites in cytosolische tRNA’s, inclusief een eerder onopgemerkte plek nabij de staart van het tRNA, terwijl RPUSD2 nabijgelegen posities in mitochondriale tRNA’s targette, en RPUSD3 geen detecteerbare tRNA-activiteit toonde. Verwante enzymen PUS1L en PUS7L bleken gespecialiseerd in verschillende regio’s of tRNA-typen, wat aangeeft dat nauw verwante eiwitten verrassend uiteenlopende taken kunnen ontwikkelen.
Enzymen die elkaars werk duwen en trekken
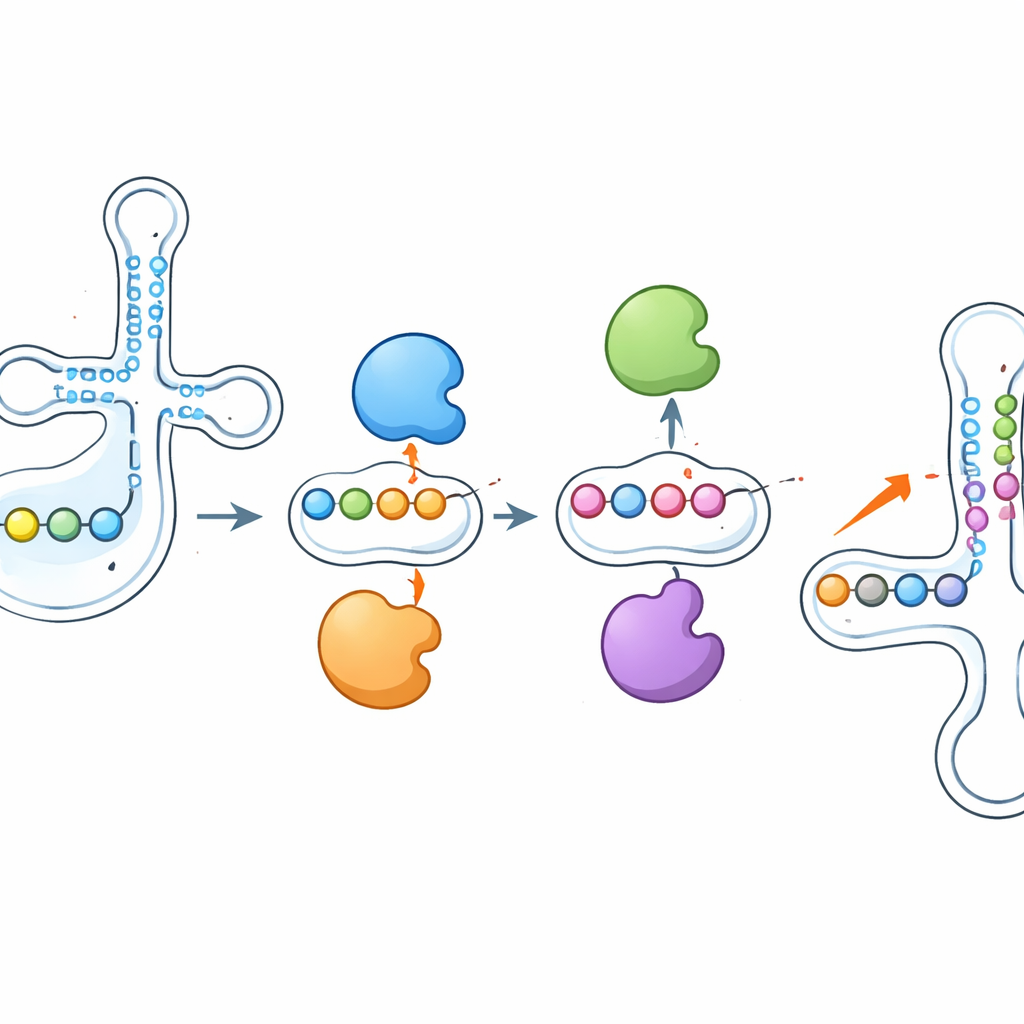
Een van de meest opvallende bevindingen was dat deze enzymen niet geïsoleerd werken. Wanneer de onderzoekers PUS1 verwijderden, daalden de pseudouridine-markeringen die het normaal bij het anticodon aanbrengt scherp—maar naburige sites, geschreven door andere enzymen zoals RPUSD1 of PUS7, werden op hetzelfde tRNA juist sterker gemodificeerd. Het uitzetten van RPUSD1 gaf het spiegelbeeld bij overlappende posities, en vergelijkbare schommelpatronen verschenen tussen PUS7 en een ander enzym, PUS3. Deze veranderingen konden niet verklaard worden door verschuivingen in enzym- of tRNA-hoeveelheid, wat wijst op een directe wisselwerking op het niveau van individuele tRNA-moleculen. De auteurs suggereren dat enzymen fysiek kunnen concurreren om nabijgelegen bindingsplaatsen, of dat het toevoegen of verwijderen van een pseudouridine de lokale RNA-structuur herschrijft, waardoor naburige posities voor andere enzymen makkelijker of moeilijker toegankelijk worden.
Wat dit betekent voor gezondheid en ziekte
Voor niet-specialisten is de kernboodschap dat de chemische markeringen op tRNA’s geen vaste versieringen zijn maar deel uitmaken van een dynamisch, onderling verbonden systeem. Meerdere enzymen werken samen en concurreren om het patroon in het anticodongebied te bepalen, dat centraal staat voor het nauwkeurig en flexibel uitlezen van de genetische code. Omdat mutaties in meerdere van deze enzymen menselijke ziekten veroorzaken—van bloedziekten en spierzwakte tot hersenfunctiestoornissen en kanker—kan inzicht in hoe ze hun doelen delen en aanpassen verklaren waarom het verlies van één enzym soms minder ernstige gevolgen heeft dan verwacht, of hoe cellen compenseren onder stress. Deze studie levert een gedetailleerde kaart van waar pseudouridine op kleine RNA’s voorkomt en toont aan dat de enzymen die deze markeringen schrijven elkaars activiteit kunnen moduleren, wat nieuwe aanknopingspunten biedt om RNA-gebaseerde defecten in de menselijke gezondheid te onderzoeken en mogelijk te corrigeren.
Bronvermelding: Liu, W., Ma, Y., Wang, L. et al. Quantitative analysis of small RNA pseudouridylation reveals interplay of PUS enzymes in tRNA anticodon stem-loop. Nat Commun 17, 2811 (2026). https://doi.org/10.1038/s41467-026-69177-7
Trefwoorden: tRNA-modificaties, pseudouridine, RNA-enzymen, mitochondriale functie, regulatie van translatie