Clear Sky Science · tr
LMO7 aracılı POLR2A yıkımı, MDM4/p53/p21 ekseni yoluyla hücresel senesansı teşvik eder
Yaşlanan hücreler neden önemli
İlerledikçe hücrelerimiz bölünme ve doku onarım yeteneklerini kademeli olarak kaybeder. Bu yıpranmış hücrelerin birçoğu ölmez; bunun yerine hücresel senesans adı verilen uzun süreli bir “uyku” durumuna girerler. Senesanslı hücreler, iltihaplı faktörler salgılayarak organları zayıflatabilir ve yaşa bağlı hastalıkları tetikleyebilir. Bu çalışma basit ama önemli bir soruyu gündeme getiriyor: sağlıklı bir hücreyi bu senesans durumuna ne geçirir — ve bu anahtarı kontrol etmek mümkün mü?
Hücrenin kopyalama odasındaki kilit bir işçi
Her hücre içinde RNA polimeraz II adı verilen büyük bir moleküler makine DNA’yı okur ve genlerin etkinleşmesine yardımcı olur. POLR2A bu makinenin en büyük ve en önemli parçasıdır. Önceki çalışmalar POLR2A düzeylerinin yaşlı dokularda ve erken yaşlanma bozukluklarında düştüğüne işaret etmişti, ancak bunun yaşlanmanın bir yan etkisi mi yoksa nedenlerinden biri mi olduğu bilinmiyordu. Yazarlar, deride ve akciğerde yaygın bir destek hücresi türü olan insan fibroblastlarını incelediler ve POLR2A’nın zamanla nasıl değiştiğini görmek için farklı yaşlardaki fare dokularına da baktılar.
Laboratuvarda hücrelerin yaşlandığını izlemek
Ekip, hücreleri bir kapta yaşlandırmak için iki yöntem kullandı. “Replikatif” yaşlanmada fibroblastlar doğal olarak yavaşlayana kadar arka arkaya bölünmelerine izin verildi. “Stres kaynaklı” yaşlanmada ise genç hücreler kısa süreli hidrojen peroksite maruz bırakıldı; bu, oksidatif hasara yol açar. Her iki modelde de giderek daha fazla hücre senansın klasik belirtilerini gösterdi: bölünmeyi bıraktılar, standart bir senesans belirteci için pozitif boyandılar ve iltihaplı moleküller salgıladılar. Çarpıcı biçimde, bu değişiklikler ortaya çıktıkça POLR2A protein düzeyleri keskin biçimde düştü; mRNA’sı düşmediği için bunun üretiminin azalmamasından çok proteinin yok edildiğini gösteriyordu. Benzer POLR2A düşüşleri yaşlı farelerin beyin, kalp ve akciğerlerinde de gözlendi; bu da süreci yaşayan hayvanlarda yaşlanmayla ilişkilendiriyordu.
POLR2A kaybı yaşlanma anahtarını nasıl çevirir
Neden‑etkiyi test etmek için araştırmacılar genç fibroblastlarda kasten POLR2A’yı düşürdüler. Hücreler hızla senesans özellikleri kazandı: bölünmeyi bıraktılar, senesans belirtecini açtılar ve iltihaplı sinyaller salgıladılar. Moleküler düzeyde, p53 proteini ve ortağı p21 etrafında kurulu iyi bilinen bir güvenlik yolu güçlü biçimde etkinleşti. POLR2A ve p53 birlikte baskılandığında hücreler büyük ölçüde senesanstan kaçındı; bu da POLR2A’nın normalde bu p53–p21 yolu üzerinden yaşlanmayı önlemeye yardımcı olduğunu gösteriyordu. Daha derinlemesine incelendiğinde, p53 seviyelerinin artmasının daha fazla p53 sentezlenmesinden değil, daha yavaş yıkılmasından kaynaklandığı bulundu. Genellikle p53’ü atılmak üzere etiketlemeye yardımcı olan MDM4 adlı bir protein, POLR2A azaldığında düştü; bu da p53’ün daha stabil olmasına ve hücre bölünmesini durdurma sinyallerinin güçlenmesine yol açtı.
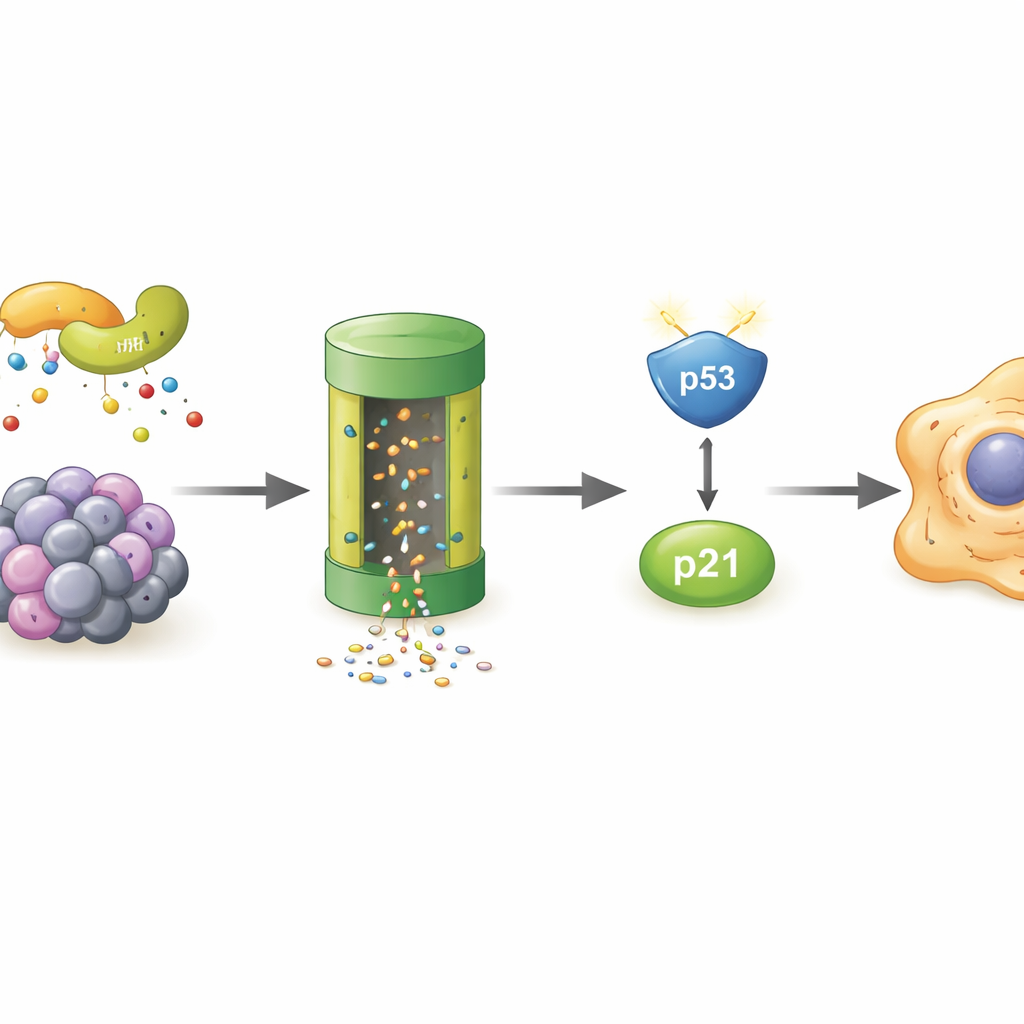
Yaşlanan hücrelerde POLR2A’yı kim yok ediyor
POLR2A’nın kendisi senesanslı hücrelerde daha hızlı kaybolduğundan, yazarlar sorumlu hücresel “çöp sistemi”ni aradılar. Proteinin ana öğütücüsü olan proteazomu engellemenin POLR2A düzeylerini kurtardığını ve POLR2A’nın yıkım için hedef proteinleri işaretleyen ubikitin etiketlerini daha fazla taşıdığını gösterdiler. Kütle spektrometrisi ekranı, bu etiketleri ekleyen enzim kompleksinin parçası olarak davranabilen bir iskelet proteini olan LMO7’yi öne çıkardı. Stres altındaki hücrelerde LMO7, POLR2A’ya daha güçlü bağlanıyordu. LMO7 kaldırıldığında POLR2A artık yoğun şekilde ubikitinlenmiyor ve düzeyleri oksidatif stres altında bile daha yüksek kalıyordu. Bu, LMO7’yi hücresel yaşlanma sırasında POLR2A kaybının merkezi sürücüsü olarak işaretledi.
Hücre içinde saati geri çevirmek
Son olarak araştırmacılar, POLR2A’yı artırmanın senesansa karşı koyup koymayacağını sordular. CRISPR aktivasyon teknolojisini kullanarak hücrenin kendi POLR2A genini nazikçe çalıştırdılar; yapay bir kopya eklemek yerine doğal ifadeyi yükselttiler. POLR2A düzeyi yükseltilmiş hücreler hem stres kaynaklı hem de replikatif senesansa karşı daha dirençliydi: daha az hücre senans belirteci için pozitif oldu ve daha çoğu bölünmeye devam etti. Aynı zamanda MDM4 düzeyleri daha yüksek kaldı ve p53–p21 yolu daha az aktiftir. Bu deney, POLR2A’yı korumanın hücreleri kalıcı yaşlı durumda bırakacak hasara karşı dayanıklı kılabileceğini düşündürüyor.
Sağlıklı yaşlanma için anlamı
Bulgular bir araya getirildiğinde yaşlanan hücreler içinde yeni bir olay zincirini ortaya koyuyor. Stres altında LMO7, POLR2A’yı yok edilmek üzere işaretliyor ve POLR2A protein düzeylerini düşürüyor. Bu da MDM4 üretimini azaltıyor, p53’ün birikmesine ve p21’i aktive etmesine izin veriyor; sonuçta hücreler senesans içinde kilitleniyor. POLR2A’yı yeniden sağlanabilir kılmanın bu zinciri kesebileceğini göstererek çalışma, LMO7–POLR2A–MDM4–p53–p21 yolunu doku yaşlanmasını geciktirmeyi veya zararlı senesanslı hücreleri temizlemeyi hedefleyen gelecekteki terapiler için potansiyel bir hedef olarak tanımlıyor. Herhangi bir tıbbi uygulama hâlâ uzak olsa da, bu içsel “yaşlanma anahtarını” anlamak, bilim insanlarını hücrelerimizin nasıl yaşlandığını yönetme yolunda bir adım daha ileriye taşıyor.
Atıf: Lai, C., Fu, W., Liu, J. et al. LMO7-mediated POLR2A degradation promotes cellular senescence through the MDM4/p53/p21 axis. Cell Death Dis 17, 421 (2026). https://doi.org/10.1038/s41419-026-08679-0
Anahtar kelimeler: hücresel senesans, yaşlanma, POLR2A, p53 yolu, ubikitinasyon