Clear Sky Science · fr
La dégradation de POLR2A médiée par LMO7 favorise la sénescence cellulaire via l’axe MDM4/p53/p21
Pourquoi les cellules âgées comptent
À mesure que nous vieillissons, nos cellules perdent progressivement leur capacité à se diviser et à réparer les tissus. Beaucoup de ces cellules usées ne meurent pas ; elles entrent plutôt dans un état de « sommeil » à long terme appelé sénescence cellulaire. Les cellules sénescentes peuvent affaiblir les organes et favoriser des maladies liées à l’âge en libérant des facteurs inflammatoires. Cette étude pose une question simple mais importante : qu’est‑ce qui fait basculer une cellule saine dans cet état sénescent — et ce commutateur peut‑il être contrôlé ?
Un acteur clé dans la salle de copie de la cellule
À l’intérieur de chaque cellule, une grande machinerie moléculaire appelée ARN polymérase II lit l’ADN et contribue à activer les gènes. POLR2A est la plus grande et la plus importante pièce de cette machinerie. Des travaux antérieurs laissaient entendre que les niveaux de POLR2A diminuent dans les tissus plus âgés et dans des troubles de vieillissement prématuré, mais on ignorait si cela était un effet secondaire du vieillissement ou faisait partie de sa cause. Les auteurs ont étudié des fibroblastes humains, un type courant de cellules de soutien dans la peau et les poumons, et ont aussi examiné des tissus de souris de différents âges pour suivre l’évolution de POLR2A dans le temps.
Observer le vieillissement cellulaire en laboratoire
L’équipe a utilisé deux méthodes pour faire vieillir des cellules en culture. Dans le vieillissement « réplicatif », les fibroblastes ont été simplement laissés se diviser de manière répétée jusqu’à ce qu’ils ralentissent naturellement. Dans le vieillissement « induit par le stress », des cellules jeunes ont été brièvement exposées au peroxyde d’hydrogène, qui provoque des dommages oxydatifs. Dans les deux modèles, un nombre croissant de cellules montraient les signes classiques de sénescence : elles cessaient de se diviser, étaient positives à un marqueur standard de sénescence et libéraient des molécules inflammatoires. De façon frappante, à mesure que ces changements apparaissaient, les niveaux de la protéine POLR2A chutaient fortement, alors que son ARN messager n’était pas réduit, indiquant que la protéine était détruite plutôt que moins synthétisée. Des déclins similaires de POLR2A ont été observés dans le cerveau, le cœur et les poumons de souris âgées, reliant ce processus au vieillissement chez l’animal vivant.
Comment la perte de POLR2A déclenche le commutateur du vieillissement
Pour tester la relation de cause à effet, les chercheurs ont délibérément réduit POLR2A dans des fibroblastes jeunes. Les cellules ont rapidement adopté un profil sénescent : elles ont arrêté de se diviser, ont activé le marqueur de sénescence et ont sécrété des signaux inflammatoires. Au niveau moléculaire, une voie de surveillance bien connue centrée sur la protéine p53 et son partenaire p21 est devenue fortement active. Lorsque POLR2A et p53 ont été diminués simultanément, les cellules ont en grande partie échappé à la sénescence, montrant que POLR2A empêche normalement le vieillissement via cette voie p53–p21. En creusant davantage, l’équipe a constaté que les niveaux de p53 augmentaient non parce que plus de p53 était produit, mais parce qu’il était dégradé plus lentement. Une protéine appelée MDM4, qui aide habituellement à marquer p53 pour son élimination, diminuait lorsque POLR2A chutait, entraînant une stabilisation de p53 et des signaux plus forts pour arrêter la division cellulaire.
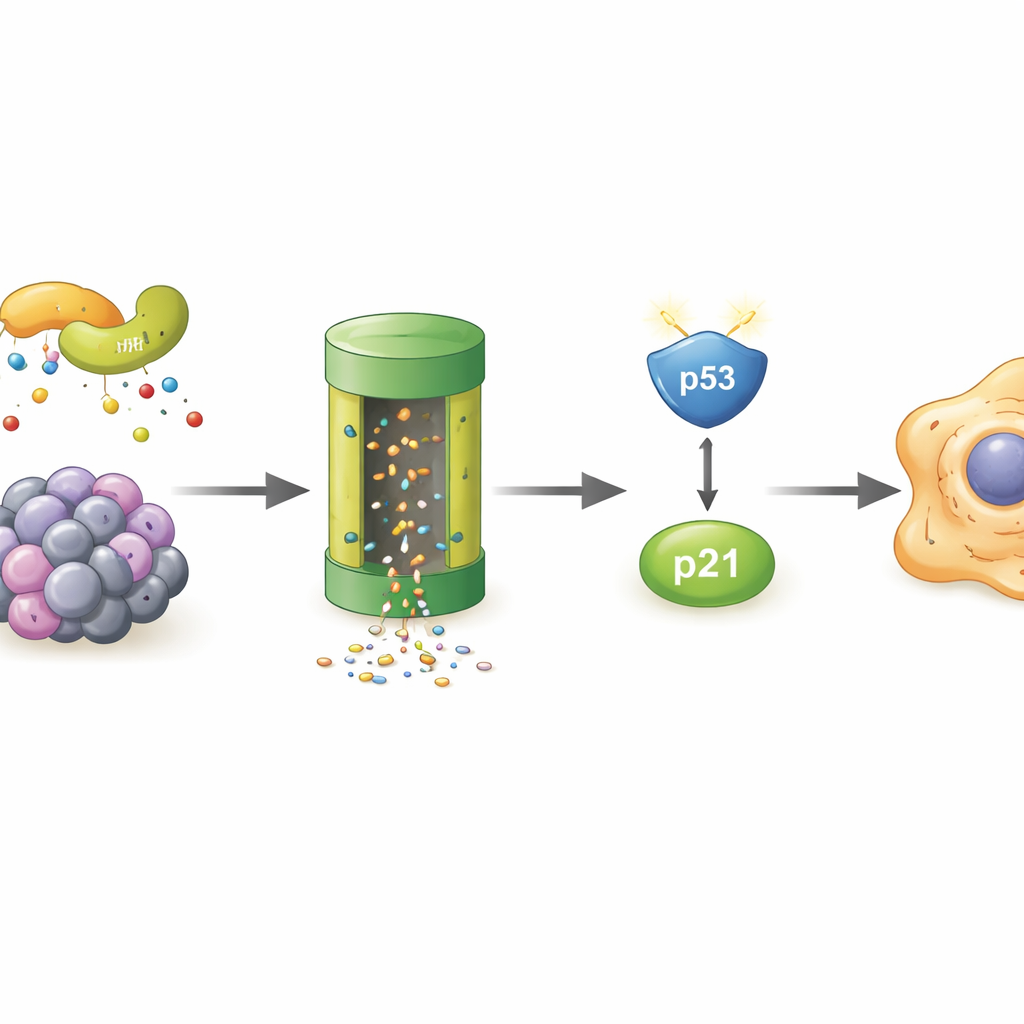
Qui détruit POLR2A dans les cellules vieillissantes
Puisque POLR2A disparaissait plus rapidement dans les cellules sénescentes, les auteurs ont cherché le « système d’élimination » responsable. Ils ont montré que bloquer le protéasome — le principal broyeur de protéines de la cellule — permettait de préserver les niveaux de POLR2A, et que POLR2A portait davantage d’étiquettes ubiquitine, des drapeaux moléculaires ciblant les protéines pour la destruction. Un criblage par spectrométrie de masse a mis en évidence LMO7, une protéine échafaudage qui peut agir dans un complexe enzymatique ajoutant ces marques. Dans les cellules stressées, LMO7 se liait plus fortement à POLR2A. Lorsque LMO7 était supprimée, POLR2A n’était plus fortement ubiquitinée et ses niveaux restaient plus élevés, même sous stress oxydatif. Cela identifie LMO7 comme un moteur central de la perte de POLR2A pendant le vieillissement cellulaire.
Rembobiner l’horloge à l’intérieur des cellules
Enfin, les chercheurs ont demandé si augmenter POLR2A pouvait repousser la sénescence. En utilisant une technologie d’activation par CRISPR, ils ont légèrement augmenté l’expression du gène POLR2A endogène plutôt que d’ajouter une copie artificielle. Les cellules avec POLR2A élevées résistaient mieux à la sénescence induite par le stress et à la sénescence réplicative : moins devenaient positives pour les marqueurs de sénescence et davantage continuaient à se diviser. Parallèlement, les niveaux de MDM4 restaient plus élevés et la voie p53–p21 était moins active. Cette expérience suggère que préserver POLR2A peut aider les cellules à supporter des dommages qui, autrement, les pousseraient vers un état âgé permanent.
Ce que cela signifie pour un vieillissement en bonne santé
Pris ensemble, ces résultats décrivent une nouvelle chaîne d’événements à l’intérieur des cellules vieillissantes. Sous stress, LMO7 marque POLR2A pour destruction, ce qui abaisse les niveaux de la protéine POLR2A. Cela réduit à son tour la production de MDM4, permettant à p53 de s’accumuler et d’activer p21, qui verrouille les cellules en sénescence. En montrant que la restauration de POLR2A peut interrompre cette chaîne, l’étude identifie la voie LMO7–POLR2A–MDM4–p53–p21 comme une cible potentielle pour de futures thérapies visant à retarder le vieillissement tissulaire ou à éliminer les cellules sénescentes nuisibles. Bien que toute application médicale soit encore lointaine, comprendre ce « commutateur du vieillissement » interne rapproche les scientifiques d’une gestion plus précise de la façon dont nos cellules vieillissent.
Citation: Lai, C., Fu, W., Liu, J. et al. LMO7-mediated POLR2A degradation promotes cellular senescence through the MDM4/p53/p21 axis. Cell Death Dis 17, 421 (2026). https://doi.org/10.1038/s41419-026-08679-0
Mots-clés: sénescence cellulaire, vieillissement, POLR2A, voie p53, ubiquitination