Clear Sky Science · es
La degradación de POLR2A mediada por LMO7 promueve la senescencia celular a través del eje MDM4/p53/p21
Por qué importan las células envejecidas
A medida que envejecemos, nuestras células van perdiendo gradualmente la capacidad de dividirse y reparar los tejidos. Muchas de estas células desgastadas no mueren; en su lugar, entran en un estado de “sueño” a largo plazo llamado senescencia celular. Las células senescentes pueden debilitar los órganos y promover enfermedades relacionadas con la edad mediante la liberación de factores inflamatorios. Este estudio plantea una pregunta sencilla pero importante: ¿qué hace que una célula sana se desplace hacia este estado senescente y se pueda controlar ese interruptor?
Un trabajador clave en la sala de copia de la célula
Dentro de cada célula, una gran máquina molecular llamada ARN polimerasa II lee el ADN y ayuda a activar los genes. POLR2A es la pieza más grande y más importante de esta máquina. Trabajos anteriores sugerían que los niveles de POLR2A disminuyen en tejidos envejecidos y en trastornos de envejecimiento prematuro, pero no estaba claro si esto era un efecto secundario del envejecimiento o parte de su causa. Los autores estudiaron fibroblastos humanos, un tipo común de células de sostén en la piel y el pulmón, y también examinaron tejidos de ratones de distintas edades para ver cómo cambia POLR2A con el tiempo.
Viendo cómo envejecen las células en el laboratorio
El equipo usó dos formas de inducir el envejecimiento celular en cultivo. En el envejecimiento «replicativo», los fibroblastos se dejaron dividir una y otra vez hasta que naturalmente se ralentizaron. En el envejecimiento «inducido por estrés», las células jóvenes se expusieron brevemente a peróxido de hidrógeno, que causa daño oxidativo. En ambos modelos, cada vez más células mostraron los signos clásicos de senescencia: dejaron de dividirse, dieron positivo en un marcador estándar de senescencia y liberaron moléculas inflamatorias. De forma llamativa, cuando aparecieron estos cambios, los niveles de proteína POLR2A cayeron bruscamente, aunque su ARNm no disminuyó, lo que indica que la proteína se estaba destruyendo en lugar de producirse menos. Descensos similares de POLR2A se observaron en cerebros, corazones y pulmones de ratones mayores, vinculando este proceso con el envejecimiento en animales vivos.
Cómo la pérdida de POLR2A cambia el interruptor del envejecimiento
Para probar causa y efecto, los investigadores redujeron deliberadamente POLR2A en fibroblastos jóvenes. Las células adoptaron rápidamente una identidad senescente: dejaron de dividirse, activaron el marcador de senescencia y secretaron señales inflamatorias. A nivel molecular, una conocida vía de control basada en la proteína p53 y su socia p21 se activó fuertemente. Cuando POLR2A y p53 se silenciaron juntos, las células escaparon en gran medida de la senescencia, lo que demuestra que POLR2A normalmente ayuda a prevenir el envejecimiento a través de esta vía p53–p21. Profundizando más, el equipo encontró que los niveles de p53 aumentaron no porque se produjera más p53, sino porque su degradación era más lenta. Una proteína llamada MDM4, que habitualmente ayuda a etiquetar a p53 para su eliminación, disminuyó cuando POLR2A cayó, conduciendo a un p53 más estable y a señales más intensas para detener la división celular.
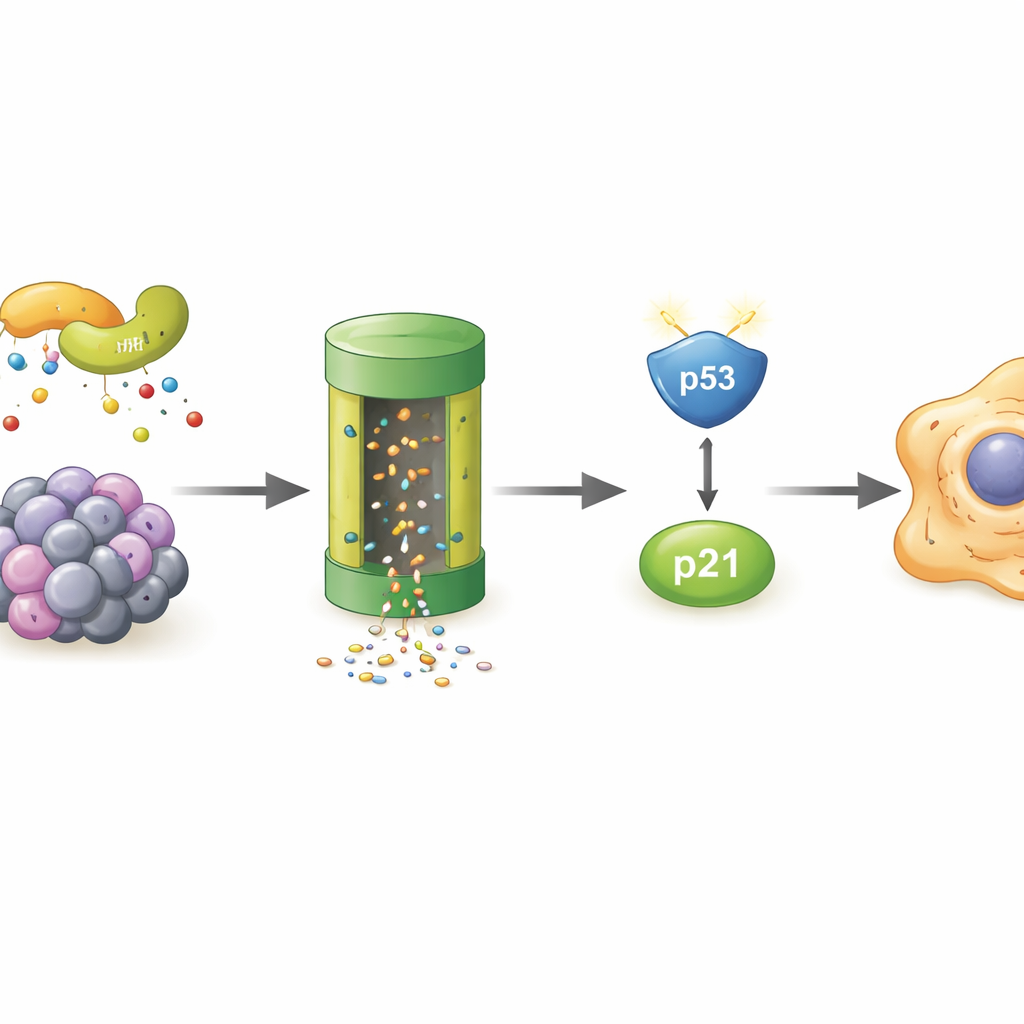
Quién destruye POLR2A en las células envejecidas
Dado que POLR2A desaparecía más rápido en las células senescentes, los autores buscaron el «sistema de basura» celular responsable. Mostraron que bloquear el proteasoma —la trituradora principal de proteínas de la célula— rescataba los niveles de POLR2A, y que POLR2A llevaba más etiquetas de ubiquitina, banderas moleculares que marcan proteínas para su destrucción. Una pantalla por espectrometría de masas destacó a LMO7, una proteína andamio que puede actuar como parte de un complejo enzimático que añade estas etiquetas. En células bajo estrés, LMO7 se unía con más fuerza a POLR2A. Cuando se eliminó LMO7, POLR2A dejó de recibir tantas etiquetas de ubiquitina y sus niveles se mantuvieron más altos, incluso bajo estrés oxidativo. Esto identificó a LMO7 como un impulsor central de la pérdida de POLR2A durante el envejecimiento celular.
Retroceder el reloj dentro de las células
Finalmente, los investigadores preguntaron si aumentar POLR2A podría contrarrestar la senescencia. Usando tecnología de activación CRISPR, aumentaron suavemente el propio gen POLR2A de la célula en lugar de añadir una copia artificial. Las células con POLR2A elevado fueron más resistentes tanto a la senescencia inducida por estrés como a la replicativa: menos células dieron positivo en marcadores de senescencia y más continuaron dividiéndose. Al mismo tiempo, los niveles de MDM4 se mantuvieron más altos y la vía p53–p21 estuvo menos activa. Este experimento sugiere que preservar POLR2A puede ayudar a las células a soportar daños que de otro modo las empujarían a un estado de envejecimiento permanente.
Qué significa esto para un envejecimiento saludable
En conjunto, los hallazgos trazan una nueva cadena de eventos dentro de las células envejecidas. Bajo estrés, LMO7 marca a POLR2A para su destrucción, disminuyendo los niveles de proteína POLR2A. Esto, a su vez, reduce la producción de MDM4, lo que permite que p53 se acumule y active a p21, que bloquea a las células en la senescencia. Al demostrar que restaurar POLR2A puede interrumpir esta cadena, el estudio identifica la vía LMO7–POLR2A–MDM4–p53–p21 como un posible objetivo para futuras terapias que busquen retrasar el envejecimiento de los tejidos o eliminar células senescentes dañinas. Aunque cualquier aplicación médica está todavía lejos, comprender este «interruptor del envejecimiento» interno acerca a los científicos un paso más a controlar cómo envejecen nuestras células.
Cita: Lai, C., Fu, W., Liu, J. et al. LMO7-mediated POLR2A degradation promotes cellular senescence through the MDM4/p53/p21 axis. Cell Death Dis 17, 421 (2026). https://doi.org/10.1038/s41419-026-08679-0
Palabras clave: senescencia celular, envejecimiento, POLR2A, vía p53, ubiquitinación