Clear Sky Science · ar
تدهور POLR2A بوساطة LMO7 يعزز شيخوخة الخلايا عبر محور MDM4/p53/p21
لماذا تهم الخلايا المسنة
مع تقدمنا في العمر، تفقد خلايانا تدريجياً قدرتها على الانقسام وإصلاح الأنسجة. العديد من هذه الخلايا المُهترِئة لا تموت؛ بل تدخل حالة «نوم» طويلة الأمد تُعرف بالشيخوخة الخلوية. يمكن للخلايا المسنة أن تضعف الأعضاء وتُحفِّز أمراضاً مرتبطة بالتقدم في السن عبر إفراز عوامل التهابية. يطرح هذا البحث سؤالاً بسيطاً لكنه مهم: ما الذي يدفع الخلية السليمة إلى الانزلاق إلى هذه الحالة المسنة—وهل يمكن التحكم في هذا المفتاح؟
عامل رئيسي في غرفة نسخ الخلية
داخل كل خلية توجد آلة جزيئية كبيرة تسمى بوليميراز الحمض الريبي النووي II تقرأ الحمض النووي وتساعد في تشغيل الجينات. POLR2A هو الجزء الأكبر والأهم في هذه الآلة. أشارت أعمال سابقة إلى أن مستويات POLR2A تنخفض في الأنسجة المسنة وفي اضطرابات الشيخوخة المبكرة، لكن لم يكن واضحاً ما إذا كان هذا أثرًا جانبيًا للشيخوخة أم جزءاً من سببها. درس الباحثون الأرومات الليفية البشرية، وهي نوع شائع من خلايا الدعامات في الجلد والرئة، ونظروا أيضاً إلى أنسجة من فئران بأعمار مختلفة ليتتبعوا كيف يتغير POLR2A مع الزمن.
مراقبة شيخوخة الخلايا في المختبر
استخدم الفريق طريقتين لجعل الخلايا تشيخ في طبق. في «الشيخوخة التكاثرية»، تُركت الأرومات الليفية لتتكرر وتقسم مراراً حتى تبطئ طبيعياً. في «الشيخوخة الناجمة عن الإجهاد»، تعرّضت الخلايا الشابة مؤقتاً لبيروكسيد الهيدروجين الذي يسبب ضرراً تأكسدياً. في كلا النموذجين، أظهرت خلايا أكثر فأكثر علامات معيارية للشيخوخة: توقفت عن الانقسام، وأظهرت صبغة إيجابية لمؤشر شائع للشيخوخة، وأفزرت جزيئات التهابية. ولافت للنظر، أنه مع ظهور هذه التغيرات انخفضت بشدة مستويات بروتين POLR2A، رغم أن مستوى رسالته المَرْسالَية لم يتغير، ما يشير إلى أن البروتين يُدمَّر بدلاً من أن يقل تصنيعه. لوحظت تراجعات مشابهة في POLR2A في أدمغة وقلوب ورئات الفئران المسنة، مما يربط هذه العملية بالشيخوخة في حيوانات حية.
كيف يؤدي فقدان POLR2A إلى قلب مفتاح الشيخوخة
لاختبار السببية، خفض الباحثون عمداً POLR2A في أرومات ليفية شابة. اكتسبت الخلايا هوية مسنة بسرعة: توقفت عن الانقسام، نشطت علامة الشيخوخة، وأفرزت إشارات التهابية. على المستوى الجزيئي، أصبح مسار الأمان المعروف المبني حول البروتين p53 وشريكه p21 نشطاً بشدة. عندما تم تثبيط POLR2A وp53 معاً، نجت الخلايا إلى حد كبير من الشيخوخة، مما يدل على أن POLR2A يساعد عادة في منع الشيخوخة عبر هذا المسار p53–p21. وبالتحري بعمق، وجد الفريق أن مستويات p53 ارتفعت ليس لأن تُصنَع منه كميات أكبر، بل لأن انهياره تباطأ. بروتين يدعى MDM4، الذي يساعد عادة في وسم p53 للتخلص منه، انخفض عندما هبط POLR2A، ما أدى إلى تراكم p53 وإطلاق إشارات أقوى لإيقاف انقسام الخلايا.
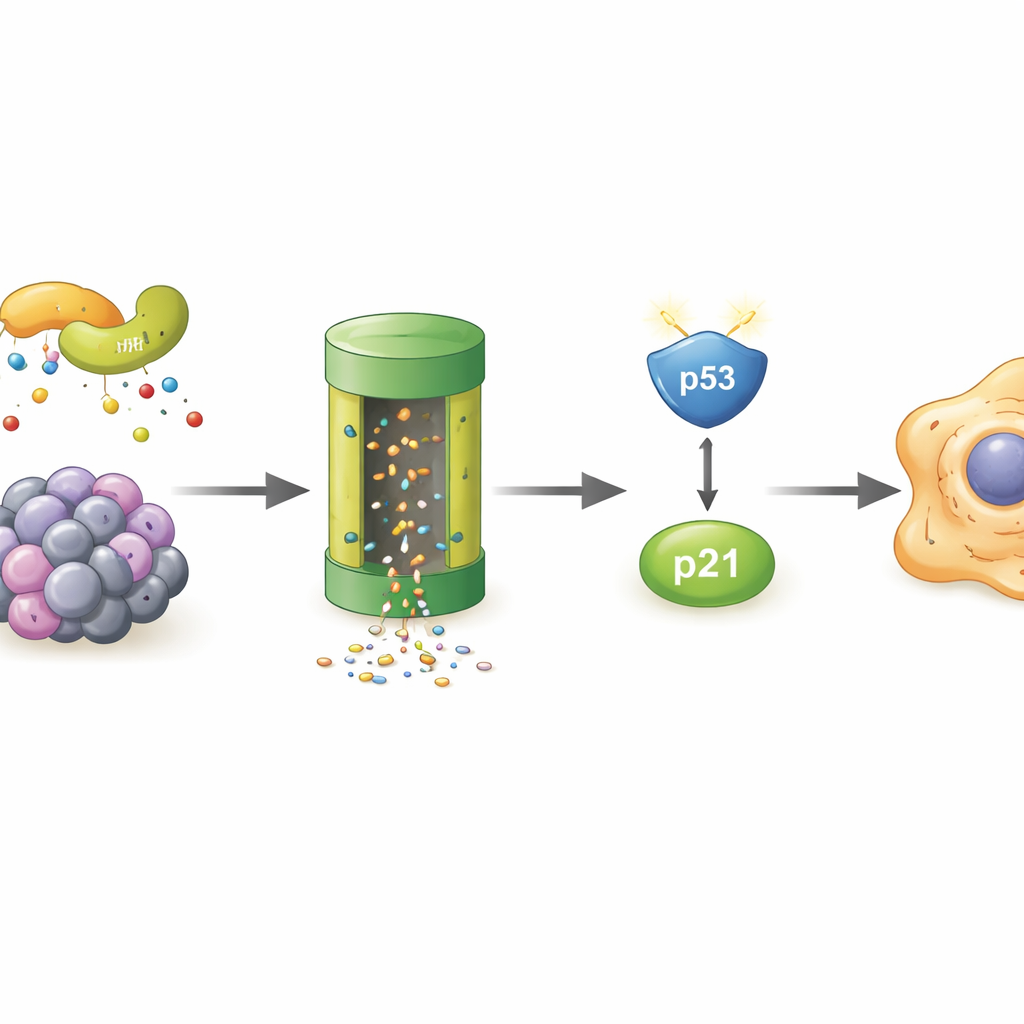
من يدمر POLR2A في الخلايا المسنة
بما أن POLR2A نفسه كان يختفي أسرع في الخلايا المسنة، بحث المؤلفون عن «نظام النفايات» الخلوي المسؤول. أظهروا أن حجب البروتيزوم—المفكك البروتيني الرئيسي في الخلية—أنقذ مستويات POLR2A، وأن POLR2A حمل علامات يوبكويتين وُضعت كأعلام جزيئية تستهدف البروتينات للتدمير. كشفت شاشة طيف الكتلة عن LMO7، بروتين حامل يعمل كجزء من معقد إنزيمي يضيف هذه العلامات في بعض الحالات. في الخلايا المتوترة، ثبت أن LMO7 ارتبط بقوة أكبر مع POLR2A. عندما أُزيل LMO7، لم يعد POLR2A يُوسم بكثرة باليوبكويتين وبقيت مستوياته أعلى، حتى تحت الإجهاد التأكسدي. هذا يحدد LMO7 كسائق مركزي لفقدان POLR2A أثناء شيخوخة الخلايا.
إرجاع الساعة داخل الخلايا
أخيراً، تساءل الباحثون عما إذا كان رفع POLR2A يمكن أن يردع الشيخوخة. باستخدام تكنولوجيا تنشيط CRISPR، قاموا برفع تعبير جين POLR2A الخاص بالخلية بلطف بدلاً من إدخال نسخة مصطنعة. كانت الخلايا ذات POLR2A المرتفع أكثر مقاومة لكل من الشيخوخة الناجمة عن الإجهاد والتكرار: أقل عدداً منها أظهر مؤشرات الشيخوخة، والمزيد واصل الانقسام. في الوقت نفسه، حافظت مستويات MDM4 على ارتفاعها وكان مسار p53–p21 أقل نشاطاً. يشير هذا التجريب إلى أن الحفاظ على POLR2A يمكن أن يساعد الخلايا على تحمل الضرر الذي قد يدفعها وإلا إلى حالة شيخوخة دائمة.
ما الذي يعنيه هذا لصحة الشيخوخة
تجمع النتائج معاً لتحدد سلسلة أحداث جديدة داخل الخلايا المسنة. تحت الإجهاد، يوسم LMO7 POLR2A للتدمير، مما يخفض مستويات بروتين POLR2A. هذا بدوره يقلل إنتاج MDM4، ما يسمح بتراكم p53 وتنشيط p21، الذي يقفل الخلايا في حالة الشيخوخة. من خلال إظهار أن استعادة POLR2A يمكن أن تقطع هذه السلسلة، تحدد الدراسة المسار LMO7–POLR2A–MDM4–p53–p21 كهدف محتمل لعلاجات مستقبلية تهدف إلى تأخير شيخوخة الأنسجة أو إزالة الخلايا المسنة الضارة. وبينما التطبيقات الطبية لا تزال بعيدة، فإن فهم هذا «مفتاح الشيخوخة» الداخلي يقرب العلماء خطوة من القدرة على إدارة كيفية شيخوخة خلايانا.
الاستشهاد: Lai, C., Fu, W., Liu, J. et al. LMO7-mediated POLR2A degradation promotes cellular senescence through the MDM4/p53/p21 axis. Cell Death Dis 17, 421 (2026). https://doi.org/10.1038/s41419-026-08679-0
الكلمات المفتاحية: شيخوخة الخلوية, الشيخوخة, POLR2A, مسار p53, اليوبيكويتيناسيون