Clear Sky Science · nl
LMO7-gemedieerde afbraak van POLR2A bevordert cellulaire veroudering via de MDM4/p53/p21-as
Waarom verouderende cellen ertoe doen
Naarmate we ouder worden, verliezen onze cellen geleidelijk hun vermogen om zich te delen en weefsels te herstellen. Veel van deze versleten cellen sterven niet; in plaats daarvan gaan ze in een langdurige "slaap"-toestand die cellulaire senescentie wordt genoemd. Senescente cellen kunnen organen verzwakken en leeftijdsgebonden ziekten bevorderen door ontstekingsfactoren vrij te geven. Deze studie stelt een eenvoudige maar belangrijke vraag: wat zorgt ervoor dat een gezonde cel omslaat naar deze senescente toestand — en kan die schakel worden bestuurd?
Een sleutelwerker in de kopieerkamer van de cel
In elke cel leest een groot moleculair apparaat, RNA-polymerase II, het DNA en helpt het genen aan te zetten. POLR2A is het grootste en belangrijkste deel van dit apparaat. Eerder onderzoek suggereerde dat POLR2A-niveaus afnemen in oudere weefsels en bij voortijdige verouderingsaandoeningen, maar men wist niet of dit een neveneffect van veroudering was of onderdeel van de oorzaak. De auteurs bestudeerden menselijke fibroblasten, een veelvoorkomend type ondersteunende cel in huid en longen, en keken ook naar weefsels van muizen van verschillende leeftijden om te zien hoe POLR2A in de loop van de tijd verandert.
Cellen in het lab oud zien worden
Het team gebruikte twee methoden om cellen in een schaaltje te laten verouderen. Bij "replicatieve" veroudering mochten fibroblasten zich eenvoudigweg keer op keer delen totdat ze natuurlijk vertraagden. Bij "stress-geïnduceerde" veroudering werden jonge cellen kort blootgesteld aan waterstofperoxide, wat oxidatieve schade veroorzaakt. In beide modellen vertoonde een groeiend aantal cellen klassieke kenmerken van senescentie: ze stopten met delen, kleurden positief voor een standaard senescentiemarker en gaven ontstekingsmoleculen af. Opvallend was dat, terwijl deze veranderingen optraden, POLR2A-proteïnespiegels sterk daalden, hoewel het mRNA niet daalde, wat aangeeft dat het eiwit werd afgebroken in plaats van minder vaak geproduceerd. Vergelijkbare afnames van POLR2A werden gezien in de hersenen, harten en longen van oudere muizen, wat dit proces koppelt aan veroudering in levende dieren.
Hoe het verlies van POLR2A de verouderingsschakel omzet
Om oorzaak en gevolg te testen, verlaagden de onderzoekers doelbewust POLR2A in jonge fibroblasten. De cellen namen snel een senescente identiteit aan: ze stopten met delen, schakelden de senescentiemarker aan en scheidden ontstekingssignalen uit. Op moleculair niveau werd een bekend bewakingspad rond het eiwit p53 en zijn partner p21 sterk geactiveerd. Toen POLR2A en p53 samen werden uitgeschakeld, ontkwamen de cellen grotendeels aan senescentie, wat laat zien dat POLR2A normaal gesproken helpt veroudering te voorkomen via deze p53–p21-route. Verder onderzoek bracht aan het licht dat de p53-niveaus stegen niet omdat er meer p53 werd gemaakt, maar omdat het langzamer werd afgebroken. Een eiwit genaamd MDM4, dat meestal helpt p53 voor verwijdering te markeren, daalde toen POLR2A afnam, wat leidde tot stabieler p53 en sterkere signalen om celdeling te stoppen.
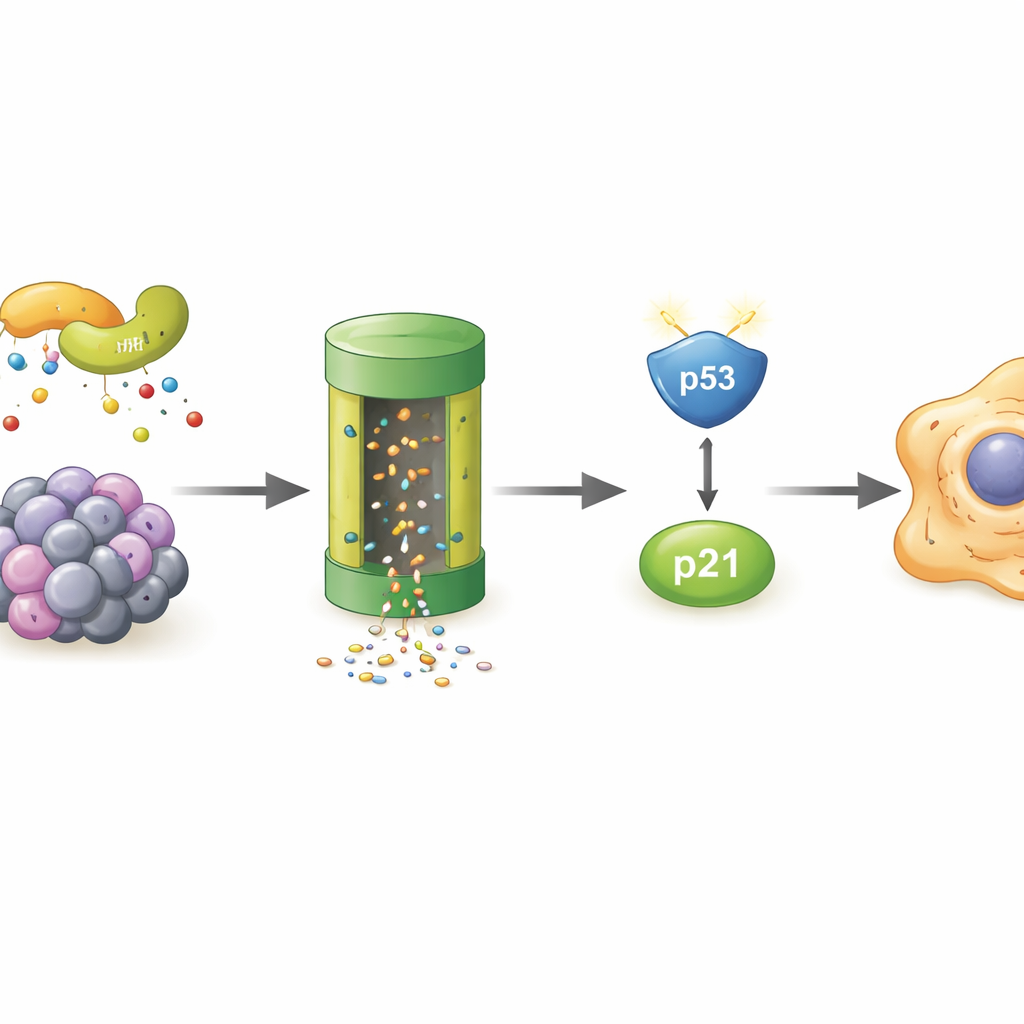
Wie POLR2A vernietigt in verouderende cellen
Aangezien POLR2A zelf sneller leek te verdwijnen in senescente cellen, zochten de auteurs naar het cellulair "afvalmechanisme" dat hiervoor verantwoordelijk is. Ze toonden aan dat het blokkeren van het proteasoom — de belangrijkste eiwitvermaler van de cel — POLR2A-niveaus redde, en dat POLR2A meer ubiquitine-tags droeg, moleculaire vlaggetjes die eiwitten naar vernietiging dirigeren. Een massaspectrometrie‑screen wees LMO7 aan, een scaffold-eiwit dat deel kan uitmaken van een enzymcomplex dat deze tags toevoegt. In gestreste cellen bond LMO7 sterker aan POLR2A. Toen LMO7 werd verwijderd, werd POLR2A niet langer sterk geubiquitineerd en bleven de niveaus hoger, zelfs onder oxidatieve stress. Dit wees LMO7 aan als een centrale aanjager van POLR2A‑verlies tijdens cellulaire veroudering.
De klok binnen cellen terugdraaien
Ten slotte vroegen de onderzoekers of het verhogen van POLR2A kon tegengaan dat cellen senescent werden. Met CRISPR-activatietechnologie zetten ze het eigen POLR2A-gen van de cel voorzichtig harder in plaats van een kunstmatige kopie toe te voegen. Cellen met verhoogde POLR2A waren beter bestand tegen zowel stress-geïnduceerde als replicatieve senescentie: minder werden positief voor senescentiemarkers en meer bleven zich delen. Tegelijkertijd bleven MDM4-niveaus hoger en was het p53–p21-pad minder actief. Dit experiment suggereert dat het behoud van POLR2A cellen kan helpen schade te weerstaan die hen anders in een permanente verouderde staat zou duwen.
Wat dit betekent voor gezond ouder worden
Samengevat schetsen de bevindingen een nieuwe keten van gebeurtenissen binnen verouderende cellen. Onder stress markeert LMO7 POLR2A voor afbraak, waardoor POLR2A-proteïneniveaus dalen. Dit verkleint op zijn beurt de productie van MDM4, waardoor p53 ophoopt en p21 activeert, wat cellen in senescentie vergrendelt. Door te laten zien dat het herstellen van POLR2A deze keten kan onderbreken, identificeert de studie de LMO7–POLR2A–MDM4–p53–p21-route als een potentiële doelstructuur voor toekomstige therapieën die erop gericht zijn weefselveroudering te vertragen of schadelijke senescente cellen te verwijderen. Hoewel geneeskundige toepassingen nog ver weg zijn, brengt het begrijpen van deze interne "verouderingsschakel" wetenschappers een stap dichter bij het beheersen van hoe onze cellen oud worden.
Bronvermelding: Lai, C., Fu, W., Liu, J. et al. LMO7-mediated POLR2A degradation promotes cellular senescence through the MDM4/p53/p21 axis. Cell Death Dis 17, 421 (2026). https://doi.org/10.1038/s41419-026-08679-0
Trefwoorden: cellulaire veroudering, veroudering, POLR2A, p53-route, ubiquitinylering