Clear Sky Science · ru
Разрушение POLR2A, опосредованное LMO7, способствует клеточному старению через ось MDM4/p53/p21
Почему клетки, стареющие, имеют значение
По мере нашего старения клетки постепенно теряют способность делиться и восстанавливать ткани. Многие из этих изношенных клеток не умирают; вместо этого они входят в длительное «спящее» состояние, называемое клеточным сенесценцией. Сенесцентные клетки ослабляют органы и способствуют возрастным заболеваниям, выделяя воспалительные факторы. В этом исследовании задают простой, но важный вопрос: что заставляет здоровую клетку перейти в сенесцентное состояние — и можно ли управлять этим переключателем?
Ключевой работник в цехе копирования клетки
Внутри каждой клетки крупный молекулярный аппарат, называемый РНК‑полимеразой II, считывает ДНК и помогает включать гены. POLR2A — самая крупная и важная часть этого аппарата. Предыдущие работы указывали, что уровни POLR2A снижаются в стареющих тканях и при синдромах преждевременного старения, но было неизвестно, является ли это побочным эффектом старения или его причиной. Авторы изучили человеческие фибробласты, распространённый тип поддерживающих клеток кожи и лёгких, а также исследовали ткани мышей разного возраста, чтобы проследить изменения POLR2A со временем.
Наблюдая за старением клеток в лаборатории
Команда использовала два подхода, чтобы вызвать старение клеток в чашке Петри. При «репликативном» старении фибробласты просто многократно делилиcь, пока их деление естественно не замедлилось. При «стресс‑индуцированном» старении молодые клетки кратковременно подвергали воздействию перекиси водорода, вызывающей окислительное повреждение. В обеих моделях всё больше клеток демонстрировало классические признаки сенесценции: они прекращали делиться, были положительны по стандартному маркеру сенесценции и выделяли воспалительные молекулы. Поразительно, что по мере появления этих изменений уровни белка POLR2A резко падали, хотя его мРНК не снижалась, что указывало на разрушение белка, а не на уменьшение синтеза. Аналогичные снижения POLR2A наблюдались в мозге, сердце и лёгких старых мышей, связывая этот процесс со старением в живом организме.
Как потеря POLR2A переключает механизм старения
Чтобы проверить причинно‑следственную связь, исследователи намеренно понижали уровень POLR2A в молодых фибробластах. Клетки быстро приобрели признаки сенесценции: прекратили делиться, активировали маркер старения и начали выделять воспалительные сигналы. На молекулярном уровне активировался известный защитный путь, опосредуемый белком p53 и его партнером p21. Когда одновременно понижали уровни POLR2A и p53, клетки в основном избегали сенесценции, что показывает: POLR2A обычно препятствует старению через путь p53–p21. При дальнейшем анализе команда обнаружила, что уровни p53 повышались не из‑за увеличенного синтеза, а из‑за замедленного разрушения. Белок MDM4, который обычно помогает помечать p53 для удаления, снижался при падении POLR2A, что приводило к более стабильному p53 и усилению сигналов остановки клеточного деления.
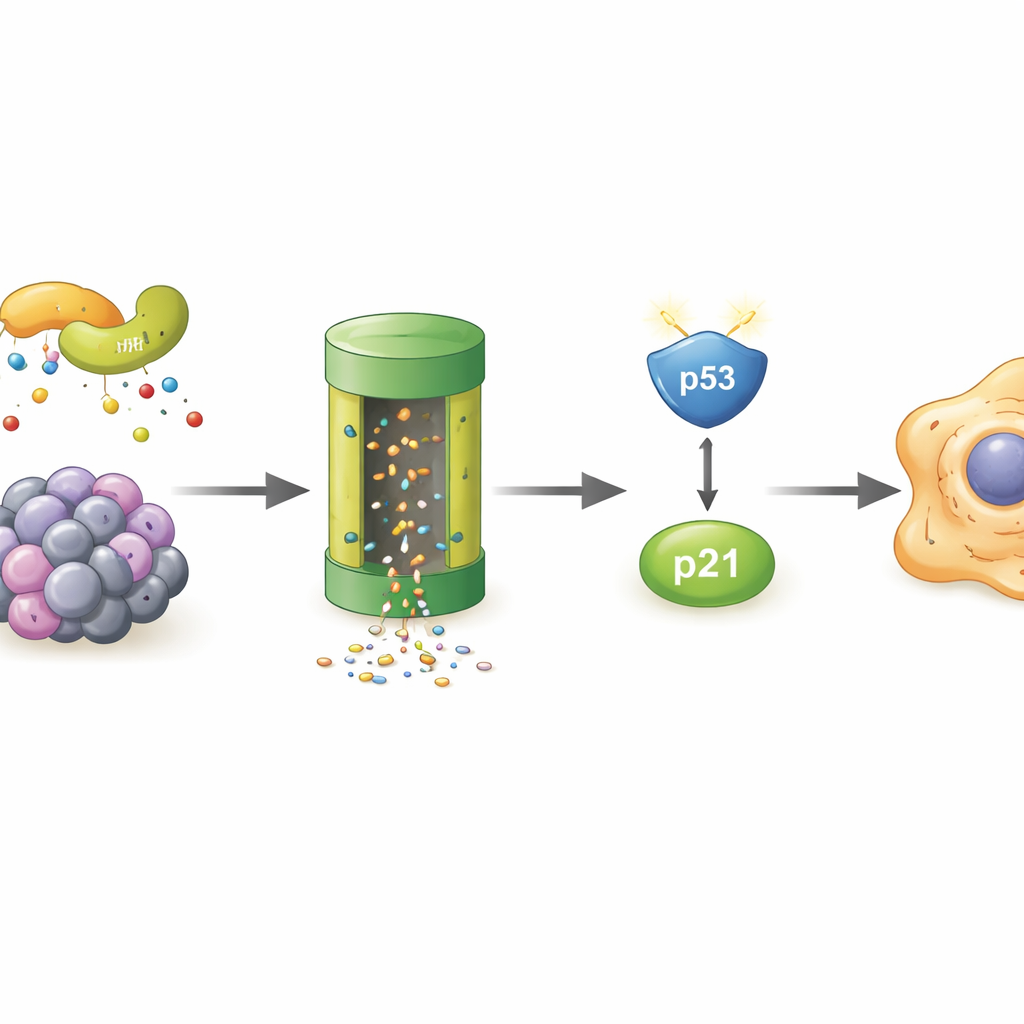
Кто уничтожает POLR2A в стареющих клетках
Поскольку сам POLR2A исчезал быстрее в сенесцентных клетках, авторы поискали клеточную «мусорную систему», ответственную за это. Они показали, что блокирование протеасомы — главного клеточного «шредера» белков — восстанавливало уровни POLR2A, и что на POLR2A появлялось больше меток убиквитина, молекулярных флагов, направляющих белки на разрушение. Скрининг методом масс‑спектрометрии выделил LMO7, штурмовой белок‑каркас, который может входить в состав комплекса ферментов, добавляющих эти метки. В стрессовых клетках LMO7 сильнее связывался с POLR2A. При удалении LMO7 POLR2A переставал интенсивно помечаться убиквитином и его уровни оставались выше, даже при окислительном стрессе. Это указывает на то, что LMO7 является центральным драйвером потери POLR2A в процессе клеточного старения.
Отматывание времени внутри клеток
Наконец, исследователи спросили, может ли повышение POLR2A противодействовать сенесценции. С помощью технологии активации CRISPR они аккуратно усилили собственный ген POLR2A клетки, а не вводили искусственную копию. Клетки с повышенным уровнем POLR2A были более устойчивы как к стресс‑индуцированной, так и к репликативной сенесценции: меньше клеток становились положительными по маркерам старения, и больше продолжали делиться. При этом уровни MDM4 оставались выше, а путь p53–p21 был менее активен. Этот эксперимент показывает, что сохранение POLR2A помогает клеткам противостоять повреждениям, которые в противном случае подтолкнули бы их в постоянное старое состояние.
Что это значит для здорового старения
В совокупности результаты очерчивают новую последовательность событий внутри стареющих клеток. Под воздействием стресса LMO7 помечает POLR2A для разрушения, что снижает уровни белка POLR2A. Это, в свою очередь, уменьшает производство MDM4, позволяя p53 накапливаться и активировать p21, который запирает клетки в состоянии сенесценции. Показав, что восстановление POLR2A может разорвать эту цепочку, исследование выделяет путь LMO7–POLR2A–MDM4–p53–p21 как потенциальную мишень для будущих терапий, направленных на замедление старения тканей или удаление вредных сенесцентных клеток. Хотя до медицинских приложений ещё далеко, понимание этого внутреннего «переключателя старения» приближает учёных к возможности управлять тем, как наши клетки стареют.
Цитирование: Lai, C., Fu, W., Liu, J. et al. LMO7-mediated POLR2A degradation promotes cellular senescence through the MDM4/p53/p21 axis. Cell Death Dis 17, 421 (2026). https://doi.org/10.1038/s41419-026-08679-0
Ключевые слова: клеточное старение, старение, POLR2A, путь p53, убиквитинирование