Clear Sky Science · ja
LMO7を介したPOLR2A分解はMDM4/p53/p21軸を通じて細胞老化を促進する
なぜ老化した細胞が重要なのか
年を重ねるにつれて、私たちの細胞は徐々に分裂や組織の修復能力を失います。これらの疲弊した細胞の多くは死ぬのではなく、長期の“休止”状態、すなわち細胞老化(セネッセンス)に入ります。老化細胞は炎症性因子を放出し、臓器の機能を低下させ、加齢関連疾患を促進します。本研究は単純だが重要な問いを立てます:健康な細胞がどのようにしてこの老化状態へ傾くのか、そしてそのスイッチは制御できるのか?
細胞のコピー室で働く重要な役割分子
すべての細胞内にはRNAポリメラーゼIIと呼ばれる大きな分子機械があり、DNAを読み取って遺伝子の発現を助けます。POLR2Aはこの機械の最大かつ最も重要な構成要素です。以前の研究は、POLR2Aの量が高齢組織や早老症で低下することを示唆していましたが、それが老化の副産物なのか原因の一部なのかは明らかではありませんでした。著者らはヒト線維芽細胞(皮膚や肺で一般的な支持細胞)を調べ、さらに年齢の異なるマウスの組織も調べて、POLR2Aが時間とともにどのように変化するかを解析しました。
培養で細胞の老化を観察する
チームは培養皿内で細胞を老化させる二つの方法を使いました。「複製性」老化では、線維芽細胞を繰り返し分裂させ、自然に増殖が遅くなるまで培養しました。「ストレス誘導」老化では、若い細胞を短時間過酸化水素にさらして酸化的損傷を与えました。どちらのモデルでも、ますます多くの細胞が古典的な老化の兆候を示しました:分裂を停止し、標準的な老化マーカーで陽性となり、炎症性分子を分泌しました。注目すべきは、これらの変化が現れると同時にPOLR2Aタンパク質量が急激に低下したことです。一方でそのmRNA量は減っておらず、つまりタンパク質が作られなくなったのではなく、分解されていることを示していました。同様のPOLR2A減少は高齢マウスの脳、心臓、肺でも観察され、この過程が生体内の老化に結びつくことを示しました。
POLR2Aの喪失が老化スイッチをどう切るか
因果関係を確かめるため、研究者らは若い線維芽細胞で意図的にPOLR2Aを低下させました。すると細胞は速やかに老化した性質を示しました:分裂をやめ、老化マーカーが発現し、炎症性シグナルを分泌しました。分子レベルでは、p53とそのパートナーp21を中心としたよく知られた安全装置経路が強く活性化しました。POLR2Aとp53を同時に低下させると、細胞は主に老化を免れたため、POLR2Aは通常このp53–p21経路を通じて老化を抑えていることが示されました。さらに掘り下げると、p53量の上昇はp53の合成が増えたためではなく、その分解が遅くなったためであることがわかりました。通常p53の廃棄に関与するMDM4というタンパク質が、POLR2Aが減ると低下し、その結果p53が安定化して細胞分裂停止へのシグナルが強まることが明らかになりました。
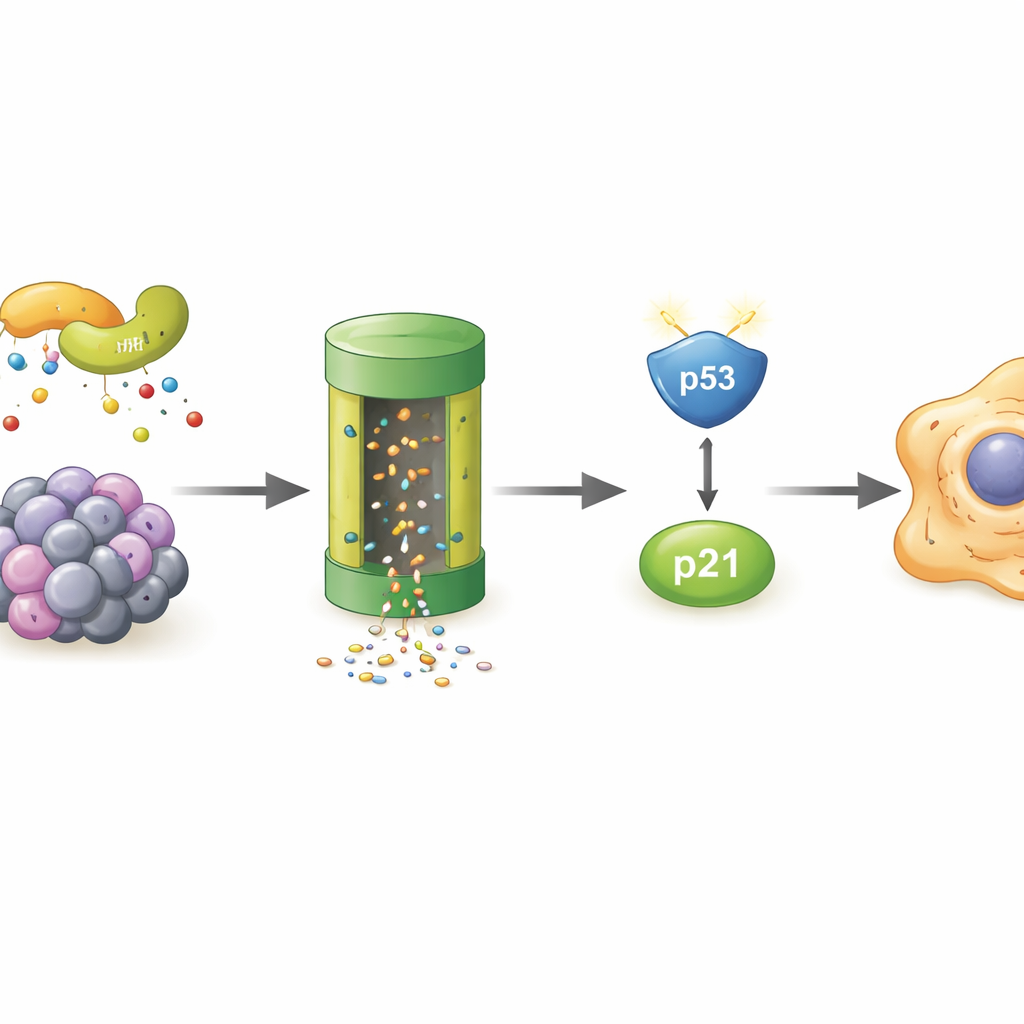
老化細胞でPOLR2Aを破壊するのは誰か
老化細胞でPOLR2A自身がより速く消失していたため、著者らはどの細胞の“廃棄システム”が関与しているかを探索しました。彼らはプロテアソーム(細胞の主要なタンパク質分解装置)を阻害するとPOLR2A量が回復すること、そしてPOLR2Aにユビキチンタグがより多く付いていることを示しました。質量分析スクリーニングにより、これらのタグ付けを行う酵素複合体の一部として作用しうる足場タンパク質LMO7が候補として挙がりました。ストレス下でLMO7はPOLR2Aにより強く結合しました。LMO7を除去すると、POLR2Aへのユビキチン付加が著しく減り、酸化ストレス下でもPOLR2A量は高く保たれました。これによりLMO7が細胞老化時のPOLR2A喪失の中心的駆動因子であることが示されました。
細胞内の時計を戻す
最後に、研究者らはPOLR2Aを増やすことで老化に対抗できるかを調べました。彼らは人工的なコピーを導入するのではなく、CRISPR活性化技術を用いて細胞自身のPOLR2A遺伝子の発現を穏やかに上げました。POLR2Aが高められた細胞は、ストレス誘導および複製性の両方の老化に対してより耐性を示しました:老化マーカー陽性になる細胞が減り、より多くが分裂を続けました。同時にMDM4量は高く保たれ、p53–p21経路の活性化は抑えられました。この実験は、POLR2Aを保持することが細胞を恒久的な老化状態へと追い込む損傷に対して耐性を与えうることを示唆します。
健康な老化にとっての意義
総じて、本研究は老化細胞内部の新たな一連の出来事を描き出します。ストレス下でLMO7がPOLR2Aに破壊の標を付け、POLR2Aタンパク質量を低下させます。これがMDM4の産生を減らし、p53が蓄積してp21を活性化し、細胞を老化に固定します。POLR2Aを回復させることでこの連鎖を断ち切れることを示したことで、LMO7–POLR2A–MDM4–p53–p21経路は組織の老化を遅らせるか有害な老化細胞を除去する将来の治療標的として注目されます。医療応用にはまだ時間がかかりますが、この内部の“老化スイッチ”を理解することで、科学者たちは細胞の老い方を管理する一歩を踏み出しました。
引用: Lai, C., Fu, W., Liu, J. et al. LMO7-mediated POLR2A degradation promotes cellular senescence through the MDM4/p53/p21 axis. Cell Death Dis 17, 421 (2026). https://doi.org/10.1038/s41419-026-08679-0
キーワード: 細胞老化, 老化, POLR2A, p53経路, ユビキチン化