Clear Sky Science · pt
A degradação de POLR2A mediada por LMO7 promove a senescência celular através do eixo MDM4/p53/p21
Por que as células envelhecidas importam
À medida que envelhecemos, nossas células perdem gradualmente a capacidade de se dividir e reparar tecidos. Muitas dessas células desgastadas não morrem; em vez disso, entram em um estado de “sono” prolongado chamado senescência celular. Células senescentes podem enfraquecer órgãos e impulsionar doenças relacionadas à idade ao liberarem fatores inflamatórios. Este estudo faz uma pergunta simples, porém importante: o que faz uma célula saudável pender para esse estado senescente — e esse interruptor pode ser controlado?
Um trabalhador-chave na sala de cópia da célula
Dentro de cada célula, uma grande máquina molecular chamada RNA polimerase II lê o DNA e ajuda a ativar genes. POLR2A é a maior e mais importante peça dessa máquina. Trabalhos anteriores sugeriram que os níveis de POLR2A caem em tecidos envelhecidos e em doenças de envelhecimento prematuro, mas ninguém sabia se isso era um efeito colateral do envelhecimento ou parte da causa. Os autores estudaram fibroblastos humanos, um tipo comum de célula de suporte na pele e no pulmão, e também examinaram tecidos de camundongos de diferentes idades para ver como o POLR2A muda ao longo do tempo.
Observando células envelhecerem no laboratório
A equipe usou duas maneiras de induzir envelhecimento de células em cultura. No envelhecimento “reprodutivo”, os fibroblastos foram simplesmente deixados dividir repetidamente até que naturalmente desacelerassem. No envelhecimento “induzido por estresse”, células jovens foram brevemente expostas a peróxido de hidrogênio, que causa dano oxidativo. Em ambos os modelos, cada vez mais células exibiram características clássicas da senescência: deixaram de se dividir, coraram positivamente para um marcador padrão de senescência e liberaram moléculas inflamatórias. De forma notável, à medida que essas mudanças surgiam, os níveis da proteína POLR2A caíam bruscamente, embora seu mRNA não tenha diminuído, indicando que a proteína estava sendo degradada em vez de ser menos produzida. Quedas semelhantes em POLR2A foram vistas nos cérebros, corações e pulmões de camundongos mais velhos, ligando esse processo ao envelhecimento em animais vivos.
Como a perda de POLR2A vira o interruptor de envelhecimento
Para testar causa e efeito, os pesquisadores reduziram deliberadamente o POLR2A em fibroblastos jovens. As células rapidamente adotaram uma identidade senescente: pararam de se dividir, acionaram o marcador de senescência e secretaram sinais inflamatórios. Em nível molecular, uma via de controle bem conhecida centrada na proteína p53 e sua parceira p21 tornou-se altamente ativa. Quando POLR2A e p53 foram silenciados juntos, as células em grande parte escaparam da senescência, mostrando que o POLR2A normalmente ajuda a prevenir o envelhecimento por meio dessa via p53–p21. Indo mais a fundo, a equipe descobriu que os níveis de p53 aumentaram não porque mais p53 foi produzido, mas porque sua degradação diminuiu. Uma proteína chamada MDM4, que normalmente ajuda a marcar o p53 para eliminação, caiu quando POLR2A diminuiu, levando a um p53 mais estável e a sinais mais fortes para interromper a divisão celular.
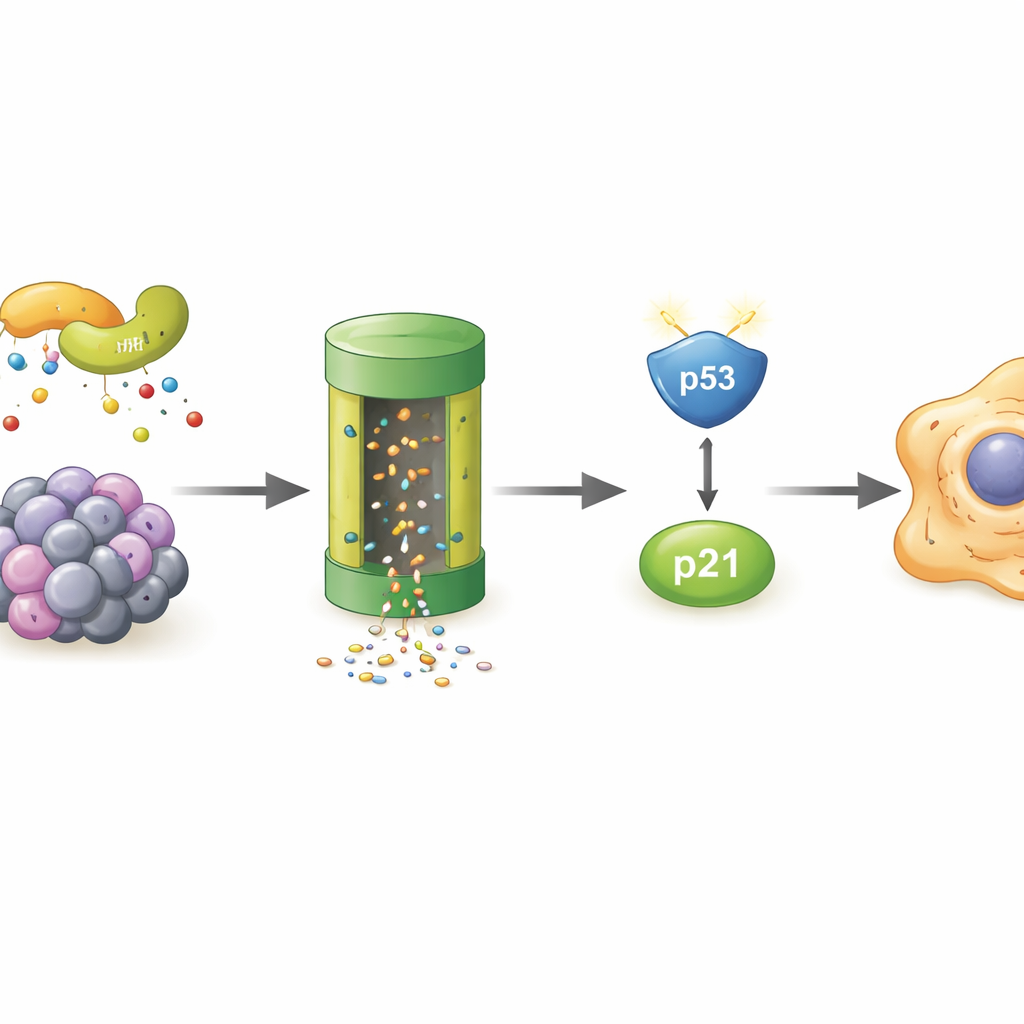
Quem destrói o POLR2A nas células envelhecidas
Visto que o próprio POLR2A estava desaparecendo mais rapidamente em células senescentes, os autores buscaram o “sistema de lixo” celular responsável. Eles mostraram que bloquear o proteassoma — o principal triturador de proteínas da célula — resgatou os níveis de POLR2A, e que POLR2A carregava mais marcas de ubiquitina, bandeiras moleculares que direcionam proteínas para destruição. Uma triagem por espectrometria de massa destacou LMO7, uma proteína scaffolding que pode atuar como parte de um complexo enzimático que adiciona essas marcas. Em células estressadas, LMO7 ligou-se com mais afinidade ao POLR2A. Quando LMO7 foi removido, POLR2A deixou de ser fortemente ubiquitinado e seus níveis permaneceram mais altos, mesmo sob estresse oxidativo. Isso apontou LMO7 como um motor central da perda de POLR2A durante o envelhecimento celular.
Virando o relógio dentro das células
Finalmente, os pesquisadores investigaram se aumentar o POLR2A poderia reverter a senescência. Usando tecnologia de ativação CRISPR, eles aumentaram suavemente o gene endógeno POLR2A em vez de adicionar uma cópia artificial. Células com POLR2A elevado foram mais resistentes tanto à senescência induzida por estresse quanto à reprodutiva: menos se tornaram positivas para marcadores de senescência e mais continuaram a se dividir. Ao mesmo tempo, os níveis de MDM4 permaneceram mais altos e a via p53–p21 ficou menos ativa. Esse experimento sugere que preservar POLR2A pode ajudar as células a suportar danos que, de outra forma, as empurrariam para um estado permanente de envelhecimento.
O que isso significa para um envelhecimento saudável
Em conjunto, os achados delineiam uma nova cadeia de eventos dentro das células envelhecidas. Sob estresse, LMO7 marca o POLR2A para destruição, reduzindo os níveis da proteína POLR2A. Isso, por sua vez, diminui a produção de MDM4, permitindo que p53 se acumule e ative p21, que tranca as células na senescência. Ao mostrar que restaurar POLR2A pode interromper essa cadeia, o estudo identifica a via LMO7–POLR2A–MDM4–p53–p21 como um alvo potencial para futuras terapias que visem retardar o envelhecimento dos tecidos ou eliminar células senescentes prejudiciais. Embora quaisquer aplicações médicas ainda estejam distantes, entender esse “interruptor de envelhecimento” interno aproxima os cientistas de controlar como nossas células envelhecem.
Citação: Lai, C., Fu, W., Liu, J. et al. LMO7-mediated POLR2A degradation promotes cellular senescence through the MDM4/p53/p21 axis. Cell Death Dis 17, 421 (2026). https://doi.org/10.1038/s41419-026-08679-0
Palavras-chave: senescência celular, envelhecimento, POLR2A, via p53, ubiquitinação