Clear Sky Science · it
La degradazione di POLR2A mediata da LMO7 promuove la senescenza cellulare attraverso l’asse MDM4/p53/p21
Perché le cellule invecchiate sono importanti
Con l’avanzare dell’età, le nostre cellule perdono progressivamente la capacità di dividersi e riparare i tessuti. Molte di queste cellule usurate non muoiono; entrano invece in uno stato duraturo di “dormienza” chiamato senescenza cellulare. Le cellule senescenti possono compromettere organi e favorire malattie legate all’età rilasciando fattori infiammatori. Questo studio pone una domanda semplice ma cruciale: cosa spinge una cellula sana a cadere in questo stato di senescenza — e si può modulare questo interruttore?
Un attore chiave nella macchina di copia della cellula
All’interno di ogni cellula, una grande macchina molecolare chiamata RNA polimerasi II legge il DNA e aiuta ad attivare i geni. POLR2A è la subunità più grande e cruciale di questa macchina. Studi precedenti suggerivano che i livelli di POLR2A diminuiscano nei tessuti più vecchi e in malattie da invecchiamento precoce, ma non era chiaro se ciò fosse un effetto collaterale dell’invecchiamento o parte della causa. Gli autori hanno studiato fibroblasti umani, un tipo comune di cellule di supporto nella pelle e nei polmoni, e hanno esaminato tessuti di topi a diverse età per osservare come POLR2A cambia nel tempo.
Osservare invecchiare le cellule in laboratorio
Il gruppo ha usato due metodi per indurre l’invecchiamento in coltura. Nell’invecchiamento “replicativo”, i fibroblasti sono stati semplicemente lasciati dividersi ripetutamente fino a rallentare naturalmente. Nell’invecchiamento “indotto da stress”, cellule giovani sono state brevemente esposte a perossido di idrogeno, che causa danno ossidativo. In entrambi i modelli, un numero crescente di cellule ha mostrato i segni classici della senescenza: hanno smesso di dividersi, sono risultate positive a un marcatore standard di senescenza e hanno rilasciato molecole infiammatorie. In modo notevole, quando questi cambiamenti comparivano, i livelli proteici di POLR2A calavano drasticamente, mentre il suo mRNA non diminuiva, indicando che la proteina veniva distrutta più rapidamente piuttosto che prodotta meno. Calo simile di POLR2A è stato osservato nei cervelli, nel cuore e nei polmoni di topi anziani, collegando questo processo all’invecchiamento negli animali vivi.
Come la perdita di POLR2A aziona l’interruttore dell’invecchiamento
Per testare causalità, i ricercatori hanno ridotto deliberatamente POLR2A in fibroblasti giovani. Le cellule hanno rapidamente assunto un’identità senescente: hanno smesso di dividersi, hanno attivato il marcatore di senescenza e hanno secreato segnali infiammatori. A livello molecolare, una nota via di controllo basata sulla proteina p53 e sul suo partner p21 è diventata altamente attiva. Quando POLR2A e p53 sono stati soppressi insieme, le cellule hanno in gran parte evitato la senescenza, dimostrando che POLR2A normalmente contribuisce a prevenire l’invecchiamento attraverso questa via p53–p21. Approfondendo, il team ha trovato che i livelli di p53 aumentavano non perché se ne producessero di più, ma perché la sua degradazione rallentava. Una proteina chiamata MDM4, che di solito aiuta a etichettare p53 per la distruzione, diminuiva quando POLR2A calava, portando a una maggiore stabilità di p53 e a segnali più forti per arrestare la divisione cellulare.
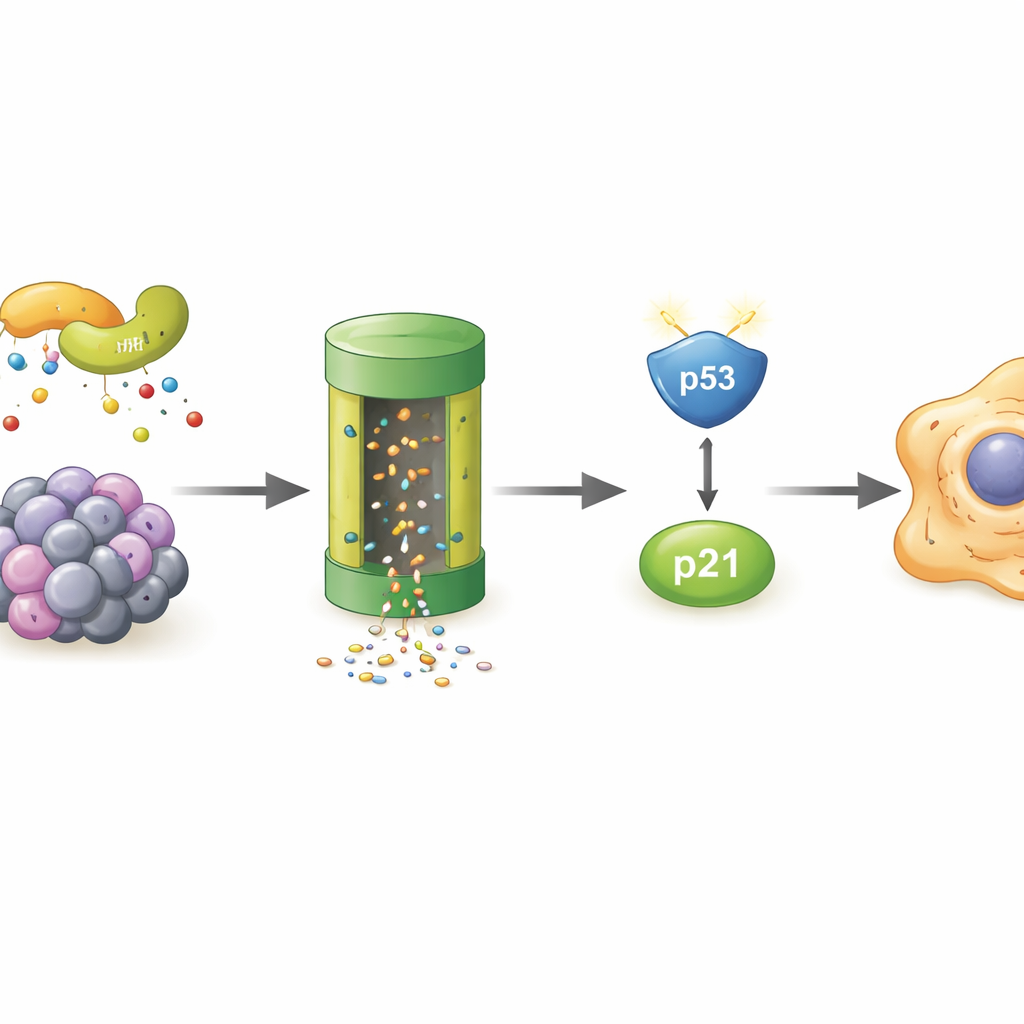
Chi distrugge POLR2A nelle cellule senescenti
Poiché POLR2A scompariva più velocemente nelle cellule senescenti, gli autori hanno cercato il “sistema di smaltimento” responsabile. Hanno dimostrato che bloccare il proteasoma — il principale trituratore di proteine della cellula — ha recuperato i livelli di POLR2A, e che POLR2A portava più marchi di ubiquitina, flag molecolari che indirizzano le proteine alla distruzione. Uno screening con spettrometria di massa ha individuato LMO7, una proteina impalcatura che può far parte di un complesso enzimatico che aggiunge questi marchi. Nelle cellule stressate, LMO7 si legava con maggiore intensità a POLR2A. Quando LMO7 è stato rimosso, POLR2A non veniva più pesantemente etichettata con ubiquitina e i suoi livelli restavano più alti, anche sotto stress ossidativo. Questo individua LMO7 come un attore centrale nella perdita di POLR2A durante la senescenza cellulare.
Riavvolgere l’orologio all’interno delle cellule
Infine, i ricercatori hanno chiesto se aumentare POLR2A potesse contrastare la senescenza. Usando la tecnologia di attivazione CRISPR, hanno leggermente incrementato l’espressione del gene endogeno POLR2A invece di introdurre una copia artificiale. Le cellule con POLR2A elevato sono risultate più resistenti sia alla senescenza indotta da stress sia a quella replicativa: meno cellule sono risultate positive ai marcatori di senescenza e più hanno continuato a dividersi. Allo stesso tempo, i livelli di MDM4 sono rimasti più alti e la via p53–p21 è risultata meno attiva. Questo esperimento suggerisce che preservare POLR2A può aiutare le cellule a sopportare danni che altrimenti le spingerebbero in uno stato di invecchiamento permanente.
Cosa significa per un invecchiamento sano
Nel complesso, i risultati delineano una nuova catena di eventi all’interno delle cellule invecchianti. Sotto stress, LMO7 marca POLR2A per la distruzione, abbassando i livelli della proteina. Ciò riduce a sua volta la produzione di MDM4, permettendo a p53 di accumularsi e attivare p21, che blocca le cellule nella senescenza. Mostrando che il ripristino di POLR2A può interrompere questa catena, lo studio identifica il percorso LMO7–POLR2A–MDM4–p53–p21 come un potenziale bersaglio per terapie future volte a ritardare l’invecchiamento dei tessuti o eliminare le cellule senescenti dannose. Sebbene eventuali applicazioni mediche siano ancora lontane, comprendere questo “interruttore dell’invecchiamento” interno avvicina gli scienziati alla possibilità di modulare come le nostre cellule invecchiano.
Citazione: Lai, C., Fu, W., Liu, J. et al. LMO7-mediated POLR2A degradation promotes cellular senescence through the MDM4/p53/p21 axis. Cell Death Dis 17, 421 (2026). https://doi.org/10.1038/s41419-026-08679-0
Parole chiave: senescenza cellulare, invecchiamento, POLR2A, via di p53, ubiquitinazione