Clear Sky Science · tr
EHMT2-MBLAC2 ekseni nükleolar DNA hasarına yanıt olarak ribozomal DNA transkripsiyonunu baskılar
Hücrenin protein fabrikalarının neden korunmaya ihtiyacı var
Hücrelerimizin her birinin içinde, ribozom adı verilen protein üretim makinelerinin inşa edildiği yoğun bir atölye olan nükleolus bulunur. Bu fabrika neredeyse sürekli çalıştığı için, şablon DNA’sı sürekli gerilim altındadır ve kırılabilir. Bu makaledeki çalışma, hücrelerin hasarı tamir etmek için bu fabrikayı geçici olarak nasıl susturduğunu ve bu güvenlik sisteminin başarısız olmasının kolorektal kanseri nasıl tetikleyebileceğini araştırıyor.
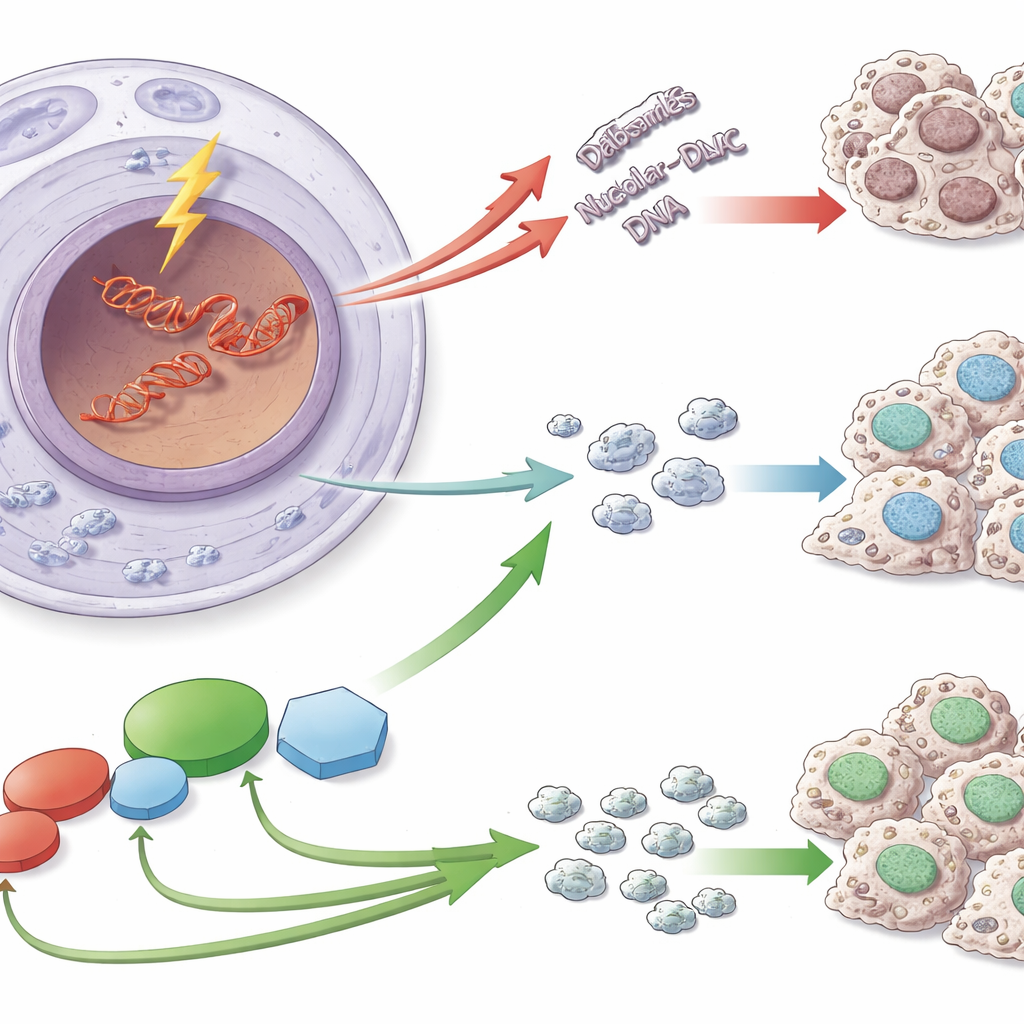
Zayıf bir DNA bölgesi
Ribozomlar, ribozomal DNA (rDNA) olarak bilinen özel DNA dizilerinde kodlanan talimatlar kullanılarak birleştirilir. Bu diziler birçok kez tekrar eder ve çok hızlı bir şekilde kopyalandıkları için çift zincirli kırılmalara özellikle yatkındırlar. rDNA’da böyle kırılmalar meydana geldiğinde hücreler yalnızca DNA’yı yamalamaz: nükleolusu yeniden düzenler ve rDNA’nın RNA’ya kopyalanmasını kısa süreliğine durdurur. Bu duraklama, onarım makinelerinin transkripsiyon mekanizmasıyla çarpışmasını önler ve rDNA tekrarlarının sayısı ile yapısını sabit tutmaya yardımcı olur—bu, rDNA kararsızlığının yaşlanma ve kanser de dahil olmak üzere birçok hastalıkla ilişkili olduğu için önemli bir korumadır.
Nükleolusta yeni bir güvenlik anahtarı
Araştırmacılar, genoma başka yerlerde kromatini değiştirmesiyle daha iyi bilinen EHMT2 adlı bir proteini bu nükleolar güvenlik yanıtında kritik bir oyuncu olarak tanımlıyor. İnsan hücrelerinde rDNA’yı tanımlı bölgelerden kesen bir sistem kullanarak, EHMT2’nin hasarlı rDNA’nın toplanıp kap adı verilen yapılara dönüştüğü nükleolus kenarına hızla gittiğini gösteriyorlar. Orada, EHMT2 hasardan sonra ribozomal RNA üretimini kapatmak için gereklidir. EHMT2 eksikse veya aktivitesi kimyasal olarak engellenirse hücreler kırılmalara rağmen rDNA transkripsiyonuna devam eder. Ekip bu etkiyi, EHMT2’nin hasarlı rDNA’daki histon proteinlerine belirli bir kimyasal işaret ekleme yeteneğine; bunun da daha baskılanmış bir kromatin durumu oluşturmasına yardımcı olduğuna bağlıyor.
Transkripsiyon duraklamasını DNA onarımıyla bağlamak
rDNA’yı susturmak hikâyenin yalnızca yarısıdır; başarılı onarım bunun ardından gelmelidir. Yazarlar, EHMT2 eksik hücrelerin rDNA kırılmalarını onarmakta zorlandığını buluyor: DNA parçaları daha uzun süre kalıyor, küçük ekstra çekirdekler (genomik kararsızlığın bir işareti) daha sık ortaya çıkıyor ve zaman içinde rDNA kopya sayısı azalıyor. Önemli olarak, hızlıca DNA uçlarını yeniden birleştiren bir ana onarım yolu olan homolog olmayan uç birleştirme (NHEJ), EHMT2 olmadan rDNA kaplarına düzgün şekilde yönlendirilemiyor; diğer onarım yolları büyük ölçüde etkilenmemiş durumda. Sonuç olarak, EHMT2 eksik hücreler nükleolar hasara karşı aşırı duyarlı hale geliyor ve rDNA kesildikten sonra sağlıklı koloni oluşturma yeteneklerini kaybediyorlar.
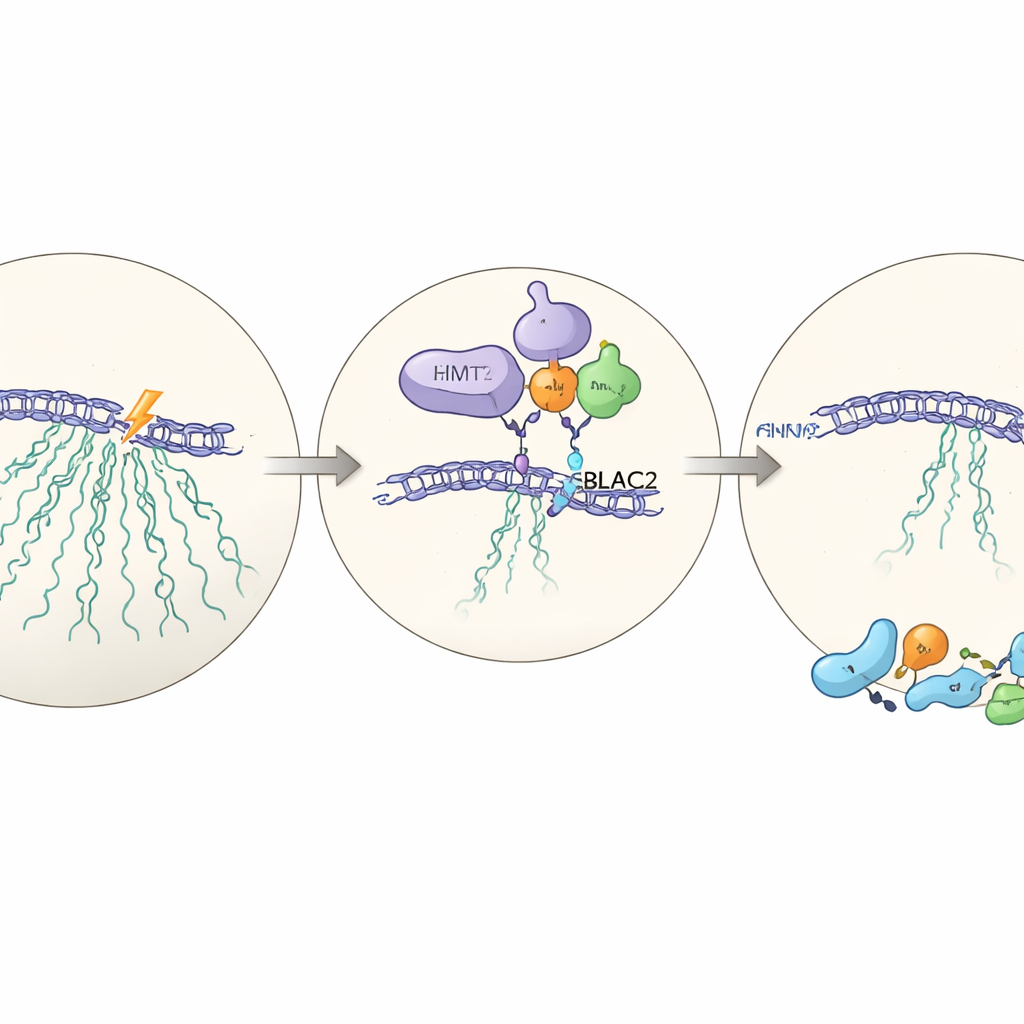
Gizli bir ortak: MBLAC2
EHMT2’nin etkisini nasıl gösterdiğini anlamak için ekip, EHMT2 olan ve olmayan hücrelerde geniş çaplı protein ölçümleri yapıyor. EHMT2 yok olduğunda azalan proteinler arasında öne çıkan bir tanesi var: normalde nükleolusta zenginleşmiş olan, az çalışılmış bir enzim olan MBLAC2. MBLAC2 hedeflenmiş RNA araçlarıyla azaltıldığında, hücreler tekrar hasar sonrası rDNA’yı susturamıyor ve hasardan sağ kalma yetenekleri düşüyor. EHMT2, MBLAC2’ye fiziksel olarak bağlanıyor ve onu protein düzeyinde stabilize ediyor; EHMT2 yokken MBLAC2 daha hızlı parçalanıyor. Her iki proteinin birden kaldırılması, tek birini kaldırmaktan daha kötü bir etki yaratmıyor; bu da onların aynı yolda aktığını gösteriyor—transkripsiyon duraklamasını etkili onarım ile koordine eden yeni tanımlanmış bir EHMT2–MBLAC2 ekseni.
Hasarlı DNA’dan kolorektal kansere
rDNA kararsızlığı birçok tümörün ayırt edici özelliği olduğundan, yazarlar bu eksenin kolorektal kanserde bir rol oynayıp oynamadığını sorguluyor; bu hastalık yükselmiş ribozom üretimine güçlü biçimde bağımlıdır. Fare modellerinde ve insan tümör örneklerinde EHMT2 ve MBLAC2, normal kolon dokusuna göre kolorektal tümörlerde tutarlı bir biçimde daha fazla bulunuyor; bu durum, artırılmış ribozom oluşumunun belirteçleriyle paralellik gösteriyor. Kolorektal kanser hücrelerinde EHMT2 baskılandığında farelerde tümör büyümesi yavaşlıyor, ribozomla ilişkili belirteçler azalıyor ve MBLAC2 seviyeleri düşüyor. The Cancer Genome Atlas’ın hasta verileri, her iki genin daha yüksek ifadesinin daha ileri hastalıkla ve radyoterapi sonrası daha kötü sağkalımla ilişkili olduğunu ortaya koyuyor. Bu gözlemler birlikte, kanser hücrelerinin rDNA hasarına daha iyi dayanabilmek ve kontrolsüz büyüme için gereken ribozom üretimini sürdürmek üzere EHMT2–MBLAC2 yolunu kötüye kullanabileceğini öne sürüyor.
Sağlık ve tedavi açısından anlamı
Genel okuyucu için ana mesaj şudur: hücrelerimiz nükleolusta adanmış bir acil durum freni geliştirmiştir: ribozomların DNA şablonu kırıldığında EHMT2 ve ortağı MBLAC2 fabrikanın durmasını, onarımı yönlendirmesini ve stabilitenin yeniden sağlanmasını sağlar. Bu fren kolorektal kanserde aşırı etkinleştiğinde veya kötüye kullanıldığında, tümör hücrelerinin strese ve tedaviye karşı hayatta kalmasına yardımcı oluyor gibi görünür. EHMT2, MBLAC2 veya bunların etkileşimini hedefleyerek geliştirilecek tedaviler, kanser hücrelerinin ribozomal DNA hasarıyla başa çıkma yeteneğini seçici olarak zayıflatabilir; böylece kemoterapi ve radyoterapi gibi standart tedavileri normal dokuya kıyasla daha etkili hale getirebilir.
Atıf: Wang, C., Lu, Q., Cao, L. et al. The EHMT2-MBLAC2 axis suppresses ribosomal DNA transcription in response to nucleolar DNA damage. Cell Death Dis 17, 320 (2026). https://doi.org/10.1038/s41419-026-08616-1
Anahtar kelimeler: ribozomal DNA hasarı, nükleolar stres, EHMT2 MBLAC2 yolu, kolorektal kanser, DNA onarımı ve transkripsiyon