Clear Sky Science · nl
De EHMT2-MBLAC2-as biedt rem op ribosomaal DNA-transcriptie als reactie op nucleolair DNA-schade
Waarom de eiwitfabrieken van de cel bescherming nodig hebben
In elke cel bevindt zich een drukke werkplaats, het nucleolus, waar de moleculaire machines die eiwitten maken—de ribosomen—worden opgebouwd. Omdat deze fabriek vrijwel onophoudelijk draait, staat het DNA‑sjabloon onder constante belasting en kan het breken. De studie in dit artikel onderzoekt hoe cellen deze fabriek tijdelijk stilleggen om schade te herstellen, en hoe falen van dit beveiligingssysteem kan bijdragen aan dikke darmkanker.
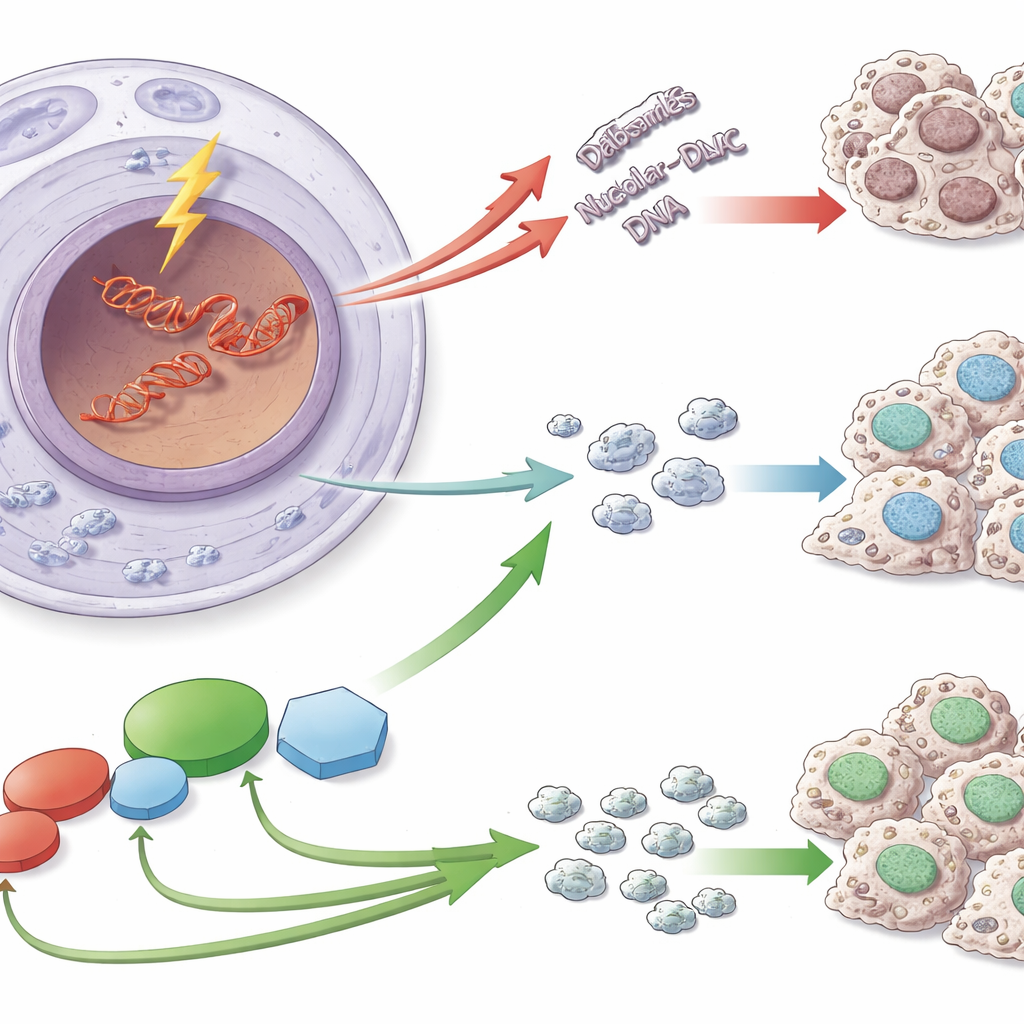
Een kwetsbare streng DNA
Ribosomen worden samengesteld met instructies die gecodeerd staan in speciale DNA‑segmenten, bekend als ribosomaal DNA (rDNA). Deze sequenties komen veelvuldig voor en worden snel gekopieerd, waardoor ze bijzonder vatbaar zijn voor gevaarlijke dubbele strengbreuken. Als zulke breuken in rDNA optreden, doen cellen meer dan alleen het DNA repareren: ze reorganiseren ook het nucleolus en stoppen tijdelijk met het kopiëren van rDNA naar RNA. Deze onderbreking voorkomt dat reparatiemechanismen botsen met de transcriptiemachinerie en draagt bij aan het behoud van het aantal en de structuur van rDNA‑herhalingen—een belangrijke beschermingsmaatregel, aangezien instabiliteit van rDNA in verband is gebracht met veroudering en veel ziekten, waaronder kanker.
Een nieuwe veiligheidschakelaar in het nucleolus
De onderzoekers identificeren een eiwit genaamd EHMT2, beter bekend om het wijzigen van chromatine elders in het genoom, als een cruciale speler in deze nucleolaire veiligheidsreactie. Met een systeem in menselijke cellen dat rDNA op gedefinieerde plaatsen knipt, tonen ze aan dat EHMT2 naar de rand van het nucleolus snelt, waar beschadigd rDNA zich verzamelt in structuren die caps worden genoemd. Daar is EHMT2 nodig om de productie van ribosomaal RNA na schade stil te leggen. Als EHMT2 ontbreekt of zijn activiteit chemisch wordt geblokkeerd, blijven cellen rDNA transcriberen ondanks de breuken. Het team brengt dit effect terug tot het vermogen van EHMT2 om een specifieke chemische markering aan histonproteïnen bij beschadigd rDNA toe te voegen, wat helpt een meer onderdrukt chromatine‑toestand te creëren.
De koppeling tussen transcriptiepauze en DNA‑reparatie
Het tot zwijgen brengen van rDNA is maar de helft van het verhaal; succesvolle reparatie moet volgen. De auteurs constateren dat cellen zonder EHMT2 moeite hebben met het herstellen van rDNA‑breuken: DNA‑fragmenten blijven langer aanwezig, kleine extra kernen (een teken van genomische instabiliteit) verschijnen vaker, en het aantal rDNA‑kopieën neemt in de loop van de tijd af. Belangrijk is dat één belangrijke reparatieroute—non‑homologous end joining, die DNA‑einden snel weer verbindt—niet goed naar rDNA‑caps wordt gerekruteerd zonder EHMT2, ook al blijven andere reparatiepaden grotendeels intact. Als gevolg daarvan worden EHMT2‑deficiënte cellen hypersensitief voor nucleolaire schade en verliezen ze het vermogen om gezonde kolonies te vormen nadat rDNA is geknipt.
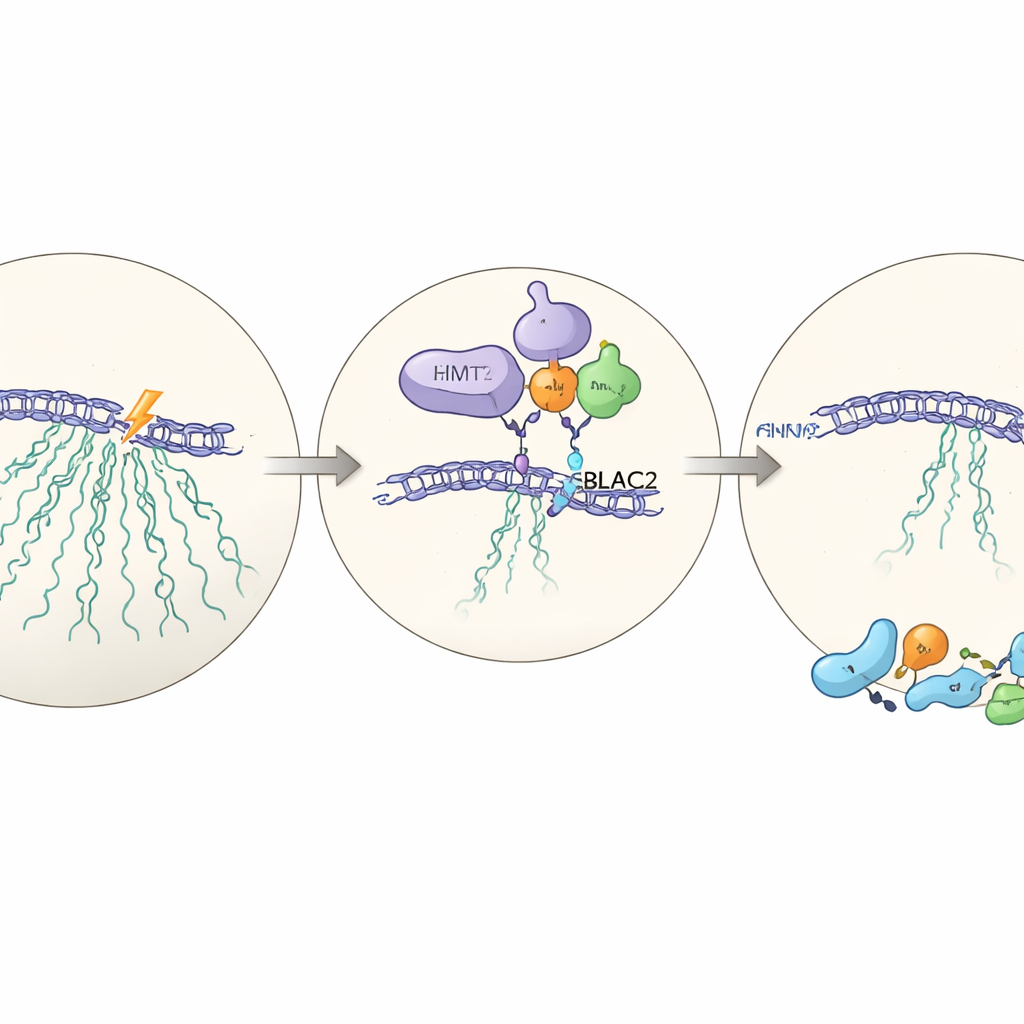
Een verborgen partner: MBLAC2
Om te begrijpen hoe EHMT2 zijn invloed uitoefent, voert het team grootschalige eiwitmetingen uit in cellen met en zonder EHMT2. Onder de eiwitten die afnemen wanneer EHMT2 ontbreekt, springt er één in het oog: MBLAC2, een weinig bestudeerd enzym dat normaal in het nucleolus geconcentreerd is. Wanneer MBLAC2 met gerichte RNA‑instrumenten wordt verminderd, falen cellen opnieuw om rDNA na schade stil te leggen en worden ze minder bestand tegen die schade. EHMT2 bindt fysiek aan MBLAC2 en stabiliseert het op eiwitniveau; zonder EHMT2 wordt MBLAC2 sneller afgebroken. Het wegnemen van beide eiwitten verergert het effect niet verder dan het wegnemen van één, wat suggereert dat ze in dezelfde route werken—een nieuw beschreven EHMT2–MBLAC2‑as die de transcriptiepauze coördineert met effectieve reparatie.
Van beschadigd DNA naar dikke darmkanker
Aangezien instabiliteit van rDNA een kenmerk is van veel tumoren, onderzoeken de auteurs of deze as een rol speelt bij dikke darmkanker, een ziekte die sterk afhankelijk is van verhoogde ribosoomproductie. In muismodellen en menselijke tumormonsters blijken zowel EHMT2 als MBLAC2 consequent in hogere mate aanwezig in colorectale tumoren dan in normaal colonweefsel, parallel aan markers van verhoogde ribosoomvorming. Het onderdrukken van EHMT2 in colorectale kankercellen vertraagt de groei van tumoren in muizen, vermindert ribosoomgerelateerde markers en verlaagt MBLAC2‑niveaus. Patiëntgegevens uit The Cancer Genome Atlas laten zien dat hogere expressie van beide genen samenhangt met meer gevorderde ziekte en slechtere overleving na radiotherapie. Samen wijzen deze observaties erop dat kankercellen mogelijk de EHMT2–MBLAC2‑route kapen om beter bestand te zijn tegen rDNA‑schade en de ribosoomproductie te behouden die nodig is voor ongecontroleerde groei.
Wat dit betekent voor gezondheid en therapie
Voor een lezer zonder vakachtergrond is de kernboodschap dat onze cellen een speciaal noodremsysteem in het nucleolus hebben ontwikkeld: wanneer het DNA‑blauwdruk voor ribosomen breekt, helpen EHMT2 en zijn partner MBLAC2 de fabriek tijdelijk stil te leggen, de reparatie te leiden en de stabiliteit te herstellen. Wanneer deze rem te actief is of bij dikke darmkanker wordt misbruikt, lijkt dit tumorcellen te helpen stress en behandeling te overleven. Door EHMT2, MBLAC2 of hun interactie te richten, zouden toekomstige therapieën selectief het vermogen van kankercellen om met schade aan ribosomaal DNA om te gaan kunnen verzwakken, waardoor standaardbehandelingen zoals chemotherapie en radiotherapie effectiever worden terwijl gezond weefsel gespaard blijft.
Bronvermelding: Wang, C., Lu, Q., Cao, L. et al. The EHMT2-MBLAC2 axis suppresses ribosomal DNA transcription in response to nucleolar DNA damage. Cell Death Dis 17, 320 (2026). https://doi.org/10.1038/s41419-026-08616-1
Trefwoorden: schade aan ribosomaal DNA, nucleolair stress, EHMT2 MBLAC2-route, dikke darmkanker, DNA-reparatie en transcriptie