Clear Sky Science · sv
EHMT2–MBLAC2-axeln dämpar transkription av ribosomalt DNA som svar på nukleolärt DNA‑skada
Varför cellens proteinfabriker behöver skydd
Inne i var och en av våra celler finns en livlig verkstad kallad nukleolen, där de molekylära maskinerna som bygger proteiner—ribosomerna—sätts ihop. Eftersom denna fabrik nästan aldrig stannar är dess DNA‑mall under konstant påfrestning och kan gå sönder. Studien i den här artikeln undersöker hur celler tillfälligt tystar denna fabrik för att laga skador, och hur fel i detta säkerhetssystem kan bidra till utvecklingen av kolorektal cancer.
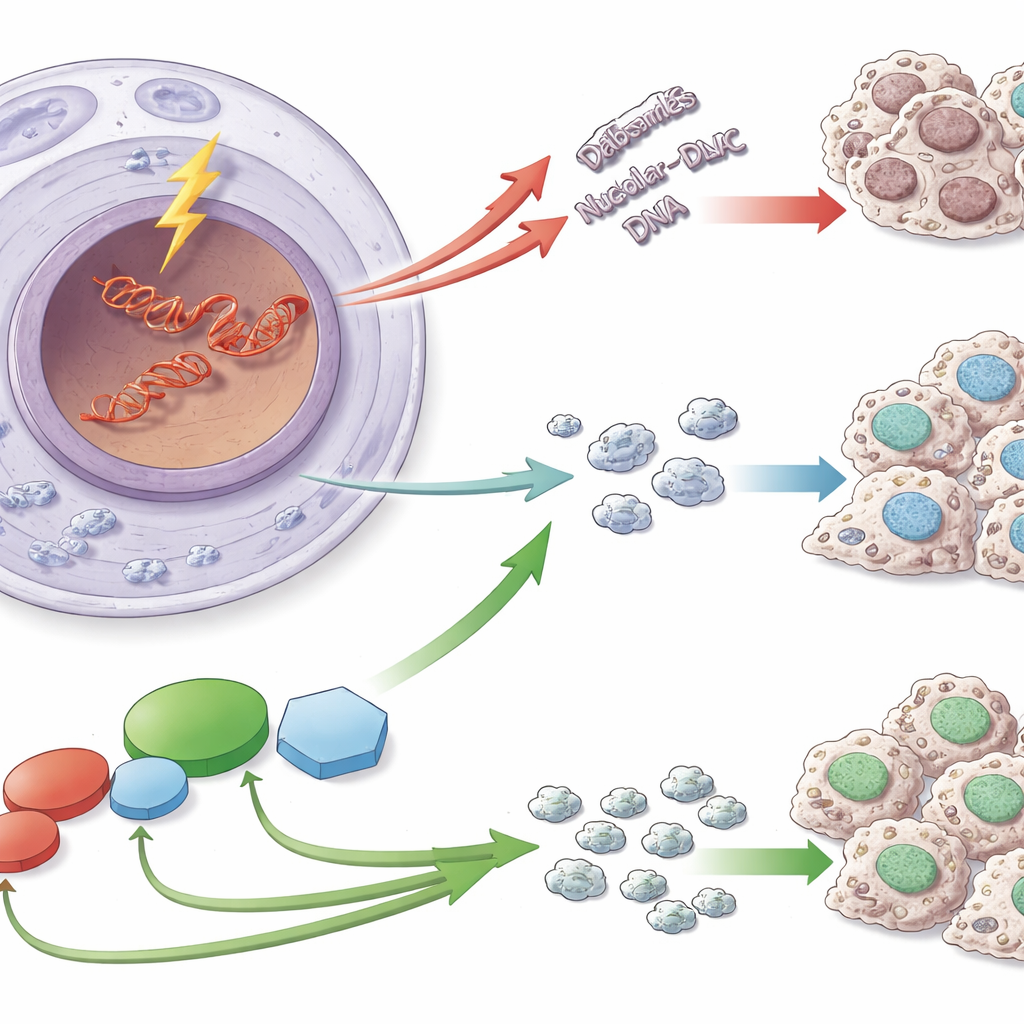
En sårbar DNA‑sträcka
Ribosomer monteras med instruktioner kodade i särskilda DNA‑segment som kallas ribosomalt DNA (rDNA). Dessa sekvenser upprepas många gånger och kopieras i mycket hög hastighet, vilket gör dem särskilt mottagliga för farliga dubbelsträngsbrott. När sådana brott uppstår i rDNA gör cellerna mer än att bara lappa ihop DNA:t: de omorganiserar också nukleolen och stänger tillfälligt av kopieringen av rDNA till RNA. Detta uppehåll förhindrar att reparationsmaskiner kolliderar med transkriptionsmaskineriet och hjälper till att hålla antalet och strukturen hos rDNA‑upprepningar stabila—en viktig skyddsåtgärd, eftersom instabilitet i rDNA har kopplats till åldrande och många sjukdomar, inklusive cancer.
En ny säkerhetsbrytare i nukleolen
Forskarna identifierar ett protein kallat EHMT2, mest känt för att modifiera kromatin på andra ställen i genomet, som en avgörande aktör i denna nukleära säkerhetsrespons. Med hjälp av ett system i människoceller som klipper rDNA på definierade platser visar de att EHMT2 skyndar till kanten av nukleolen där skadat rDNA samlas i strukturer kallade caps. Där krävs EHMT2 för att stänga av produktionen av ribosomalt RNA efter skada. När EHMT2 saknas eller dess aktivitet kemiskt blockeras fortsätter cellerna att transkribera rDNA trots brotten. Teamet härleder denna effekt till EHMT2:s förmåga att lägga till en specifik kemisk markering på histonproteiner vid skadat rDNA, vilket bidrar till att skapa ett mer repressivt kromatintillstånd.
Kopplingen mellan transkriptionsuppehåll och DNA‑reparation
Att tysta rDNA är bara halva berättelsen; framgångsrik reparation måste följa. Författarna finner att celler utan EHMT2 har svårt att reparera rDNA‑brott: DNA‑fragment kvarstår längre, små extra kärnor (ett tecken på genomisk instabilitet) uppträder oftare, och antalet rDNA‑kopior sjunker över tid. Viktigt är att en huvudväg för reparation—non‑homologous end joining, som snabbt återförsluter DNA‑ändar—inte rekryteras korrekt till rDNA‑caps utan EHMT2, även om andra reparationsvägar i stort sett förblir intakta. Som ett resultat blir EHMT2‑bristfälliga celler hypersensitiva för nukleolära skador och förlorar sin förmåga att bilda friska kolonier efter att rDNA klippts.
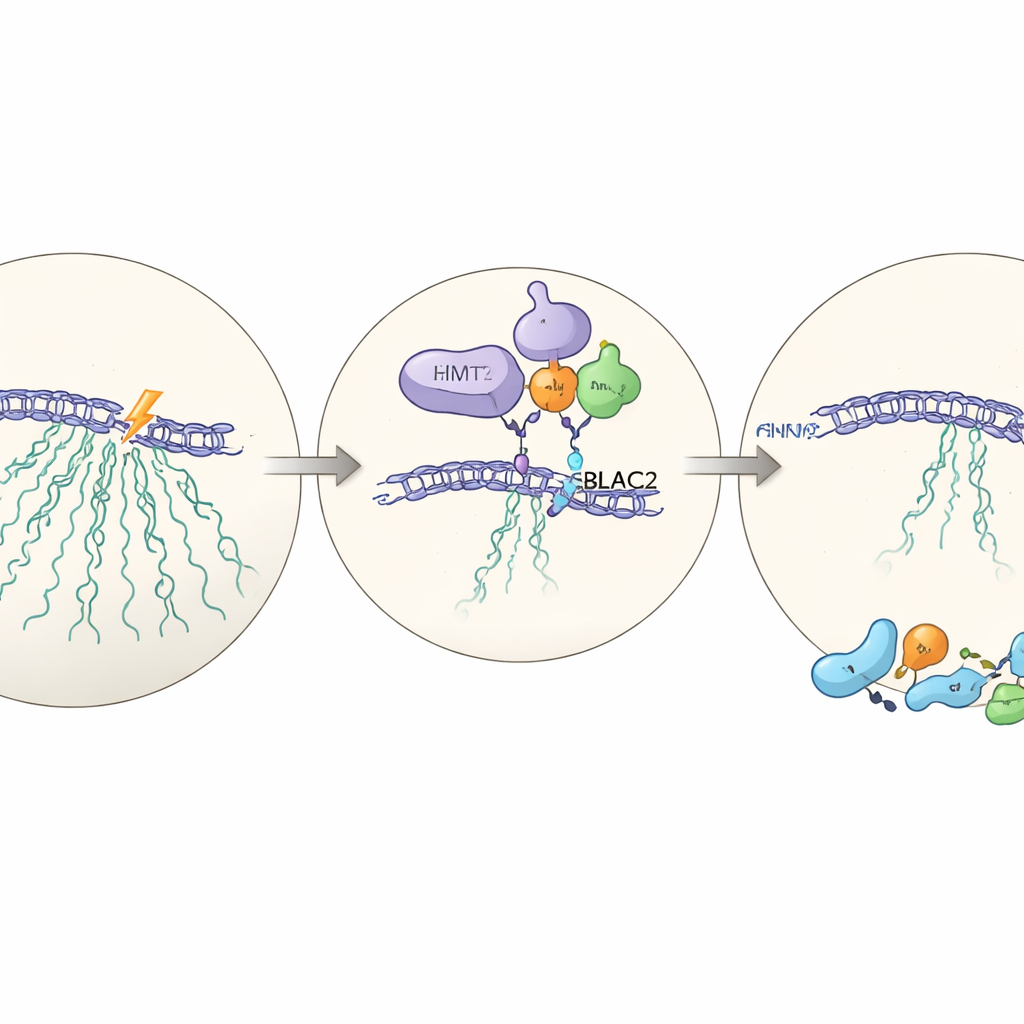
En dold partner: MBLAC2
För att förstå hur EHMT2 utövar sitt inflytande utför teamet storskaliga proteinmätningar i celler med och utan EHMT2. Bland de proteiner som minskar när EHMT2 saknas utmärker sig ett: MBLAC2, ett lite studerat enzym som normalt är berikat i nukleolen. När MBLAC2 minskas med riktade RNA‑verktyg misslyckas cellerna återigen med att tysta rDNA efter skada och blir mindre kapabla att överleva den. EHMT2 binder fysiskt till MBLAC2 och stabiliserar det på proteinnivå; utan EHMT2 degraderas MBLAC2 snabbare. Att ta bort båda proteinerna förvärrar inte effekten utöver att ta bort ett, vilket tyder på att de verkar i samma bana—en nyligen beskriven EHMT2–MBLAC2‑axel som koordinerar transkriptionsuppehållet med effektiv reparation.
Från skadat DNA till kolorektal cancer
Eftersom instabilitet i rDNA är ett kännetecken för många tumörer frågar författarna om denna axel spelar en roll i kolorektal cancer, en sjukdom som starkt förlitar sig på ökad ribosomproduktion. I musemodeller och mänskliga tumörprover är både EHMT2 och MBLAC2 konsekvent mer rikliga i kolorektala tumörer än i normalt kolonvävnad, parallellt med markörer för ökad ribosombildning. Att undertrycka EHMT2 i kolorektala cancerceller bromsar tumörtillväxt i möss, minskar ribosomrelaterade markörer och sänker MBLAC2‑nivåerna. Patientdata från The Cancer Genome Atlas visar att högre uttryck av båda generna förknippas med mer avancerad sjukdom och sämre överlevnad efter strålbehandling. Tillsammans tyder dessa observationer på att cancerceller kan kapa EHMT2–MBLAC2‑vägen för att bättre tolerera rDNA‑skador och upprätthålla det ribosomflöde som krävs för okontrollerad tillväxt.
Vad detta betyder för hälsa och terapi
För en lekman är huvudbudskapet att våra celler har utvecklat en dedikerad nödbroms inne i nukleolen: när DNA‑ritningen för ribosomer bryts hjälper EHMT2 och dess partner MBLAC2 till att pausa fabriken, styra reparationen och återställa stabiliteten. När denna broms är överaktiv eller missbrukas i kolorektal cancer verkar den hjälpa tumörceller att överleva stress och behandling. Genom att rikta in sig på EHMT2, MBLAC2 eller deras interaktion kan framtida terapier selektivt försvaga cancercellers förmåga att hantera skador i ribosomalt DNA, vilket skulle kunna göra standardbehandlingar som kemoterapi och strålning mer effektiva samtidigt som normal vävnad skonas.
Citering: Wang, C., Lu, Q., Cao, L. et al. The EHMT2-MBLAC2 axis suppresses ribosomal DNA transcription in response to nucleolar DNA damage. Cell Death Dis 17, 320 (2026). https://doi.org/10.1038/s41419-026-08616-1
Nyckelord: skada på ribosomalt DNA, nukleolärt stress, EHMT2 MBLAC2‑väg, kolorektal cancer, DNA‑reparation och transkription