Clear Sky Science · it
L’asse EHMT2-MBLAC2 sopprime la trascrizione del DNA ribosomale in risposta al danno al nucleolo
Perché le “fabbriche” proteiche della cellula hanno bisogno di protezione
All’interno di ciascuna delle nostre cellule c’è un laboratorio in fermento chiamato nucleolo, dove vengono assemblate le macchine molecolari che producono le proteine—i ribosomi. Poiché questa «fabbrica» lavora quasi senza sosta, il suo modello di DNA è sottoposto a stress continuo e può rompersi. Lo studio descritto in questo articolo analizza come le cellule mettano temporaneamente in silenzio questa attività per riparare i danni e come la mancata attivazione di questo meccanismo di sicurezza possa favorire il carcinoma colorettale.
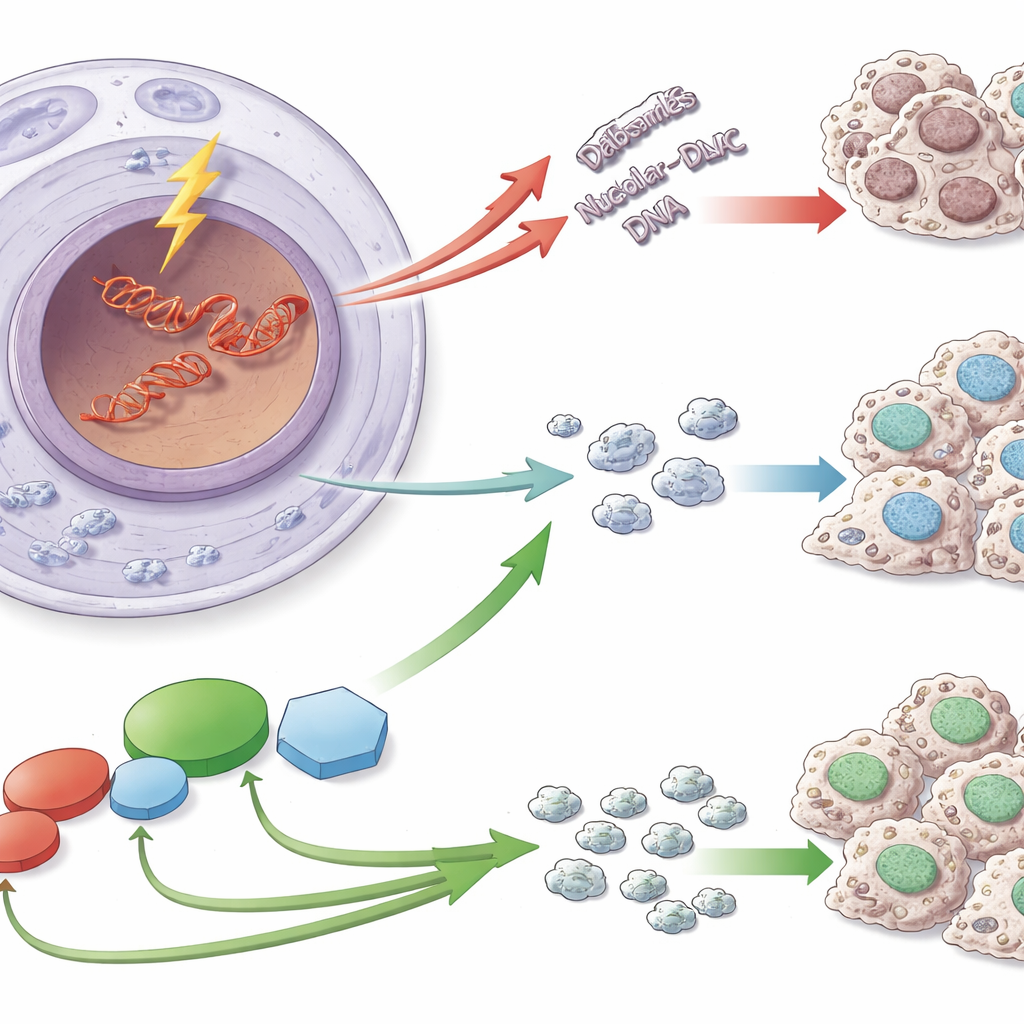
Un tratto di DNA vulnerabile
I ribosomi vengono assemblati usando le istruzioni codificate in segmenti di DNA speciali noti come DNA ribosomale (rDNA). Queste sequenze sono ripetute molte volte e vengono copiate a velocità molto elevata, il che le rende particolarmente soggette a rotture a doppio filamento pericolose. Quando si verificano tali rotture nell’rDNA, le cellule non si limitano a riparare il DNA: riorganizzano anche il nucleolo e sospendono temporaneamente la trascrizione dell’rDNA in RNA. Questa pausa impedisce che le macchine di riparazione si scontrino con la macchina di trascrizione e aiuta a mantenere stabile il numero e la struttura delle ripetizioni di rDNA—una salvaguardia importante, perché l’instabilità dell’rDNA è stata collegata all’invecchiamento e a molte malattie, incluso il cancro.
Un nuovo interruttore di sicurezza nel nucleolo
I ricercatori identificano una proteina chiamata EHMT2, nota soprattutto per modificare la cromatina in altre parti del genoma, come un elemento cruciale di questa risposta di sicurezza nucleolare. Usando un sistema in cellule umane che taglia l’rDNA in siti definiti, mostrano che EHMT2 corre al bordo del nucleolo dove l’rDNA danneggiato si raccoglie in strutture chiamate «cap». Lì, EHMT2 è necessario per bloccare la produzione di RNA ribosomale dopo il danno. Quando EHMT2 manca o la sua attività è bloccata chimicamente, le cellule continuano a trascrivere l’rDNA nonostante le rotture. Il gruppo collega questo effetto alla capacità di EHMT2 di aggiungere un marchio chimico specifico alle proteine istoniche sull’rDNA danneggiato, contribuendo a creare uno stato di cromatina più reprimente.
Collegare la pausa nella trascrizione alla riparazione del DNA
Silenziare l’rDNA è solo metà della storia; alla pausa deve seguire una riparazione efficace. Gli autori rilevano che le cellule prive di EHMT2 faticano a riparare le rotture nell’rDNA: i frammenti di DNA persistono più a lungo, compaiono più spesso piccoli nuclei extra (un segno di instabilità genomica) e il numero di copie di rDNA diminuisce nel tempo. Importante, una via di riparazione principale—la giunzione per non omologia (NHEJ), che richiude rapidamente gli estremi del DNA—non viene adeguatamente reclutata nei cap dell’rDNA senza EHMT2, anche se altre vie di riparazione rimangono per lo più intatte. Di conseguenza, le cellule carenti di EHMT2 diventano ipersensibili al danno nucleolare e perdono la capacità di formare colonie sane dopo il taglio dell’rDNA.
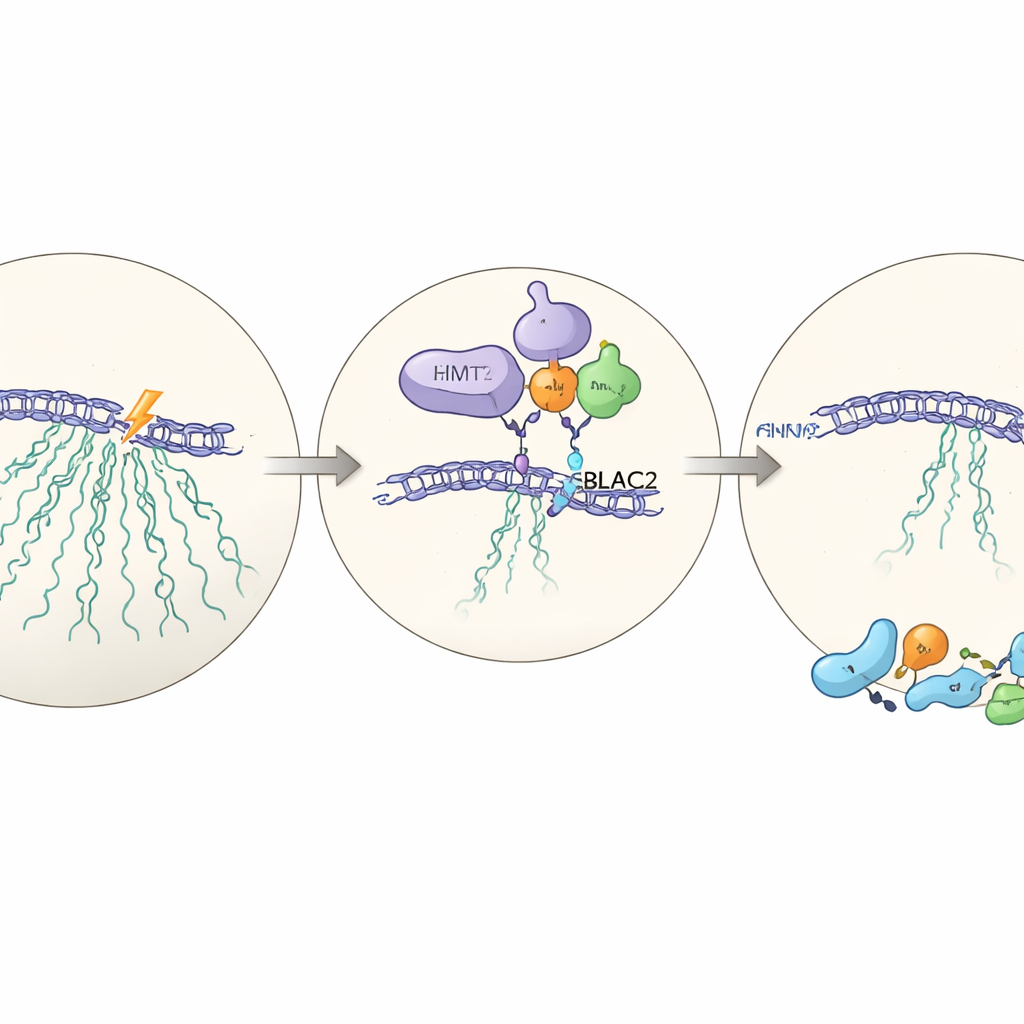
Un partner nascosto: MBLAC2
Per capire come EHMT2 eserciti la sua influenza, il gruppo esegue misurazioni proteiche su larga scala in cellule con e senza EHMT2. Tra le proteine che diminuiscono in assenza di EHMT2, una emerge in modo significativo: MBLAC2, un enzima poco studiato normalmente arricchito nel nucleolo. Quando MBLAC2 viene ridotto con strumenti di RNA mirati, le cellule nuovamente non riescono a silenziare l’rDNA dopo il danno e diventano meno in grado di sopravvivere. EHMT2 si lega fisicamente a MBLAC2 e lo stabilizza a livello proteico; senza EHMT2, MBLAC2 viene degradato più rapidamente. La rimozione di entrambe le proteine non peggiora l’effetto rispetto alla rimozione di una sola, suggerendo che agiscano nella stessa via—un asse EHMT2–MBLAC2 appena descritto che coordina la pausa della trascrizione con una riparazione efficace.
Dal DNA danneggiato al carcinoma colorettale
Poiché l’instabilità dell’rDNA è una caratteristica di molti tumori, gli autori si chiedono se questo asse giochi un ruolo nel carcinoma colorettale, una malattia che dipende fortemente dall’aumento della produzione di ribosomi. Nei modelli murini e nei campioni tumorali umani, sia EHMT2 sia MBLAC2 sono costantemente più abbondanti nei tumori colorettali rispetto al tessuto colonico normale, in parallelo con marcatori di formazione ribosomale potenziata. Sopprimere EHMT2 nelle cellule di carcinoma colorettale rallenta la crescita dei tumori nei topi, riduce i marker legati ai ribosomi e abbassa i livelli di MBLAC2. Dati clinici provenienti da The Cancer Genome Atlas rivelano che una maggiore espressione di entrambi i geni si associa a una malattia più avanzata e a una sopravvivenza peggiore dopo la radioterapia. Nel complesso, queste osservazioni suggeriscono che le cellule tumorali possano sfruttare l’asse EHMT2–MBLAC2 per tollerare meglio il danno all’rDNA e mantenere la produzione di ribosomi necessaria alla crescita incontrollata.
Cosa significa per la salute e la terapia
Per il lettore non specialista, il messaggio chiave è che le nostre cellule hanno evoluto un freno d’emergenza nel nucleolo: quando si rompe il progetto in DNA per i ribosomi, EHMT2 e il suo partner MBLAC2 aiutano a mettere in pausa la fabbrica, guidare la riparazione e ristabilire la stabilità. Quando questo freno è iperattivo o sfruttato nel carcinoma colorettale, sembra aiutare le cellule tumorali a sopravvivere allo stress e alle terapie. Mirare a EHMT2, MBLAC2 o alla loro interazione potrebbe permettere a future terapie di indebolire selettivamente la capacità delle cellule tumorali di affrontare il danno al DNA ribosomale, rendendo più efficaci trattamenti standard come la chemioterapia e la radioterapia, risparmiando al contempo i tessuti normali.
Citazione: Wang, C., Lu, Q., Cao, L. et al. The EHMT2-MBLAC2 axis suppresses ribosomal DNA transcription in response to nucleolar DNA damage. Cell Death Dis 17, 320 (2026). https://doi.org/10.1038/s41419-026-08616-1
Parole chiave: danno al DNA ribosomale, stress nucleolare, percorso EHMT2 MBLAC2, carcinoma colorettale, riparazione del DNA e trascrizione