Clear Sky Science · he
ציר EHMT2-MBLAC2 מדכא את שעתוק ה-DNA הריבוזומלי בתגובה לפגיעות בגרעינית
למה המפעלים שמייצרים חלבונים בתא זקוקים להגנה
בתוך כל אחד מתאינו שוכן אתר הומה בשם הגרעינית, שבו נבנים המכונות המולקולריות שמייצרות חלבונים — הריבוזומים. מאחר שמפעל זה פועל כמעט ללא הרף, תבנית ה‑DNA שלו נתונה למתח מתמיד ועלולה להישבר. המחקר המתואר כאן חוקר כיצד התאים משתקפים באופן זמני את המפעל הזה כדי לתקן נזקים, וכיצד כישלון במערכת הבטיחות הזו עשוי לתרום להתפתחות סרטן המעי הגס.
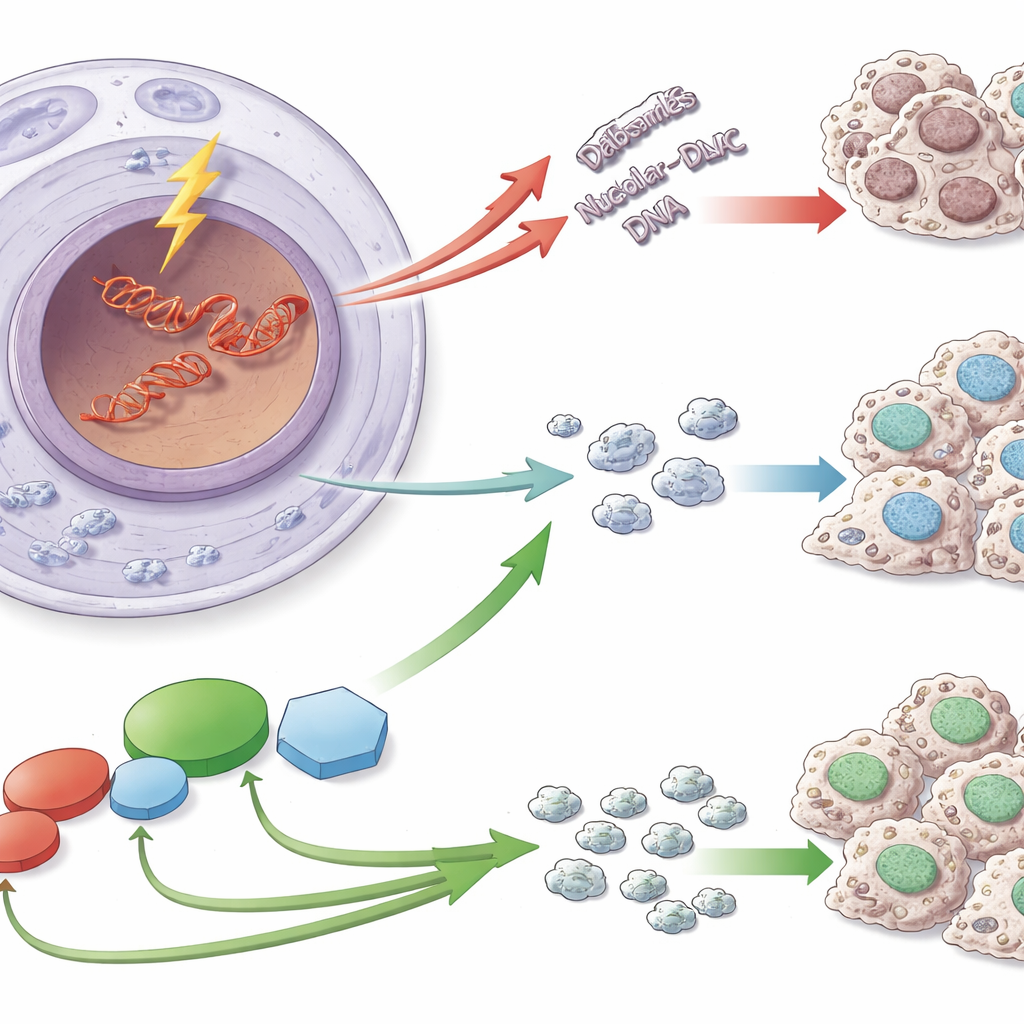
קטע DNA פגיע
הריבוזומים נאספים לפי הוראות המקודדות במקטעים מיוחדים של ה‑DNA הידועים כ‑ribosomal DNA (rDNA). רצפים אלה חוזרים על עצמם פעמים רבות ומועתקים בקצב גבוה מאוד, מה שהופך אותם לפגיעים במיוחד לשברים דו‑גדיליים מסוכנים. כאשר שברים כאלה מתרחשים ב‑rDNA, התאים עושים יותר מאשר רק לתקן את ה‑DNA: הם גם מארגנים מחדש את הגרעינית ומפחיתים זמנית את שעתוק ה‑rDNA ל‑RNA. עצירה זו מונעת התנגשות בין מכונות התיקון למכונות השעתוק ועוזרת לשמר את מספר ומבנה החזרות של ה‑rDNA — אמצעי הגנה חשוב, שכן нестабильность של rDNA נקשרה להזדקנות ולמחלות רבות, כולל סרטן.
מכשול בטיחות חדש בגרעינית
החוקרים מזהים חלבון בשם EHMT2, המוכר יותר כבעל תפקיד בשינוי הכרומטין באזורים אחרים של הגנום, כשחקן מכריע בתגובה זו של הגרעינית. באמצעות מערכת בתאים אנושיים שמבצעת חיתוך ב‑rDNA במקומות מוגדרים, הם מראים ש‑EHMT2 מתמקד בקצה הגרעינית, שם ה‑rDNA הפגוע נאסף למבנים הנקראים caps. שם נדרש EHMT2 כדי להפסיק את ייצור ה‑rRNA לאחר הנזק. כאשר EHMT2 חסר או שהפעילות שלו מעוכבת כימית, התאים ממשיכים לשעתק את ה‑rDNA למרות השברים. הצוות מייחס השפעה זו ליכולתו של EHMT2 להוסיף סימון כימי מסוים לחלבוני היסטון ב‑rDNA הפגוע, ובכך לסייע ליצור מצע כרומטיני יותר מדוכא.
קישור בין עצירת השעתוק לתיקון ה‑DNA
החרשת ה‑rDNA היא רק חצי מהסיפור; תיקון מוצלח חייב להימשך אחריה. המחברים מגלים שתאים חסרי EHMT2 מתקשים לתקן את שברי ה‑rDNA: שברי DNA נמשכים זמן רב יותר, גרעינים קטנים נוספים (אינדיקציה לחוסר יציבות גנומית) מופיעים בתדירות גבוהה יותר, ומספר העתקים של ה‑rDNA יורד עם הזמן. באופן חשוב, אחד מסלולי התיקון המרכזיים — non‑homologous end joining, שמחבר במהירות קצוות DNA — לא מגויס כראוי ל‑rDNA caps בלי EHMT2, אף על פי שדרכי תיקון אחרות נשארות במידה רבה תקינות. כתוצאה מכך, תאים חסרי EHMT2 הופכים לרגישים במיוחד לנזק בגרעינית ומאבדים את יכולתם להקים מושבות בריאות לאחר חיתוך ה‑rDNA.
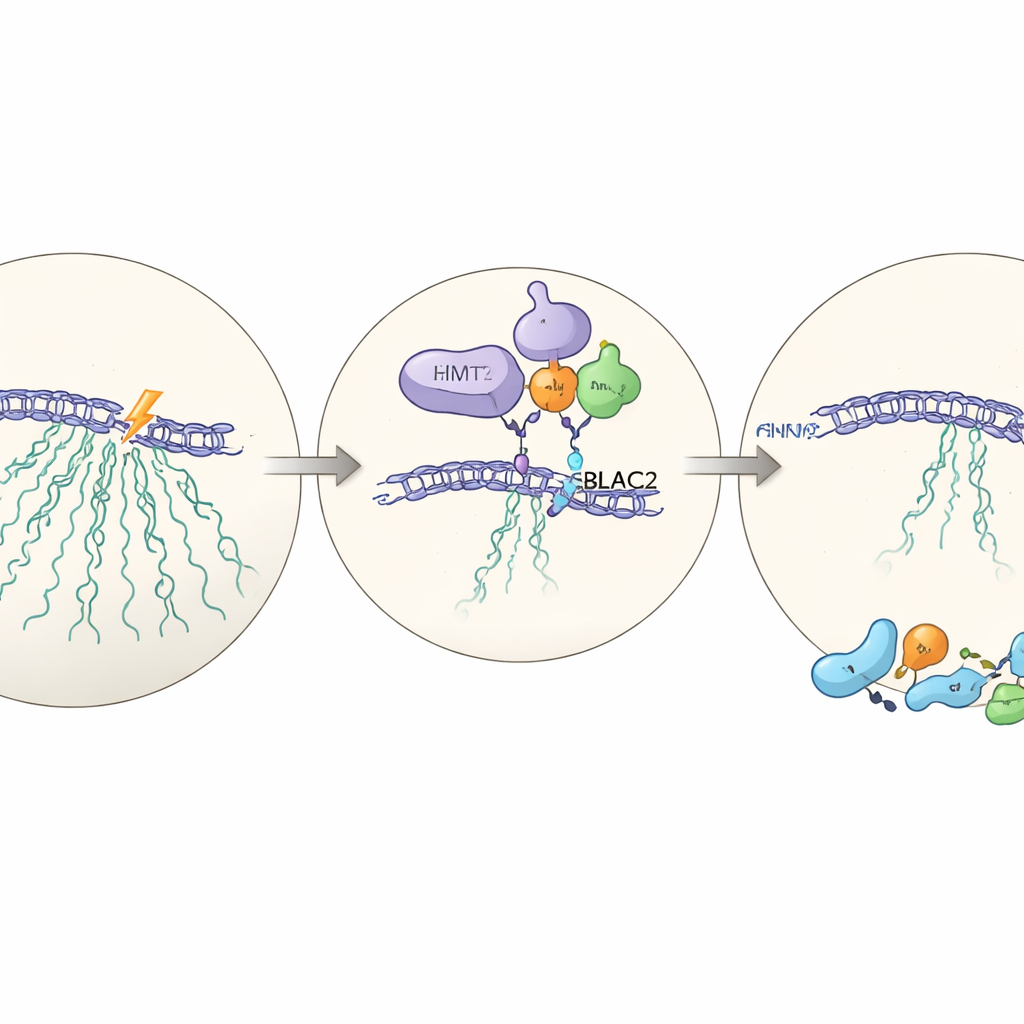
שותף חבוי: MBLAC2
למען הבנת האופן שבו EHMT2 מממש את השפעתו, הצוות מבצע מדידות חלבונים בקנה מידה גדול בתאים עם EHMT2 וללאו. בין החלבונים שמצטמצמים בהיעדר EHMT2, אחד בולט במיוחד: MBLAC2, אנזים מועט מחקר שמצטבר בדרך כלל בגרעינית. כאשר MBLAC2 מופחת באמצעות כלים מותאמי RNA, התאים שוב נכשלו להשתיק את ה‑rDNA לאחר נזק והפכו לפחות עמידים לו. EHMT2 נקשר פיזית ל‑MBLAC2 ומייצב אותו ברמת החלבון; בלי EHMT2, MBLAC2 מתפרק מהר יותר. הסרת שני החלבונים יחד לא מחמירה את ההשפעה מעבר להסרת אחד מהם, מה שמעיד שהם פועלים באותו מסלול — ציר EHMT2–MBLAC2 שתיאר המחקר, שמקשר בין עצירת השעתוק לתיקון יעיל.
מ‑DNA פגוע לסרטן המעי הגס
מכיוון שחוסר יציבות ב‑rDNA הוא אות היכר של גידולים רבים, המחברים בדקו האם הציר משחק תפקיד בסרטן המעי הגס, מחלה שתלויה במידה רבה בהגברה של ייצור ריבוזומים. במודלים עכבריים ובמדגמי גידול אנושיים, גם EHMT2 וגם MBLAC2 נמצאים בעמדה גבוהה יותר בגידולי מעי גס מאשר ברקמה קולונית תקינה, במקביל לסמנים של ייצור ריבוזומים מוגבר. דיכוי EHMT2 בתאי סרטן המעי הגס מאט את גדילת הגידולים בעכברים, מפחית סמנים הקשורים לריבוזום ומוריד רמות של MBLAC2. נתוני מטופלים ממאגר The Cancer Genome Atlas מראים שביטוי גבוה של שני הגנים מקושר למחלה מתקדמת יותר ולהישרדות נמוכה יותר לאחר הקרנות. יחד, התצפיות האלה מרמזות שתאי הסרטן עשויים לחטוף את מסלול EHMT2–MBLAC2 כדי להתמודד טוב יותר עם נזק ב‑rDNA ולשמר תפוקת ריבוזומים הנדרשת לצמיחה בלתי מוגבלת.
מסקנות לשירות הבריאות והטיפול
לקורא שאינו מומחה, המסר המרכזי הוא שתאינו פיתחו בלם חירום ייעודי בתוך הגרעינית: כאשר שבר נוצר בתוכנית ה‑DNA לריבוזומים, EHMT2 ושותפו MBLAC2 מסייעים להשהות את המפעל, לכוון את התיקון ולהשיב יציבות. כאשר הבלם הזה פעיל מדי או מנוצל לרעת המארח בסרטן המעי הגס, נראה שהוא מסייע לתאי הגידול לשרוד מתח וטיפול. על‑ידי מיקוד EHMT2, MBLAC2 או האינטראקציה ביניהם, טיפולים עתידיים עשויים להחליש באופן סלקטיבי את יכולת תאי הסרטן להתמודד עם נזק ל‑rDNA, ולשפר את היעילות של טיפולים סטנדרטיים כמו כימותרפיה והקרנות תוך שמירה על רקמה בריאה.
ציטוט: Wang, C., Lu, Q., Cao, L. et al. The EHMT2-MBLAC2 axis suppresses ribosomal DNA transcription in response to nucleolar DNA damage. Cell Death Dis 17, 320 (2026). https://doi.org/10.1038/s41419-026-08616-1
מילות מפתח: פגיעה ב‑DNA ריבוזומלי, מתח גרעינתי, מסלול EHMT2 MBLAC2, סרטן המעי הגס, תיקון DNA ושעתוק