Clear Sky Science · es
El eje EHMT2-MBLAC2 suprime la transcripción del ADN ribosomal en respuesta al daño del nucleolo
Por qué las fábricas de proteínas de la célula necesitan protección
En el interior de cada una de nuestras células hay un taller bullicioso llamado nucleolo, donde se ensamblan las máquinas moleculares que fabrican proteínas —los ribosomas—. Como esta fábrica funciona casi sin pausa, su ADN molde está sometido a estrés constante y puede romperse. El estudio descrito en este artículo explora cómo las células silencian temporalmente esta fábrica para reparar el daño, y cómo la falla de este sistema de seguridad puede contribuir al desarrollo del cáncer colorrectal.
Un tramo de ADN vulnerable
Los ribosomas se ensamblan usando las instrucciones codificadas en segmentos especiales de ADN conocidos como ADN ribosomal (ADNr). Estas secuencias se repiten muchas veces y se copian a gran velocidad, lo que las hace especialmente propensas a rupturas de doble cadena peligrosas. Cuando ocurren estas roturas en el ADNr, las células hacen más que reparar el ADN: también reorganizan el nucleolo y detienen brevemente la copia del ADNr a ARN. Esta pausa evita que las máquinas de reparación choquen con la maquinaria de transcripción y ayuda a mantener el número y la estructura de las repeticiones de ADNr estables—una salvaguarda importante, porque la inestabilidad del ADNr se ha vinculado al envejecimiento y a muchas enfermedades, incluido el cáncer.
Un nuevo interruptor de seguridad en el nucleolo
Los investigadores identifican una proteína llamada EHMT2, más conocida por modificar la cromatina en otras partes del genoma, como una pieza clave en esta respuesta de seguridad nucleolar. Usando un sistema en células humanas que corta el ADNr en sitios definidos, muestran que EHMT2 acude a la periferia del nucleolo donde el ADNr dañado se agrupa en estructuras llamadas «caps» (tapas). Allí, EHMT2 es necesario para apagar la producción de ARN ribosómico tras el daño. Cuando falta EHMT2 o su actividad se bloquea químicamente, las células continúan transcribiendo el ADNr a pesar de las roturas. El equipo rastrea este efecto hasta la capacidad de EHMT2 para añadir una marca química específica a las histonas en el ADNr dañado, contribuyendo a crear un estado de cromatina más reprimido.
Relacionando la pausa de la transcripción con la reparación del ADN
Silenciar el ADNr es solo la mitad de la historia; debe seguir una reparación eficaz. Los autores encuentran que las células sin EHMT2 tienen dificultades para reparar las roturas en ADNr: los fragmentos de ADN persisten más tiempo, aparecen con más frecuencia pequeños núcleos extra (una señal de inestabilidad genómica), y el número de copias de ADNr disminuye con el tiempo. De manera importante, una vía de reparación principal—la unión directa de extremos (non-homologous end joining), que vuelve a sellar los extremos del ADN rápidamente—no se recluta correctamente en los caps del ADNr sin EHMT2, aunque otras rutas de reparación permanecen en gran medida intactas. Como resultado, las células deficientes en EHMT2 se vuelven hipersensibles al daño nucleolar y pierden su capacidad de formar colonias sanas tras el corte del ADNr.
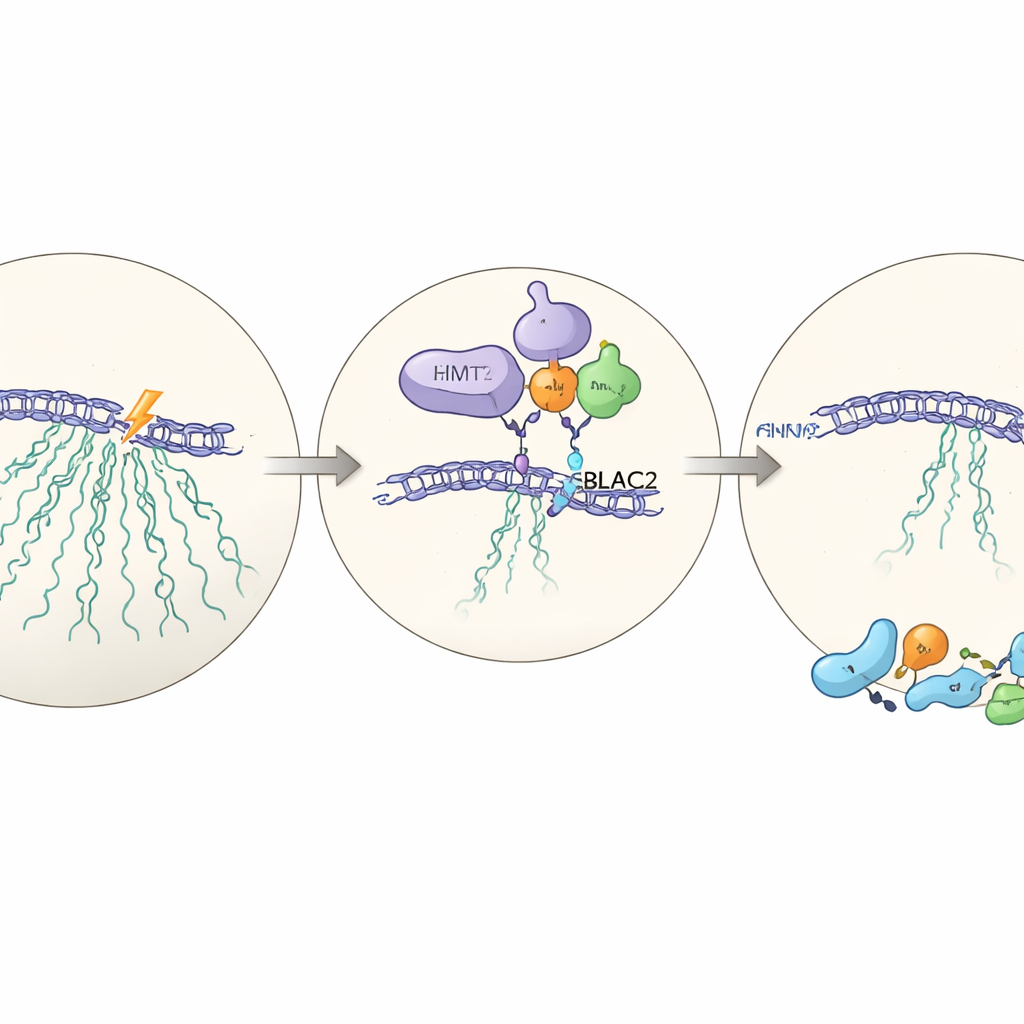
Un socio oculto: MBLAC2
Para entender cómo EHMT2 ejerce su influencia, el equipo realiza mediciones proteicas a gran escala en células con y sin EHMT2. Entre las proteínas que disminuyen cuando EHMT2 está ausente, destaca una: MBLAC2, una enzima poco estudiada que normalmente está enriquecida en el nucleolo. Cuando MBLAC2 se reduce con herramientas de ARN dirigidas, las células vuelven a fallar en silenciar el ADNr tras el daño y se vuelven menos capaces de sobrevivir. EHMT2 se une físicamente a MBLAC2 y la estabiliza a nivel proteico; sin EHMT2, MBLAC2 se degrada más rápido. La eliminación de ambas proteínas no empeora el efecto más allá de la eliminación de una sola, lo que sugiere que actúan en la misma vía—un eje EHMT2–MBLAC2 recién descrito que coordina la pausa de la transcripción con una reparación eficaz.
Del ADN dañado al cáncer colorrectal
Dado que la inestabilidad del ADNr es una característica de muchos tumores, los autores preguntan si este eje desempeña un papel en el cáncer colorrectal, una enfermedad que depende en gran medida del aumento de la producción de ribosomas. En modelos de ratón y en muestras de tumores humanos, tanto EHMT2 como MBLAC2 son consistentemente más abundantes en tumores colorrectales que en tejido de colon normal, en paralelo con marcadores de una mayor formación de ribosomas. Suprimir EHMT2 en células de cáncer colorrectal ralentiza el crecimiento de tumores en ratones, reduce los marcadores relacionados con ribosomas y disminuye los niveles de MBLAC2. Datos de pacientes del Cancer Genome Atlas revelan que la mayor expresión de ambos genes se asocia con enfermedad más avanzada y peor supervivencia tras la radioterapia. En conjunto, estas observaciones sugieren que las células cancerosas pueden secuestrar la vía EHMT2–MBLAC2 para tolerar mejor el daño en el ADNr y mantener la producción de ribosomas necesaria para el crecimiento descontrolado.
Qué significa esto para la salud y la terapia
Para un lector no especializado, el mensaje clave es que nuestras células han desarrollado un freno de emergencia dedicado dentro del nucleolo: cuando se rompe el plano de ADN para los ribosomas, EHMT2 y su socio MBLAC2 ayudan a pausar la fábrica, guiar la reparación y restaurar la estabilidad. Cuando este freno está sobreactivado o se utiliza indebidamente en el cáncer colorrectal, parece ayudar a las células tumorales a sobrevivir al estrés y al tratamiento. Al dirigirse a EHMT2, MBLAC2 o su interacción, futuras terapias podrían debilitar selectivamente la capacidad de las células cancerosas para afrontar el daño del ADN ribosomal, haciendo que tratamientos estándar como la quimioterapia y la radioterapia sean más eficaces al tiempo que se preserva el tejido normal.
Cita: Wang, C., Lu, Q., Cao, L. et al. The EHMT2-MBLAC2 axis suppresses ribosomal DNA transcription in response to nucleolar DNA damage. Cell Death Dis 17, 320 (2026). https://doi.org/10.1038/s41419-026-08616-1
Palabras clave: daño en el ADN ribosomal, estrés nucleolar, vía EHMT2 MBLAC2, cáncer colorrectal, reparación del ADN y transcripción