Clear Sky Science · ru
Ось EHMT2–MBLAC2 подавляет транскрипцию рибосомной ДНК в ответ на повреждение нуклеолярной ДНК
Почему фабрикам белка внутри клетки нужна защита
В каждой нашей клетке есть оживлённая мастерская — нуклеол, где собираются молекулярные машины для синтеза белка, рибосомы. Поскольку эта фабрика работает почти без перерыва, её ДНК-шаблон постоянно испытывает нагрузку и может ломаться. Исследование, описанное в этой статье, объясняет, как клетки временно притормаживают работу этой фабрики для ремонта повреждений и как сбой этой системы безопасности может способствовать развитию колоректального рака.
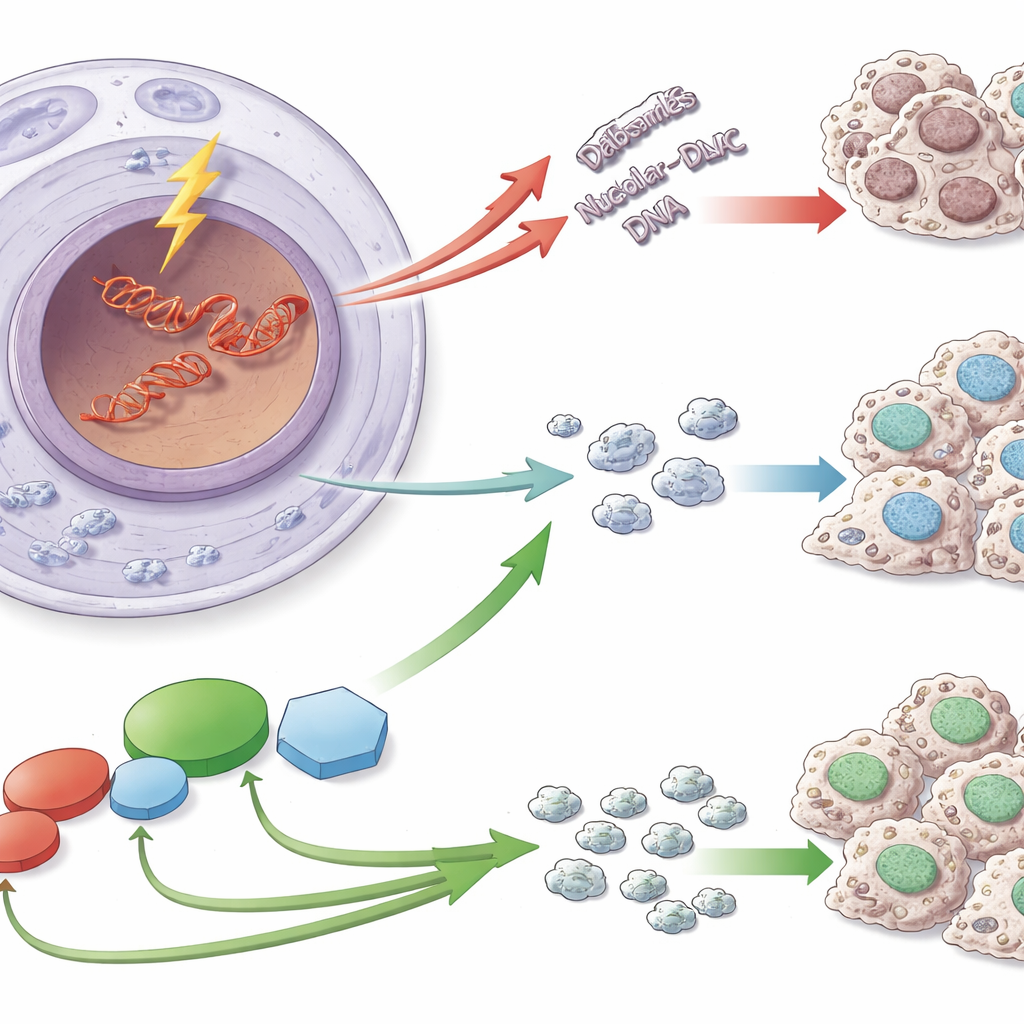
Уязвимый участок ДНК
Рибосомы собираются по инструкциям, записанным в специальных сегментах ДНК — рибосомной ДНК (rDNA). Эти последовательности многократно повторяются и копируются очень быстро, что делает их особенно уязвимыми к опасным двухцепочечным разрывам. Когда такие разрывы возникают в rDNA, клетки делают не только ремонт: они также реорганизуют нуклеол и временно останавливают копирование rDNA в РНК. Эта пауза предотвращает столкновения репарационных комплексов с аппаратом транскрипции и помогает сохранять число и структуру повторов rDNA — важный механизм защиты, поскольку нестабильность rDNA связана со старением и множеством заболеваний, включая рак.
Новый переключатель безопасности в нуклеоле
Исследователи выявили белок EHMT2, более известный как модификатор хроматина в других частях генома, как ключевой элемент этой нуклеолярной ответной реакции. Используя систему в человеческих клетках, которая целенаправленно разрезает rDNA в заданных местах, они показали, что EHMT2 устремляется к краю нуклеола, где повреждённая rDNA собирается в структуры, называемые «кепы» (caps). Там EHMT2 необходим для остановки синтеза рибосомной РНК после повреждения. При отсутствии EHMT2 или при химическом блокировании его активности клетки продолжают транскрибировать rDNA несмотря на разрывы. Команда связывает этот эффект со способностью EHMT2 добавлять специфическую химическую метку на гистоны в повреждённой rDNA, способствуя формированию более репрессивного состояния хроматина.
Связь между паузой транскрипции и репарацией ДНК
Притушение rDNA — лишь половина дела; за ним должен последовать успешный ремонт. Авторы показывают, что клетки, лишённые EHMT2, испытывают трудности с восстановлением разрывов в rDNA: фрагменты ДНК дольше сохраняются, чаще появляются мелкие дополнительные ядра (признак геномной нестабильности), и со временем количество копий rDNA снижается. Важно, что один из основных путей репарации — не гомологичное объединение концов (NHEJ), которое быстро зашивает концы ДНК — не может правильно рекрутироваться в rDNA-кепы без EHMT2, хотя другие пути репарации в основном функционируют. В результате клетки, лишённые EHMT2, становятся гиперчувствительными к нуклеолярным повреждениям и теряют способность формировать жизнеспособные колонии после разрезания rDNA.
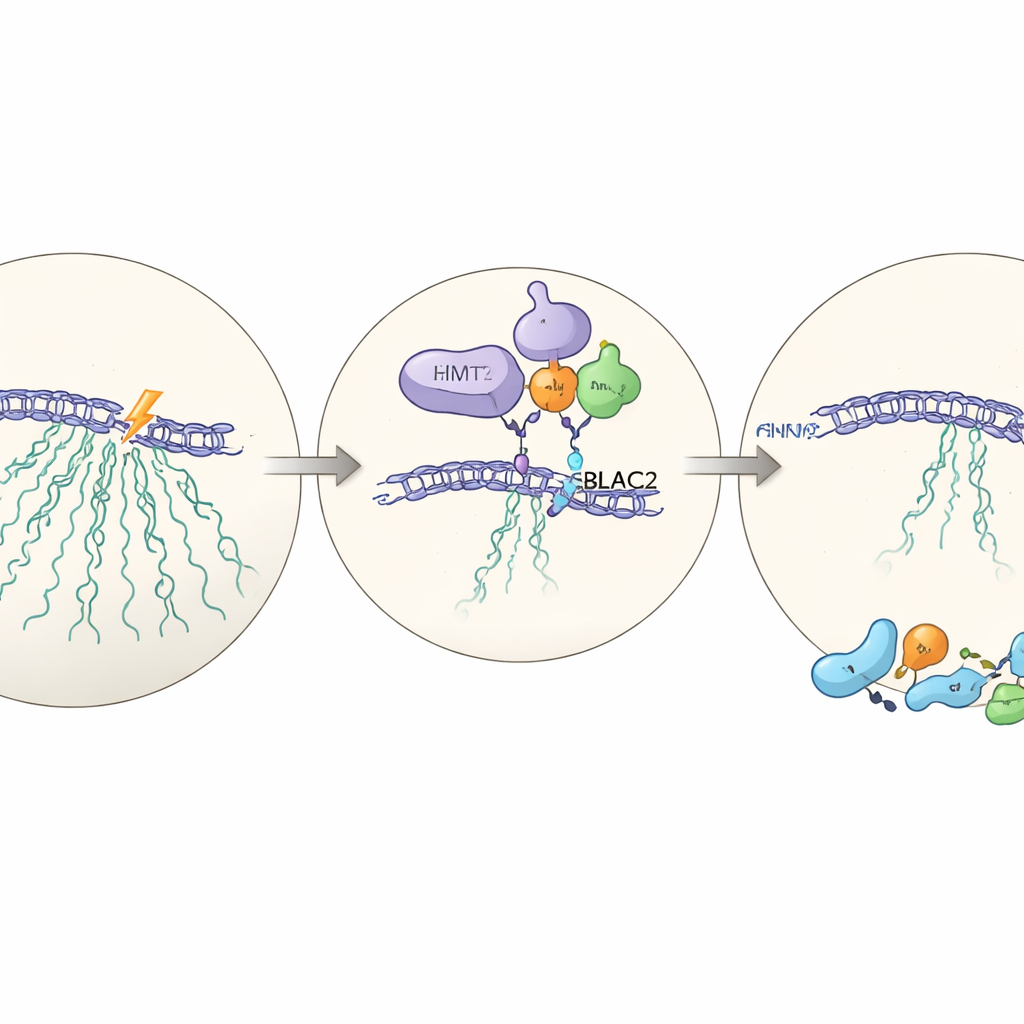
Скрытый партнёр: MBLAC2
Чтобы понять, как EHMT2 оказывает влияние, команда провела масштабные измерения белков в клетках с EHMT2 и без него. Среди белков, уровни которых падают при отсутствии EHMT2, выделился один: MBLAC2, малоизученный фермент, обычно обогащённый в нуклеоле. При снижении уровня MBLAC2 с помощью направленных РНК-инструментов клетки снова не могут заглушить транскрипцию rDNA после повреждения и хуже выживают. EHMT2 физически связывается с MBLAC2 и стабилизирует его на уровне белка; при отсутствии EHMT2 MBLAC2 разрушается быстрее. Удаление обоих белков не усугубляет эффект по сравнению с удалением одного, что указывает на их работу в одном и том же пути — недавно описанной оси EHMT2–MBLAC2, координирующей паузу транскрипции с эффективным ремонтом.
От повреждённой ДНК к колоректальному раку
Поскольку нестабильность rDNA является отличительной чертой многих опухолей, авторы изучили, играет ли эта ось роль в колоректальном раке — заболевании, сильно зависящем от повышенного производства рибосом. В моделях на мышах и в образцах человеческих опухолей EHMT2 и MBLAC2 с consistently большей интенсивностью экспрессируются в колоректальных опухолях по сравнению с нормальной тканью толстой кишки, параллельно маркерам усиленного образования рибосом. Подавление EHMT2 в клетках колоректального рака замедляет рост опухолей у мышей, снижает маркеры, связанные с рибосомами, и понижает уровни MBLAC2. Клинические данные из The Cancer Genome Atlas показывают, что повышенная экспрессия обоих генов связана с более продвинутой стадией заболевания и худшей выживаемостью после радиотерапии. В совокупности эти наблюдения свидетельствуют о том, что раковые клетки могут использовать ось EHMT2–MBLAC2, чтобы лучше переносить повреждения rDNA и поддерживать выпуск рибосом, необходимый для неконтролируемого роста.
Что это значит для здоровья и терапии
Для неспециалиста ключевая мысль такова: наши клетки выработали специальный аварийный тормоз внутри нуклеола — когда ломается ДНК-шаблон рибосом, EHMT2 и его партнёр MBLAC2 помогают приостановить фабрику, направить ремонт и восстановить стабильность. Когда этот тормоз гиперактивен или используется не по назначению в колоректальном раке, он, по-видимому, помогает опухолевым клеткам переживать стресс и лечение. Прицельное воздействие на EHMT2, MBLAC2 или их взаимодействие может в будущем выборочно ослаблять способность раковых клеток справляться с повреждениями рибосомной ДНК, делая стандартные терапии, такие как химио- и радиотерапия, более эффективными при относительном сохранении нормальных тканей.
Цитирование: Wang, C., Lu, Q., Cao, L. et al. The EHMT2-MBLAC2 axis suppresses ribosomal DNA transcription in response to nucleolar DNA damage. Cell Death Dis 17, 320 (2026). https://doi.org/10.1038/s41419-026-08616-1
Ключевые слова: повреждение рибосомной ДНК, нуклеолярный стресс, путь EHMT2 MBLAC2, колоректальный рак, репарация ДНК и транскрипция