Clear Sky Science · ar
محور EHMT2-MBLAC2 يكبح نسخ حمض الريبي النووي الريبوزي استجابةً لضرر الحمض النووي النووي
لماذا تحتاج مصانع البروتين داخل الخلية إلى حماية
داخل كل خلية منا يوجد مشغل حيوي يُدعى النوية، حيث تُبنى الآليات الجزيئية التي تصنع البروتينات — الريبوسومات. وبما أن هذا المصنع يعمل تقريبًا دون انقطاع، فإن قالب الحمض النووي الخاص به يتعرَّض لضغط مستمر ويمكن أن ينكسر. تستعرض الدراسة الواردة في هذا المقال كيف تُخمد الخلايا هذا المصنع مؤقتًا لإصلاح الضرر، وكيف أن فشل هذه الآلية الوقائية قد يساهم في دفع تطور سرطان القولون والمستقيم.
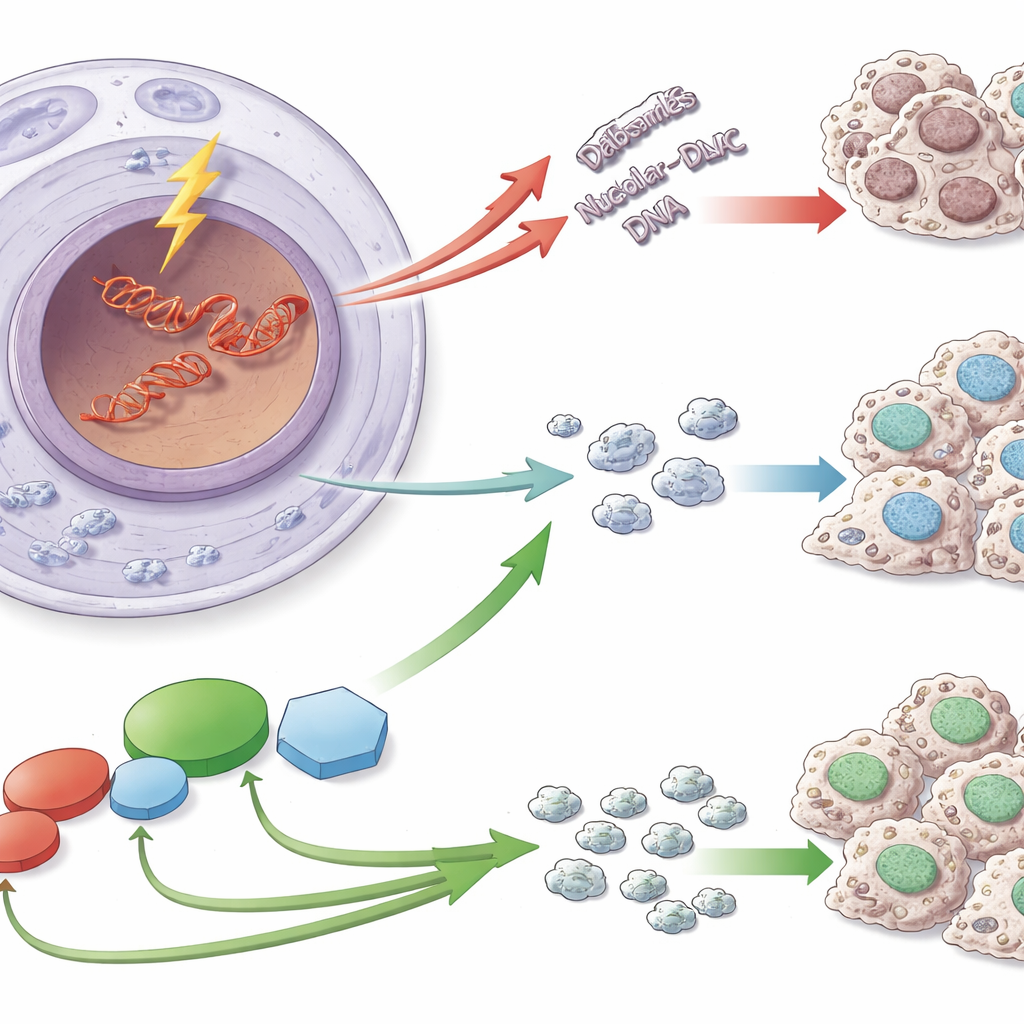
مقطع من الحمض النووي عرضة للخطر
تُجمَّع الريبوسومات باستخدام تعليمات مشفرة في مقاطع خاصة من الحمض النووي تُعرف بالحِمض النووي الريبوزي الريباسي (rDNA). هذه التسلسلات متكررة عدة مرات وتُنسخ بسرعة عالية، مما يجعلها عُرضة بشكل خاص لحدوث كسور مزدوجة الخطورة. عندما تحدث مثل هذه الكسور في rDNA، تفعل الخلايا أكثر من مجرد رقع الحمض النووي: فهي تعيد تنظيم النوية وتوقف مؤقتًا عملية نسخ rDNA إلى RNA. تمنع هذه الوقفة اصطدام آلات الإصلاح بآليات النسخ وتُسهم في الحفاظ على عدد وبنية تكرارات rDNA — وهو حاجز أمان مهم، لأن عدم استقرار rDNA رُبط بالشيخوخة والعديد من الأمراض بما في ذلك السرطان.
مفتاح أمان جديد في النوية
حدَّد الباحثون بروتينًا يُدعى EHMT2، المعروف أكثر بتعديله للكروماتين في أجزاء أخرى من الجينوم، كلاعب أساسي في استجابة الأمان هذه داخل النوية. باستخدام نظام في خلايا بشرية يقطع rDNA في مواقع محددة، يُظهرون أن EHMT2 يتسارع إلى حافة النوية حيث تُجمَع شظايا rDNA المتضررة في هياكل تُسمى القِبَب. هناك، يكون EHMT2 ضروريًا لإيقاف إنتاج الحمض النووي الريبي الريباسي بعد الضرر. عندما يغيب EHMT2 أو تُثبَّطُ نشاطاته كيميائيًا، تواصل الخلايا نسخ rDNA رغم الكسور. يعود هذا التأثير إلى قدرة EHMT2 على إضافة علامة كيميائية محددة إلى بروتينات الهيستون في rDNA المتضرر، مما يساعد على تكوين حالة كروماتين أكثر قمعًا.
ربط وقفة النسخ بإصلاح الحمض النووي
تهدئة rDNA ليست سوى نصف القصة؛ فالإصلاح الناجح يجب أن يتبعها. يجد المؤلفون أن الخلايا التي تفتقر إلى EHMT2 تكافح لإصلاح كسور rDNA: تبقى شظايا الحمض النووي لفترة أطول، وتظهر نوى صغيرة إضافية (علامة على عدم استقرار جينومي) بتواتر أعلى، وينخفض عدد نسخ rDNA مع الوقت. والأهم من ذلك أن مسار إصلاح رئيسيًا — هو الانضمام النهائي غير المتجانس (NHEJ)، الذي يُعيد إغلاق نهايات الحمض النووي بسرعة — يفشل في الانجذاب بشكل صحيح إلى قِبَب rDNA بدون EHMT2، رغم أن مسارات إصلاح أخرى تظل إلى حد كبير سليمة. ونتيجة لذلك، تصبح الخلايا الناقصة EHMT2 فائقة الحساسية تجاه ضرر النوية وتفقد قدرتها على تكوين مستعمرات صحية بعد قطع rDNA.
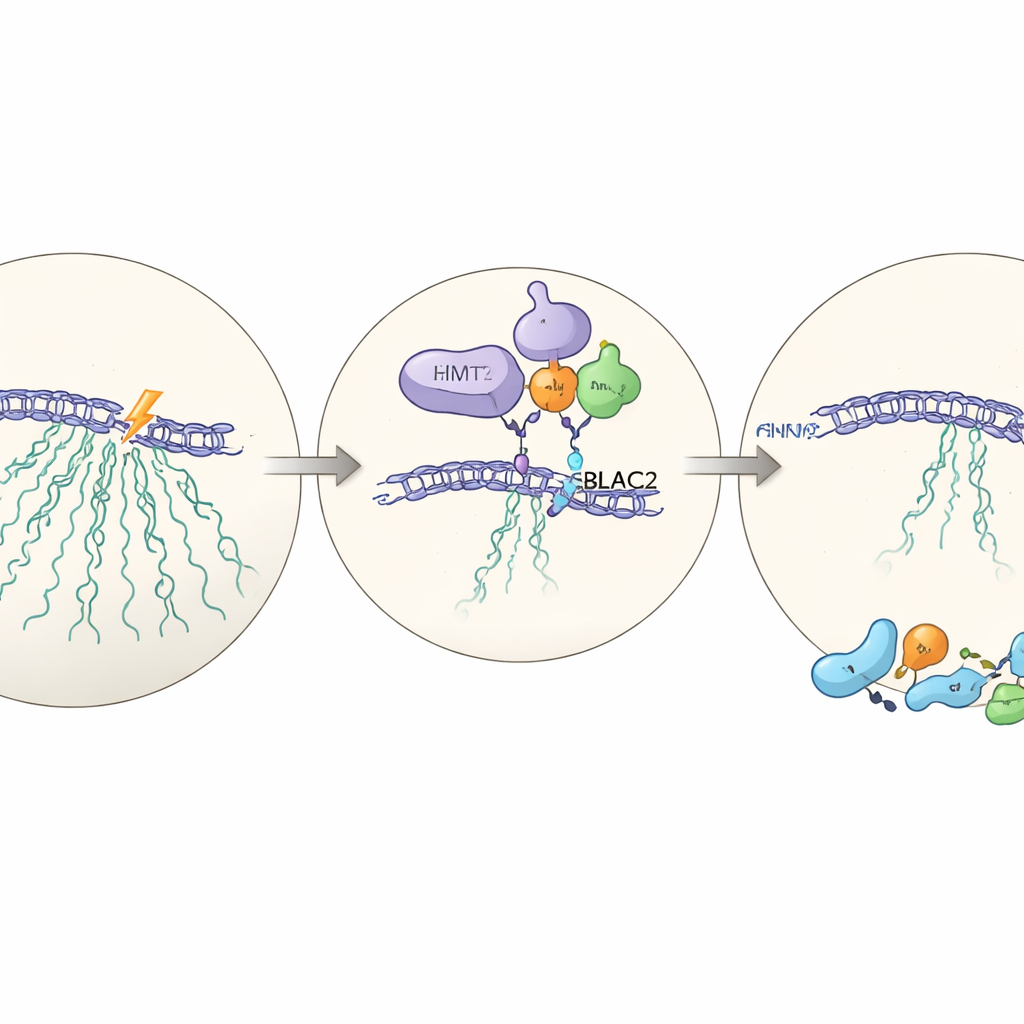
شريك مخفي: MBLAC2
لفهم كيف يمارس EHMT2 تأثيره، أجرى الفريق قياسات بروتينية واسعة النطاق في خلايا مع وبدون EHMT2. من بين البروتينات التي تنخفض عند غياب EHMT2، يبرز واحد: MBLAC2، إنزيم قليل الدراسة يتواجد عادةً بتركيز أعلى في النوية. عندما تُقلَّل مستويات MBLAC2 بأدوات RNA المستهدفة، تفشل الخلايا مجدداً في إخماد rDNA بعد الضرر وتصبح أقل قدرة على النجاة منه. يرتبط EHMT2 جسديًا بـ MBLAC2 ويُثبِّته على مستوى البروتين؛ بدون EHMT2 يُتحلَّل MBLAC2 بسرعة أكبر. وإزالة كلا البروتينين لا تزيد التأثير سوءًا مقارنة بإزالة أحدهما فحسب، مما يشير إلى أنهما يعملان في نفس المسار — محور EHMT2–MBLAC2 الموصوف حديثًا الذي ينسق وقفة النسخ مع الإصلاح الفعّال.
من الحمض النووي المتضرر إلى سرطان القولون والمستقيم
نظرًا لأن عدم استقرار rDNA علامة مميزة للعديد من الأورام، يسأل المؤلفون ما إذا كان لهذا المحور دور في سرطان القولون والمستقيم، وهو مرض يعتمد بدرجة كبيرة على زيادة إنتاج الريبوسومات. في نماذج الفئران وعينات الأورام البشرية، يُظهر كل من EHMT2 وMBLAC2 وفرة أعلى باستمرار في أورام القولون مقارنةً بالنسيج القولوني الطبيعي، بالتوازي مع علامات على تعزيز تشكّل الريبوسومات. يؤدي كبح EHMT2 في خلايا سرطان القولون والمستقيم إلى إبطاء نمو الأورام في الفئران، وتقليل مؤشرات المرتبطة بالريبوسومات، وخفض مستويات MBLAC2. تكشف بيانات المرضى من مشروع جينوم السرطان أن التعبير الأعلى عن كلا الجينين يرتبط بمرض أكثر تقدمًا وبنجاة أسوأ بعد العلاج الإشعاعي. معًا، تشير هذه الملاحظات إلى أن خلايا السرطان قد تستغل محور EHMT2–MBLAC2 لتحمّل ضرر rDNA بشكل أفضل والحفاظ على إنتاج الريبوسومات اللازم للنمو غير المنضبط.
ما يعنيه هذا للصحة والعلاج
للقارئ غير المتخصص، الرسالة الأساسية هي أن خلايانا طوَّرت فرامل طوارئ مخصّصة داخل النوية: عندما ينكسر قالب الحمض النووي لصنع الريبوسومات، يساعد EHMT2 وشريكه MBLAC2 في إيقاف المصنع مؤقتًا، وتوجيه الإصلاح، واستعادة الاستقرار. عندما تكون هذه الفرملة مفرطة النشاط أو يُساء استخدامها في سرطان القولون والمستقيم، يبدو أنها تساعد الخلايا الورمية على تحمل الضغوط والعلاج. من خلال استهداف EHMT2 أو MBLAC2 أو تفاعلهما، قد تضعف العلاجات المستقبلية قدرة خلايا السرطان على التعامل مع ضرر حمض الريبي النووي الريبوزي بشكل انتقائي، مما يجعل العلاجات القياسية مثل العلاج الكيميائي والإشعاعي أكثر فاعلية مع الحفاظ على الأنسجة السليمة.
الاستشهاد: Wang, C., Lu, Q., Cao, L. et al. The EHMT2-MBLAC2 axis suppresses ribosomal DNA transcription in response to nucleolar DNA damage. Cell Death Dis 17, 320 (2026). https://doi.org/10.1038/s41419-026-08616-1
الكلمات المفتاحية: ضرر حمض الريبي النووي الريبوزي, إجهاد النوية, مسار EHMT2 MBLAC2, سرطان القولون والمستقيم, إصلاح الحمض النووي والنسخ