Clear Sky Science · fr
L’axe EHMT2–MBLAC2 réprime la transcription de l’ADN ribosomique en réponse aux lésions de l’ADN nucléolaire
Pourquoi les usines à protéines de la cellule doivent être protégées
À l’intérieur de chacune de nos cellules se trouve un atelier animé appelé nucléole, où sont assemblées les machines moléculaires qui fabriquent les protéines — les ribosomes. Parce que cette usine fonctionne presque sans interruption, son modèle d’ADN est soumis à une tension constante et peut se rompre. L’étude présentée ici explore la manière dont les cellules mettent temporairement cette usine en pause pour réparer les dégâts, et comment la défaillance de ce système de sécurité peut favoriser le développement du cancer colorectal.
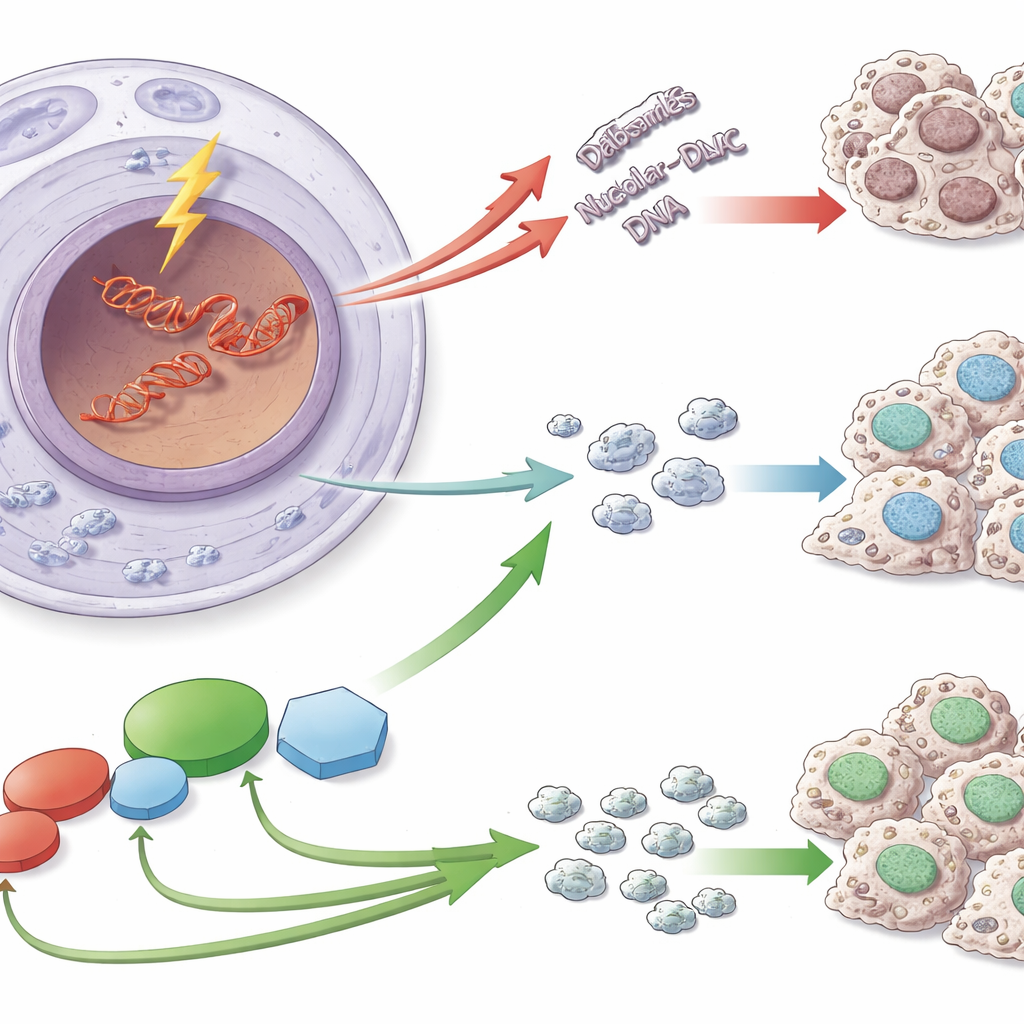
Une tranche d’ADN vulnérable
Les ribosomes sont assemblés à partir d’instructions codées dans des segments d’ADN particuliers appelés ADN ribosomique (ADNr). Ces séquences sont répétées de nombreuses fois et sont copiées à très grande vitesse, ce qui les rend particulièrement sujettes aux cassures double-brin dangereuses. Lorsqu’un tel bris survient dans l’ADNr, la cellule ne se contente pas de recoller l’ADN : elle réorganise aussi le nucléole et interrompt brièvement la transcription de l’ADNr en ARN. Cette pause empêche les machines de réparation de heurter la machinerie de transcription et contribue à maintenir stables le nombre et la structure des répétitions d’ADNr — une protection importante, car l’instabilité de l’ADNr a été liée au vieillissement et à de nombreuses maladies, dont le cancer.
Un nouveau commutateur de sécurité dans le nucléole
Les chercheurs identifient une protéine nommée EHMT2, mieux connue pour modifier la chromatine ailleurs dans le génome, comme un acteur crucial de cette réponse de sécurité nucléolaire. À l’aide d’un système dans des cellules humaines qui coupe l’ADNr en sites définis, ils montrent que EHMT2 se précipite vers le bord du nucléole où l’ADNr endommagé est rassemblé en structures appelées calottes. Là, EHMT2 est nécessaire pour arrêter la production d’ARN ribosomique après une lésion. Quand EHMT2 manque ou que son activité est bloquée chimiquement, les cellules continuent de transcrire l’ADNr malgré les cassures. L’équipe relie cet effet à la capacité d’EHMT2 d’ajouter une marque chimique spécifique aux histones au niveau de l’ADNr endommagé, contribuant à instaurer un état de chromatine plus réprimé.
Relier la pause transcriptionnelle à la réparation de l’ADN
Mettre l’ADNr au repos n’est que la moitié de l’histoire ; il faut ensuite réparer correctement. Les auteurs constatent que les cellules dépourvues d’EHMT2 ont du mal à réparer les cassures d’ADNr : des fragments d’ADN persistent plus longtemps, des micronoyaux (signe d’instabilité génomique) apparaissent plus fréquemment, et le nombre de copies d’ADNr décline avec le temps. De manière importante, une voie majeure de réparation — la jonction d’extrémités non homologues (NHEJ), qui recolle rapidement les bouts d’ADN — n’est pas correctement recrutée aux calottes d’ADNr en l’absence d’EHMT2, alors que d’autres voies de réparation restent globalement fonctionnelles. En conséquence, les cellules déficientes en EHMT2 deviennent hypersensibles aux lésions nucléolaires et perdent leur capacité à former des colonies saines après la coupure de l’ADNr.
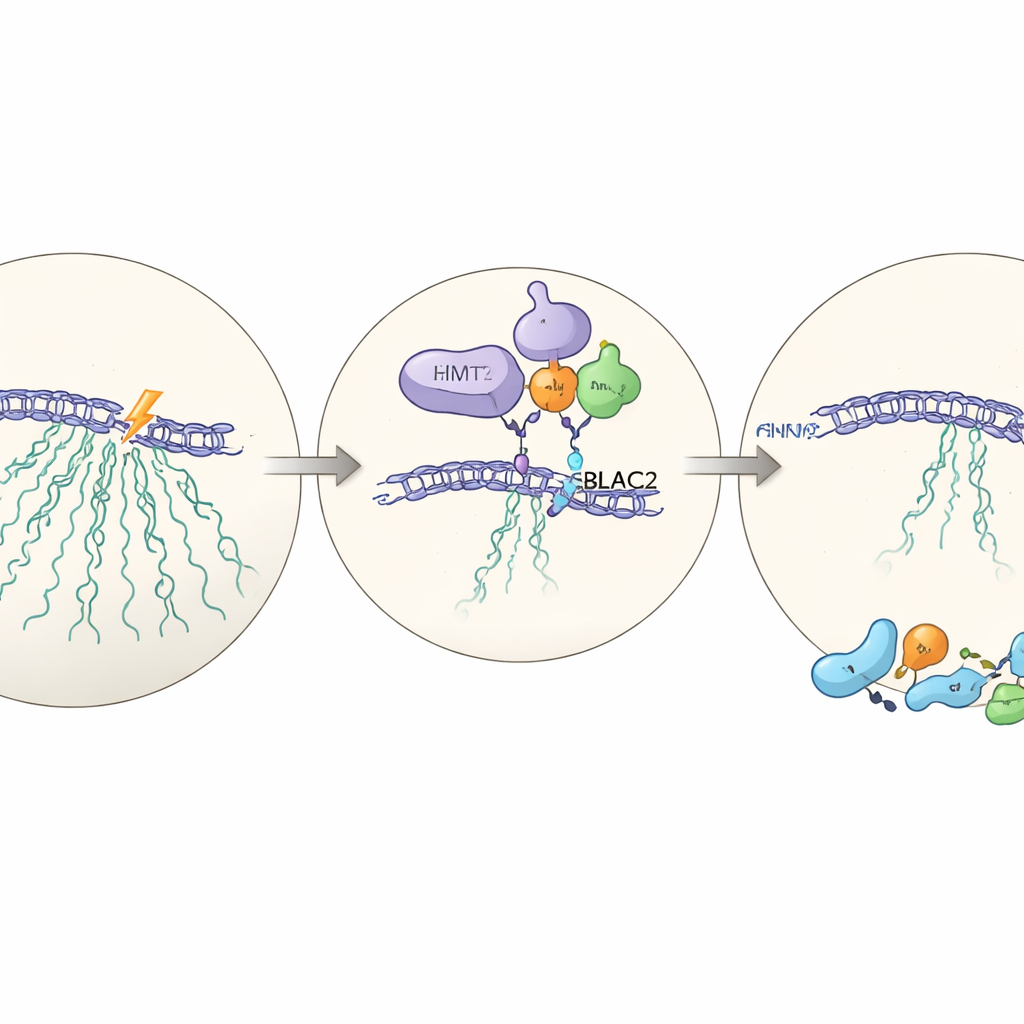
Un partenaire caché : MBLAC2
Pour comprendre comment EHMT2 exerce son influence, l’équipe réalise des mesures protéomiques à grande échelle dans des cellules avec ou sans EHMT2. Parmi les protéines qui diminuent en l’absence d’EHMT2, une se détache : MBLAC2, une enzyme peu étudiée normalement enrichie dans le nucléole. Lorsque MBLAC2 est réduite par des outils d’ARN ciblés, les cellules échouent à nouveau à silencer l’ADNr après dommage et deviennent moins aptes à y survivre. EHMT2 se lie physiquement à MBLAC2 et la stabilise au niveau protéique ; sans EHMT2, MBLAC2 est dégradée plus rapidement. L’élimination des deux protéines n’aggrave pas l’effet au-delà de la suppression d’une seule, ce qui suggère qu’elles agissent dans la même voie — un axe EHMT2–MBLAC2 nouvellement décrit qui coordonne la pause transcriptionnelle avec une réparation efficace.
De l’ADN endommagé au cancer colorectal
Étant donné que l’instabilité de l’ADNr est une caractéristique de nombreuses tumeurs, les auteurs se demandent si cet axe joue un rôle dans le cancer colorectal, une maladie qui dépend fortement d’une production accrue de ribosomes. Chez la souris et dans des échantillons tumoraux humains, EHMT2 et MBLAC2 sont systématiquement plus abondants dans les tumeurs colorectales que dans le tissu colique normal, en parallèle avec des marqueurs d’augmentation de la formation des ribosomes. Supprimer EHMT2 dans des cellules de cancer colorectal ralentit la croissance tumorale chez la souris, réduit les marqueurs liés aux ribosomes et abaisse les niveaux de MBLAC2. Les données de patients issues du Cancer Genome Atlas révèlent qu’une expression élevée des deux gènes s’associe à une maladie plus avancée et à une survie plus mauvaise après radiothérapie. Ensemble, ces observations suggèrent que les cellules cancéreuses peuvent détourner la voie EHMT2–MBLAC2 pour mieux tolérer les dommages de l’ADNr et maintenir la production de ribosomes nécessaire à leur prolifération incontrôlée.
Ce que cela signifie pour la santé et la thérapie
Pour un lecteur non spécialiste, le message clé est que nos cellules ont évolué un frein d’urgence dédié à l’intérieur du nucléole : lorsque le plan d’assemblage des ribosomes se brise, EHMT2 et son partenaire MBLAC2 aident à mettre l’usine en pause, orienter la réparation et restaurer la stabilité. Quand ce frein est hyperactif ou détourné dans le cancer colorectal, il semble aider les cellules tumorales à survivre au stress et aux traitements. En ciblant EHMT2, MBLAC2 ou leur interaction, des thérapies futures pourraient affaiblir sélectivement la capacité des cellules cancéreuses à gérer les dommages de l’ADN ribosomique, rendant les traitements standards comme la chimiothérapie et la radiothérapie plus efficaces tout en épargnant les tissus normaux.
Citation: Wang, C., Lu, Q., Cao, L. et al. The EHMT2-MBLAC2 axis suppresses ribosomal DNA transcription in response to nucleolar DNA damage. Cell Death Dis 17, 320 (2026). https://doi.org/10.1038/s41419-026-08616-1
Mots-clés: dommages de l’ADN ribosomique, stress nucléolaire, voie EHMT2 MBLAC2, cancer colorectal, réparation de l’ADN et transcription