Clear Sky Science · de
Die EHMT2‑MBLAC2‑Achse unterdrückt die Transkription der ribosomalen DNA als Reaktion auf DNA‑Schäden im Nukleolus
Warum die Proteinfabriken der Zelle Schutz brauchen
Im Inneren jeder unserer Zellen befindet sich eine geschäftige Werkstatt, der Nukleolus, in dem die molekularen Maschinen zur Proteinsynthese – die Ribosomen – zusammengebaut werden. Weil diese Fabrik nahezu ununterbrochen arbeitet, steht ihre DNA‑Vorlage unter ständigem Stress und kann beschädigt werden. Die vorliegende Studie untersucht, wie Zellen diese Fabrik vorübergehend beruhigen, um Schäden zu reparieren, und wie ein Versagen dieses Sicherheitsmechanismus möglicherweise zur Entstehung von kolorektalem Krebs beitragen kann.
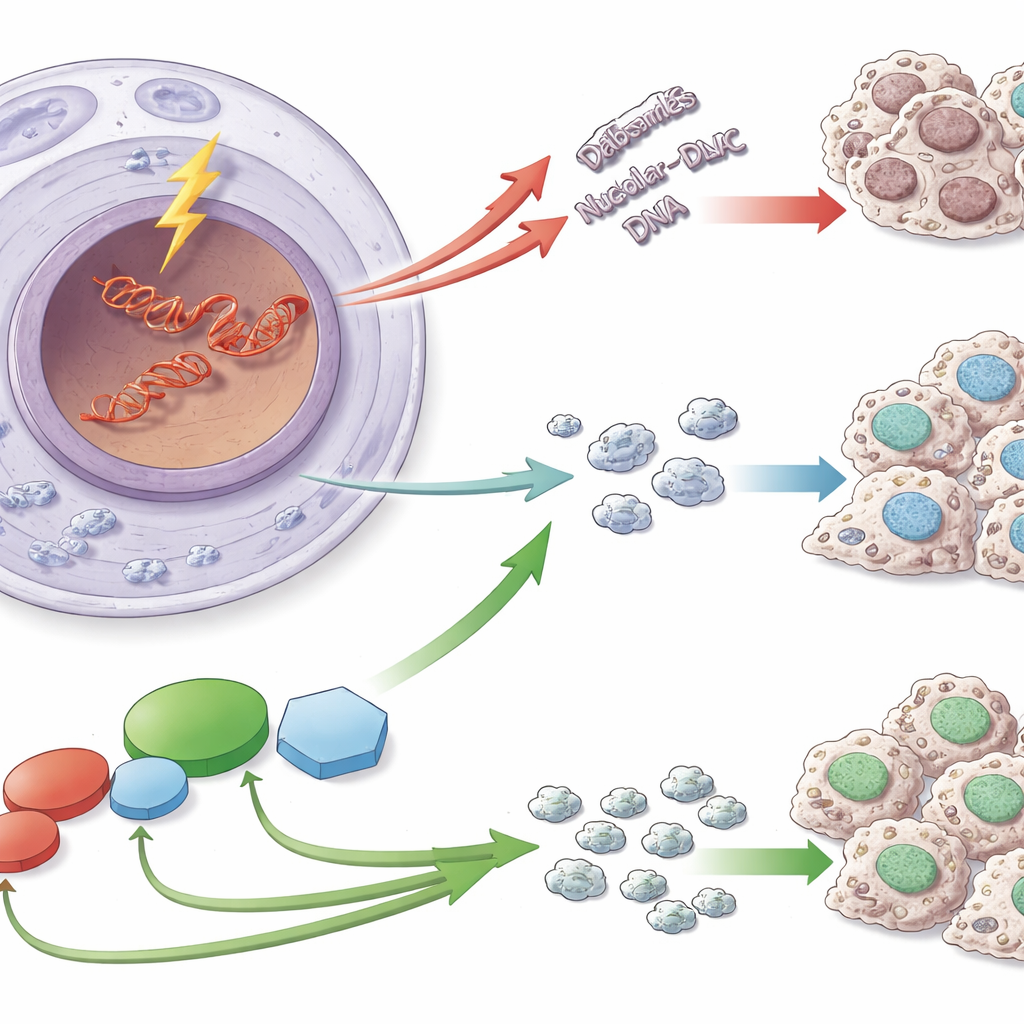
Ein verwundbarer DNA‑Abschnitt
Ribosomen werden mithilfe von Anweisungen zusammengesetzt, die in speziellen DNA‑Abschnitten codiert sind, den ribosomalen DNA‑Sequenzen (rDNA). Diese Sequenzen kommen vielfach vor und werden sehr schnell kopiert, wodurch sie besonders anfällig für gefährliche Doppelstrangbrüche sind. Wenn solche Brüche in der rDNA auftreten, unternehmen Zellen mehr als nur eine einfache Reparatur: Sie reorganisieren den Nukleolus und stellen vorübergehend das Abschreiben der rDNA zu RNA ein. Diese Pause verhindert, dass Reparatursysteme mit der Transkriptionsmaschinerie kollidieren, und trägt dazu bei, Zahl und Struktur der rDNA‑Wiederholungen stabil zu halten – ein wichtiger Schutzmechanismus, denn Instabilität der rDNA wurde mit Alterung und vielen Krankheiten, einschließlich Krebs, in Verbindung gebracht.
Ein neuer Sicherheitshebel im Nukleolus
Die Forscher identifizieren ein Protein namens EHMT2, das ansonsten dafür bekannt ist, Chromatin an anderen Stellen des Genoms zu modifizieren, als entscheidenden Akteur dieser nukleolaren Sicherheitsantwort. Mithilfe eines Systems in menschlichen Zellen, das die rDNA an definierten Stellen schneidet, zeigen sie, dass EHMT2 an den Rand des Nukleolus eilt, wo beschädigte rDNA in sogenannte Caps zusammengeführt wird. Dort ist EHMT2 erforderlich, um die Produktion von ribosomaler RNA nach einer Schädigung herunterzufahren. Fehlt EHMT2 oder ist seine Aktivität chemisch blockiert, transkribieren die Zellen die rDNA trotz der Brüche weiter. Das Team führt diesen Effekt auf die Fähigkeit von EHMT2 zurück, an beschädigter rDNA ein spezifisches chemisches Signal an Histonproteine anzubringen und so einen stärker repressiven Chromatinzustand zu schaffen.
Die Verbindung zwischen Transkriptionspause und DNA‑Reparatur
Das Beruhigen der rDNA ist nur die halbe Geschichte; auf die Pause muss eine erfolgreiche Reparatur folgen. Die Autoren stellen fest, dass Zellen ohne EHMT2 Schwierigkeiten haben, rDNA‑Brüche zu reparieren: DNA‑Fragmente bleiben länger bestehen, kleine zusätzliche Zellkerne (ein Zeichen genomischer Instabilität) treten häufiger auf, und die Anzahl der rDNA‑Kopien nimmt mit der Zeit ab. Wichtig ist, dass ein wesentlicher Reparaturweg – die nicht‑homologe Endverknüpfung (NHEJ), die DNA‑Enden schnell wieder verbindet – ohne EHMT2 nicht korrekt an rDNA‑Caps rekrutiert wird, während andere Reparaturwege weitgehend intakt bleiben. Infolgedessen werden EHMT2‑defiziente Zellen gegenüber nukleolaren Schäden hypersensibel und verlieren nach rDNA‑Schnitten die Fähigkeit, gesunde Kolonien zu bilden.
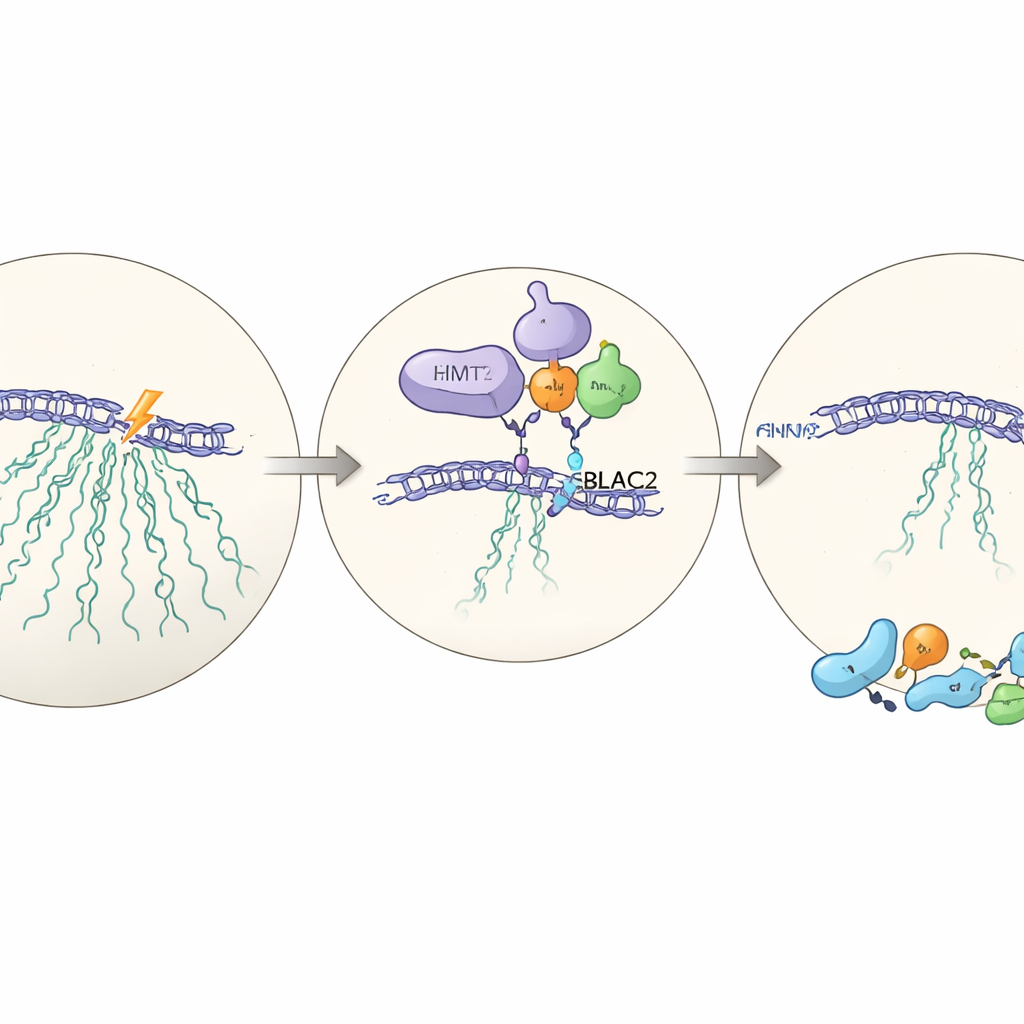
Ein versteckter Partner: MBLAC2
Um zu verstehen, wie EHMT2 seine Wirkung ausübt, führten die Forscher groß angelegte Proteinanalyse in Zellen mit und ohne EHMT2 durch. Unter den Proteinen, die bei Fehlen von EHMT2 abnehmen, sticht eines hervor: MBLAC2, ein wenig untersuchtes Enzym, das normalerweise im Nukleolus angereichert ist. Wird MBLAC2 mittels gezielter RNA‑Werkzeuge reduziert, schaffen es die Zellen ebenfalls nicht, die rDNA nach einer Schädigung zu stilllegen, und sind weniger überlebensfähig. EHMT2 bindet physisch an MBLAC2 und stabilisiert es auf Proteinebene; ohne EHMT2 wird MBLAC2 schneller abgebaut. Das Entfernen beider Proteine verschlechtert den Effekt nicht über das Entfernen eines einzelnen hinaus, was darauf hindeutet, dass sie im selben Weg wirken – eine neu beschriebene EHMT2–MBLAC2‑Achse, die die Transkriptionspause mit einer effektiven Reparatur koordiniert.
Von beschädigter DNA zum kolorektalen Krebs
Da rDNA‑Instabilität ein Kennzeichen vieler Tumoren ist, untersuchen die Autoren, ob diese Achse eine Rolle beim kolorektalen Krebs spielt, einer Erkrankung, die stark von erhöhter Ribosomenproduktion abhängt. In Mausmodellen und humanen Tumorproben sind sowohl EHMT2 als auch MBLAC2 in kolorektalen Tumoren konsistent häufiger vorhanden als im normalen Kolongewebe, parallel zu Markern erhöhter Ribosomenbildung. Die Unterdrückung von EHMT2 in kolorektalen Krebszellen verlangsamt das Tumorwachstum in Mäusen, reduziert ribosomale Marker und senkt die MBLAC2‑Spiegel. Patientendaten aus dem Cancer Genome Atlas zeigen, dass eine höhere Expression beider Gene mit fortgeschrittenerer Erkrankung und schlechterem Überleben nach Radiotherapie einhergeht. Zusammengenommen deuten diese Beobachtungen darauf hin, dass Krebszellen möglicherweise die EHMT2–MBLAC2‑Achse kapern, um rDNA‑Schäden besser zu tolerieren und die für unkontrolliertes Wachstum benötigte Ribosomenproduktion aufrechtzuerhalten.
Was das für Gesundheit und Therapie bedeutet
Für eine nichtfachliche Leserschaft lautet die Kernbotschaft: Unsere Zellen haben eine spezialisierte Notbremse im Nukleolus entwickelt: Wenn die DNA‑Vorlage für Ribosomen bricht, helfen EHMT2 und sein Partner MBLAC2, die Fabrik kurzfristig zu stoppen, die Reparatur zu lenken und die Stabilität wiederherzustellen. Wenn diese Notbremse bei kolorektalem Krebs überaktiv oder missbraucht wird, scheint sie Tumorzellen zu helfen, Stress und Behandlung besser zu überstehen. Durch das gezielte Anvisieren von EHMT2, MBLAC2 oder ihrer Wechselwirkung könnten künftige Therapien die Fähigkeit von Krebszellen, mit Schäden an der ribosomalen DNA umzugehen, selektiv schwächen und so gängige Behandlungen wie Chemotherapie und Radiotherapie wirksamer machen, während gesundes Gewebe geschont wird.
Zitation: Wang, C., Lu, Q., Cao, L. et al. The EHMT2-MBLAC2 axis suppresses ribosomal DNA transcription in response to nucleolar DNA damage. Cell Death Dis 17, 320 (2026). https://doi.org/10.1038/s41419-026-08616-1
Schlüsselwörter: Schäden an ribosomaler DNA, Nukleolarer Stress, EHMT2‑MBLAC2‑Signalweg, kolorektales Karzinom, DNA‑Reparatur und Transkription