Clear Sky Science · pt
Eixo EHMT2-MBLAC2 suprime a transcrição do DNA ribossomal em resposta a danos ao DNA nucleolar
Por que as fábricas de proteínas da célula precisam de proteção
Dentro de cada uma de nossas células existe uma oficina movimentada chamada nucléolo, onde são montadas as máquinas moleculares que produzem proteínas — os ribossomos. Como essa fábrica funciona quase sem interrupção, seu molde de DNA fica sob tensão constante e pode se quebrar. O estudo descrito neste artigo investiga como as células silenciam temporariamente essa fábrica para reparar danos, e como a falha nesse sistema de segurança pode contribuir para o desenvolvimento do câncer colorretal.
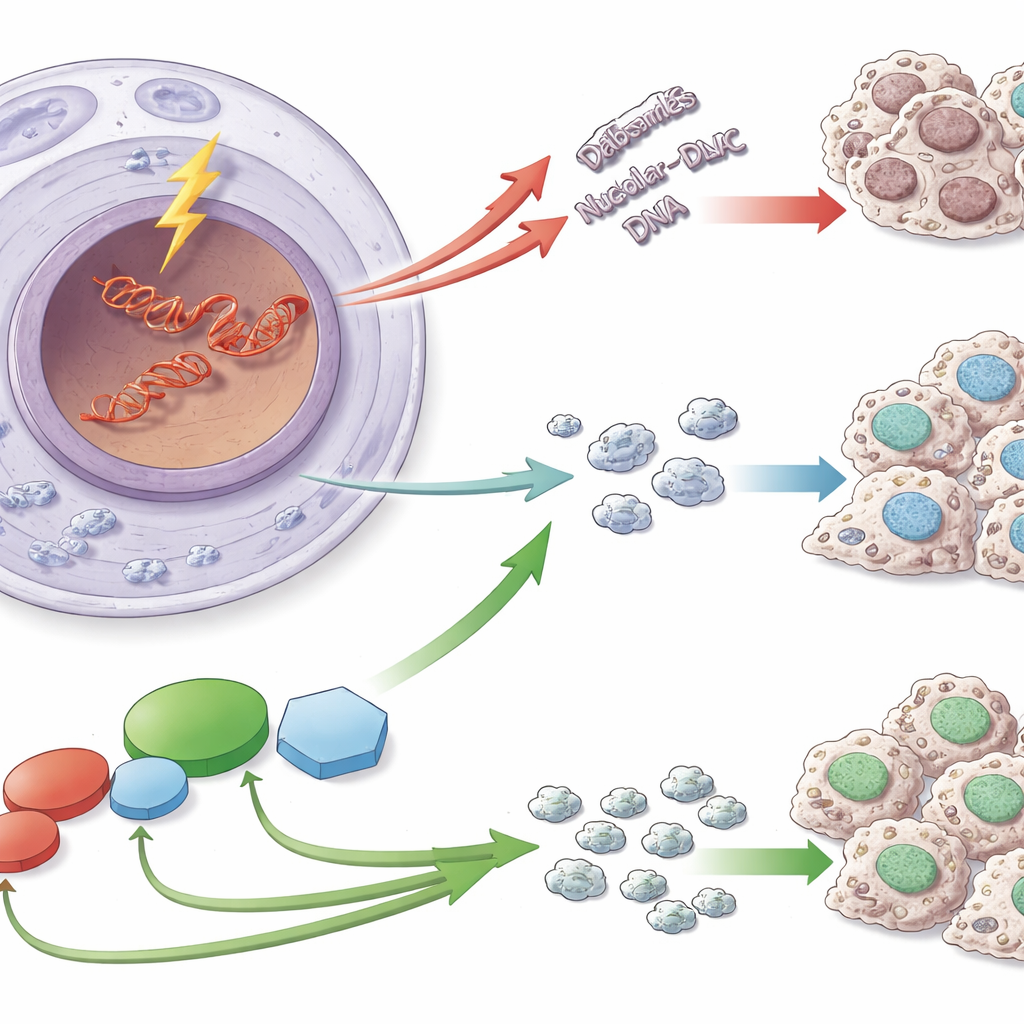
Um trecho vulnerável do DNA
Os ribossomos são montados a partir de instruções codificadas em segmentos especiais de DNA conhecidos como DNA ribossomal (rDNA). Essas sequências são repetidas muitas vezes e são copiadas em alta velocidade, o que as torna especialmente propensas a quebras de dupla hélice perigosas. Quando tais quebras ocorrem no rDNA, as células fazem mais do que apenas remendar o DNA: elas também reorganizam o nucléolo e suspendem brevemente a cópia do rDNA em RNA. Essa pausa evita que as máquinas de reparo colidam com a maquinaria de transcrição e ajuda a manter o número e a estrutura das repetições de rDNA estáveis — uma salvaguarda importante, porque a instabilidade do rDNA tem sido associada ao envelhecimento e a muitas doenças, incluindo o câncer.
Um novo interruptor de segurança no nucléolo
Os pesquisadores identificam uma proteína chamada EHMT2, mais conhecida por modificar a cromatina em outras regiões do genoma, como um ator crucial nessa resposta de segurança nucleolar. Usando um sistema em células humanas que corta o rDNA em locais definidos, eles mostram que o EHMT2 corre até a borda do nucléolo, onde o rDNA danificado é reunido em estruturas chamadas “caps”. Ali, o EHMT2 é necessário para desligar a produção de RNA ribossomal após o dano. Quando o EHMT2 está ausente ou sua atividade é bloqueada quimicamente, as células continuam a transcrever o rDNA apesar das quebras. A equipe rastreia esse efeito à habilidade do EHMT2 de adicionar uma marca química específica às histonas no rDNA danificado, ajudando a criar um estado de cromatina mais reprimido.
Ligando a pausa da transcrição ao reparo do DNA
Silenciar o rDNA é apenas metade da história; o reparo bem-sucedido precisa ocorrer em seguida. Os autores descobrem que células sem EHMT2 têm dificuldade em reparar quebras no rDNA: fragmentos de DNA persistem por mais tempo, pequenos núcleos extras (um sinal de instabilidade genômica) aparecem com mais frequência, e o número de cópias de rDNA diminui ao longo do tempo. De modo importante, uma via de reparo principal — junção de extremidades não homóloga (NHEJ), que sela rapidamente as pontas do DNA — não é recrutada adequadamente para os caps de rDNA sem EHMT2, embora outras rotas de reparo permaneçam em grande parte intactas. Como resultado, células deficientes em EHMT2 tornam-se hipersensíveis ao dano nucleolar e perdem a capacidade de formar colônias saudáveis após o corte do rDNA.
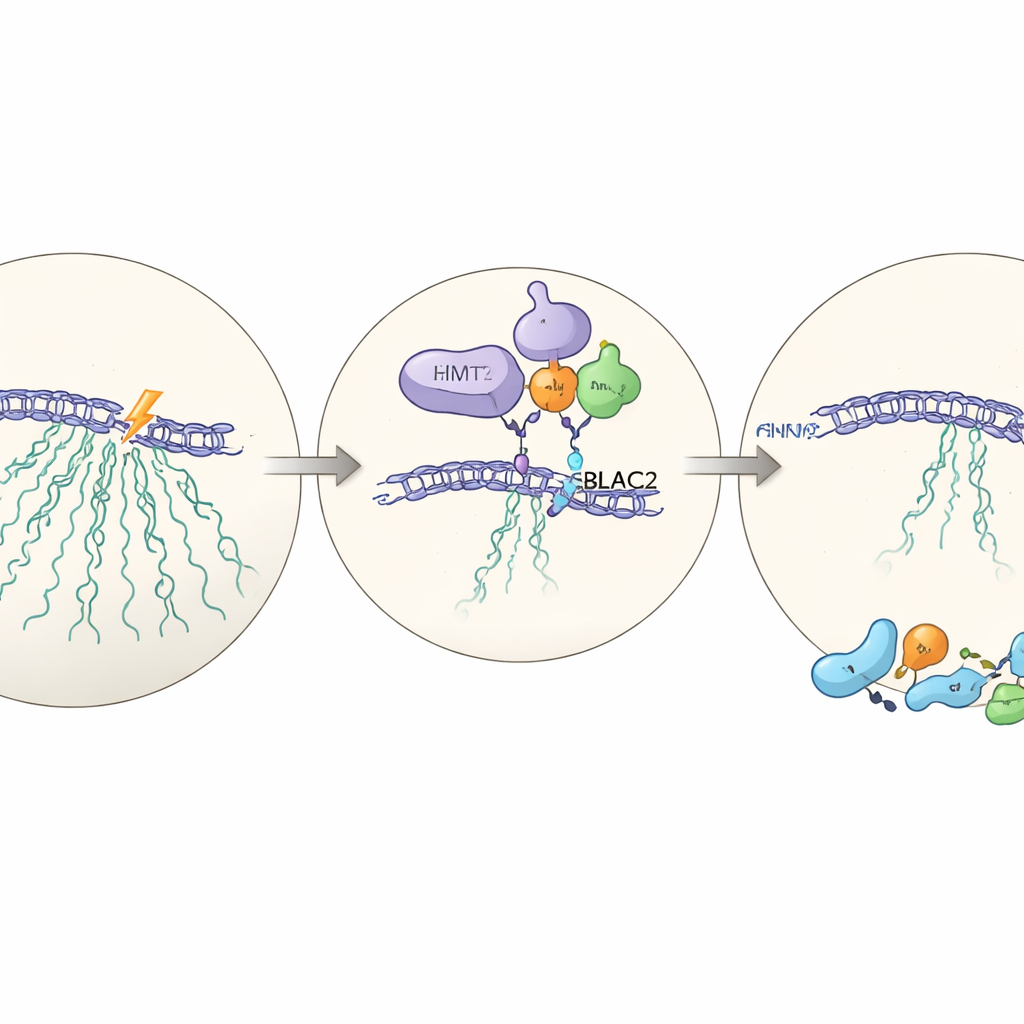
Um parceiro oculto: MBLAC2
Para entender como o EHMT2 exerce sua influência, a equipe realiza medições em grande escala de proteínas em células com e sem EHMT2. Entre as proteínas que diminuem quando o EHMT2 está ausente, uma se destaca: MBLAC2, uma enzima pouco estudada normalmente enriquecida no nucléolo. Quando o MBLAC2 é reduzido com ferramentas de RNA direcionadas, as células novamente falham em silenciar o rDNA após o dano e se tornam menos capazes de sobreviver a ele. O EHMT2 se liga fisicamente ao MBLAC2 e o estabiliza ao nível proteico; sem o EHMT2, o MBLAC2 é degradado mais rapidamente. Remover ambas as proteínas não agrava o efeito além de remover apenas uma, sugerindo que elas atuam na mesma via — um eixo EHMT2–MBLAC2 recém-descrito que coordena a pausa da transcrição com o reparo eficaz.
Do DNA danificado ao câncer colorretal
Como a instabilidade do rDNA é uma característica de muitos tumores, os autores investigam se esse eixo desempenha um papel no câncer colorretal, uma doença que depende fortemente da produção aumentada de ribossomos. Em modelos de camundongo e amostras de tumores humanos, tanto o EHMT2 quanto o MBLAC2 são consistentemente mais abundantes em tumores colorretais do que no tecido normal do cólon, em paralelo com marcadores de produção ribossomal aumentada. Suprimir o EHMT2 em células de câncer colorretal retarda o crescimento de tumores em camundongos, reduz marcadores relacionados a ribossomos e diminui os níveis de MBLAC2. Dados de pacientes do The Cancer Genome Atlas revelam que maior expressão de ambos os genes se associa a doença mais avançada e pior sobrevida após radioterapia. Em conjunto, essas observações sugerem que células cancerosas podem sequestrar a via EHMT2–MBLAC2 para tolerar melhor danos ao rDNA e manter a produção de ribossomos necessária ao crescimento descontrolado.
O que isso significa para a saúde e a terapia
Para um leitor leigo, a mensagem-chave é que nossas células evoluíram um freio de emergência dedicado dentro do nucléolo: quando o molde de DNA para ribossomos se quebra, o EHMT2 e seu parceiro MBLAC2 ajudam a pausar a fábrica, guiar o reparo e restaurar a estabilidade. Quando esse freio está excessivamente ativo ou é utilizado de forma indevida no câncer colorretal, parece ajudar as células tumorais a sobreviver ao estresse e ao tratamento. Ao direcionar o EHMT2, o MBLAC2 ou a interação entre eles, terapias futuras podem enfraquecer seletivamente a capacidade das células cancerosas de lidar com danos ao DNA ribossomal, tornando tratamentos padrão como quimioterapia e radioterapia mais eficazes enquanto poupam o tecido normal.
Citação: Wang, C., Lu, Q., Cao, L. et al. The EHMT2-MBLAC2 axis suppresses ribosomal DNA transcription in response to nucleolar DNA damage. Cell Death Dis 17, 320 (2026). https://doi.org/10.1038/s41419-026-08616-1
Palavras-chave: danos ao DNA ribossomal, estresse nucleolar, via EHMT2 MBLAC2, câncer colorretal, reparo do DNA e transcrição